早教吧作业答案频道 -->化学-->
在已经发现的一百多种元素中,除稀有气体外,非金属元素只有十多种,但与生产生活有密切的联系.(1)为了提高煤的利用率,常将其气化为可燃性气体,主要反应是碳和水蒸气反应生
题目详情
在已经发现的一百多种元素中,除稀有气体外,非金属元素只有十多种,但与生产生活有密切的联系.
(1)为了提高煤的利用率,常将其气化为可燃性气体,主要反应是碳和水蒸气反应生成水煤气,化学反应方程式为___,其中氧化剂是___.
(2)氮是动植物生长不可缺少的元素,合成氨的反应对人类解决粮食问题贡献巨大,反应如下:N2(g)+3H2(g)
2NH3(g).
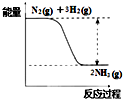
①合成氨的反应中的能量变化如图所示.该反应是___反应(填“吸热”或“放热”),其原因是反应物化学键断裂吸收的总能量___(填“大于”或“小于”)生成物化学键形成放出的总能量.
②在一定条件下,将一定量的N2和H2的混合气体充入某定容密闭容器中,一段时间后,下列叙述能说明该反应达到平衡状态的是___(填序号).
A.容器中混合气体的密度不随时间变化 B.断裂3mol H-H键的同时形成6mol N-H键
C. N2、H2、NH3的物质的量之比为1:3:2 D.容器中的压强不随时间变化
(3)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压.高铁电池的总反应为:3Zn+2K2FeO4+8H2O
3Zn(OH)2+2Fe(OH)3+4KOH
则高铁电池的负极材料是___,放电时,正极发生___(填“氧化”或“还原”)反应.

(1)为了提高煤的利用率,常将其气化为可燃性气体,主要反应是碳和水蒸气反应生成水煤气,化学反应方程式为___,其中氧化剂是___.
(2)氮是动植物生长不可缺少的元素,合成氨的反应对人类解决粮食问题贡献巨大,反应如下:N2(g)+3H2(g)
| 高温高压 |
| |
| 催化剂 |
①合成氨的反应中的能量变化如图所示.该反应是___反应(填“吸热”或“放热”),其原因是反应物化学键断裂吸收的总能量___(填“大于”或“小于”)生成物化学键形成放出的总能量.
②在一定条件下,将一定量的N2和H2的混合气体充入某定容密闭容器中,一段时间后,下列叙述能说明该反应达到平衡状态的是___(填序号).
A.容器中混合气体的密度不随时间变化 B.断裂3mol H-H键的同时形成6mol N-H键
C. N2、H2、NH3的物质的量之比为1:3:2 D.容器中的压强不随时间变化
(3)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压.高铁电池的总反应为:3Zn+2K2FeO4+8H2O
| 放电 |
| |
| 充电 |
则高铁电池的负极材料是___,放电时,正极发生___(填“氧化”或“还原”)反应.
▼优质解答
答案和解析
(1)C与水反应生成CO和氢气,反应为C(s)+H2O(g)
CO (g)+H2(g),水中H元素的化合价降低,则氧化剂为H2O,
故答案为:C(s)+H2O(g)
CO (g)+H2(g);H2O;
(2)①由图可知,反应物的总能量大于生成物的总能量,则该反应为放热反应,断裂化学键吸收能量,生成化学键释放能量,△H=断裂化学键吸收能量-生成化学键释放能量<0,可知断裂化学键吸收能量小于生成化学键释放能量,
故答案为:放热;小于;
②A.体积不变,质量守恒,则密度始终不变,所以不能判断平衡状态,故A错误;
B.断裂3mol H-H键,表示正速率,形成6mol N-H键表示正速率,都是正速率不能判断平衡状态,故B错误;
C. N2、H2、NH3的物质的量之比为1:3:2,取决起始浓度与转化率,不能判断平衡状态,故C错误;
D.该反应为反应前后气体物质的量不等的反应,则容器中的压强不随时间变化,可知反应达到平衡状态,故D正确;
故答案为:D;
(3)原电池负极上失电子化合价升高而发生氧化反应,所以Zn为负极;放电时,正极上K2FeO4得电子发生还原反应;
故答案为:Zn;还原.
| ||
故答案为:C(s)+H2O(g)
| ||
(2)①由图可知,反应物的总能量大于生成物的总能量,则该反应为放热反应,断裂化学键吸收能量,生成化学键释放能量,△H=断裂化学键吸收能量-生成化学键释放能量<0,可知断裂化学键吸收能量小于生成化学键释放能量,
故答案为:放热;小于;
②A.体积不变,质量守恒,则密度始终不变,所以不能判断平衡状态,故A错误;
B.断裂3mol H-H键,表示正速率,形成6mol N-H键表示正速率,都是正速率不能判断平衡状态,故B错误;
C. N2、H2、NH3的物质的量之比为1:3:2,取决起始浓度与转化率,不能判断平衡状态,故C错误;
D.该反应为反应前后气体物质的量不等的反应,则容器中的压强不随时间变化,可知反应达到平衡状态,故D正确;
故答案为:D;
(3)原电池负极上失电子化合价升高而发生氧化反应,所以Zn为负极;放电时,正极上K2FeO4得电子发生还原反应;
故答案为:Zn;还原.
看了在已经发现的一百多种元素中,除...的网友还看了以下:
碳酸钠溶液可以和稀盐酸溶液反应,我们可以有两种方式进行反应.1)将稀盐酸溶液慢慢地滴入碳酸钠溶液中; 2020-03-30 …
将碳和碳酸钙的混合物在空气中充分灼烧后,碳酸钙完全反应,碳也完全氧化.若生成 将碳和碳酸钙的混合物 2020-05-16 …
在一氧化碳还原氧化铜的实验中(非计算)要将玻璃导管伸入试管底部,并在加热前先通入片刻一氧化碳气体, 2020-05-21 …
碳酸铵及碳酸氢铵和氢氧化钠加热反应将碳酸氢铵和碳酸铵配成水溶液,然后加入足量氢氧化钠并加热,请问化 2020-06-29 …
实验室将A装置加以改动,在高温下是碳酸钙分解生成氧化钙和二氧化碳,(CaCO3高温.CaO+CO2 2020-07-21 …
已知黑火药的爆炸反应是S+2KNO3+3C→K2S+N2↑+3CO2↑,由此可知1molKNO3可氧 2020-11-03 …
下面关于光合作用的有关叙述,错误的是()A.光反应产生的NADPH也是碳反应中将CO2还原为糖的直接 2020-11-13 …
碳需要积多少热量才能把二氧化碳还原一氧化碳,根据方程式:2C+CO2=2CO—172.5kj则有2M 2020-11-16 …
干粉灭火器喷射出来的干粉主要是碳酸氢钠,该物质受热分解生成碳酸钠、水和二氧化碳;二氧化碳可将燃烧物与 2020-11-16 …
将碳酸钠和碳酸氢钠分别加热,可发生分解反应的是,反应的化学方程式.鉴别碳酸钠和碳酸氢钠的溶液,可用氯 2021-02-09 …