早教吧作业答案频道 -->化学-->
草酸(H2C2O4)溶液与酸性KMnO4溶液反应时,溶液褪色总是先慢后快.某学习小组结合化学反应原理提出猜想与假设,并设计了一系列实验进行探究.实验Ⅰ:在2支试管中分别加入5mL等浓度的H
题目详情
草酸(H2C2O4)溶液与酸性KMnO4溶液反应时,溶液褪色总是先慢后快.某学习小组结合化学反应原理提出猜想与假设,并设计了一系列实验进行探究.
实验Ⅰ:在2支试管中分别加入5mL等浓度的H2C2O4溶液,在其中一支试管中先加入少量MnSO4固体再各加入5滴0.1mol•L-1KMnO4溶液.记录溶液褪色时间,如表1:
[表1]
实验Ⅱ:另取2支试管分别加入5mL等浓度的H2C2O4溶液,在其中一支试管中先加入10滴稀硫酸,再各加入5滴0.1mol•L-1 KMnO4溶液.记录溶液褪色时间,如表2:
[表2]
实验Ⅲ:另取3支试管分别加入5mL等浓度H2C2O4溶液,然后在试管中先分别加入10滴、1mL、2mL稀硫酸溶液,再各加入5滴0.1mol•L-1KMnO4溶液,然后置于温度为65℃的水浴中加热.记录溶液褪色时间,如表3:
[表3]
(1)实验Ⅰ得出的结论是___.
(2)比较实验Ⅱ、Ⅲ得出的结论正确的是:___.
①温度对该反应速率有影响
②硫酸对草酸和KMnO4溶液的反应有影响
③加入少量硫酸,可促进草酸和KMnO4溶液反应,而加入大量硫酸,反应速率比较小
④在酸性范围内,pH值越小对反应越有利
(3)写出草酸溶液与酸性KMnO4溶液反应的离子方程式:___.实验室利用该反应标定未知浓度H2C2O4溶液,滴定终点的现象是:溶液颜色___,且30s不改变.滴定完成后仰视读取KMnO4溶液体积会导致测得H2C2O4溶液的浓度___(选填:偏大、偏小、无影响).
(4)有同学根据查阅的资料提出KMnO4溶液氧化H2C2O4的反应历程为:
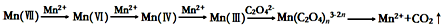
上述实验中,实验___可证明这个历程是可信的.
实验Ⅰ:在2支试管中分别加入5mL等浓度的H2C2O4溶液,在其中一支试管中先加入少量MnSO4固体再各加入5滴0.1mol•L-1KMnO4溶液.记录溶液褪色时间,如表1:
| 试 管 | 未加MnSO4的试管 | 加有MnSO4的试管 |
| 褪色时间 | 30s | 2s |
实验Ⅱ:另取2支试管分别加入5mL等浓度的H2C2O4溶液,在其中一支试管中先加入10滴稀硫酸,再各加入5滴0.1mol•L-1 KMnO4溶液.记录溶液褪色时间,如表2:
| 试 管 | 未滴加稀硫酸的试管 | 滴加了稀硫酸的试管 |
| 褪色时间 | 100s | 90s |
实验Ⅲ:另取3支试管分别加入5mL等浓度H2C2O4溶液,然后在试管中先分别加入10滴、1mL、2mL稀硫酸溶液,再各加入5滴0.1mol•L-1KMnO4溶液,然后置于温度为65℃的水浴中加热.记录溶液褪色时间,如表3:
| 试 管 | 滴入10滴稀硫酸的试管 | 加入1mL稀硫酸的试管 | 加入2mL稀硫酸的试管 |
| 褪色时间 | 70s | 100s | 120s |
(1)实验Ⅰ得出的结论是___.
(2)比较实验Ⅱ、Ⅲ得出的结论正确的是:___.
①温度对该反应速率有影响
②硫酸对草酸和KMnO4溶液的反应有影响
③加入少量硫酸,可促进草酸和KMnO4溶液反应,而加入大量硫酸,反应速率比较小
④在酸性范围内,pH值越小对反应越有利
(3)写出草酸溶液与酸性KMnO4溶液反应的离子方程式:___.实验室利用该反应标定未知浓度H2C2O4溶液,滴定终点的现象是:溶液颜色___,且30s不改变.滴定完成后仰视读取KMnO4溶液体积会导致测得H2C2O4溶液的浓度___(选填:偏大、偏小、无影响).
(4)有同学根据查阅的资料提出KMnO4溶液氧化H2C2O4的反应历程为:
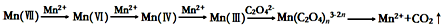
上述实验中,实验___可证明这个历程是可信的.
▼优质解答
答案和解析
(1)根据表中数据知,有硫酸锰的溶液褪色时间短,反应速率快,没有硫酸锰的溶液褪色时间长、反应速率慢,说明硫酸锰作催化剂而加快反应速率,故答案为:Mn2+(或硫酸锰)在反应中起到催化剂的作用,加快了反应速率[或需要Mn2+(硫酸锰)作催化剂];
(2)①根据实验II、III知,温度不同其褪色时间不同,说明温度对该反应速率有影响,故①正确;
②根据实验III知,混合溶液中硫酸浓度不同其褪色时间不同,说明硫酸对草酸和KMnO4溶液的反应有影响,故②正确;
③根据实验III知,加入少量硫酸,可促进草酸和KMnO4溶液反应,褪色时间变短,而加入大量硫酸,反应速率比较小,褪色时间加长,故③正确;
④根据实验三知,在酸性范围内,pH值越小褪色时间越长,则对反应越不利,故④错误;
故答案为:①②③;
(3)酸性条件下,高锰酸钾具有强氧化性,能氧化还原性物质,所以草酸和高锰酸钾发生氧化还原反应生成硫酸锰、二氧化碳和水,离子方程式为5H2C2O4+2MnO4-+6H+=2Mn2++10CO2↑+8H2O,导致溶液褪色,所以当溶液由无色变为紫红色且半分钟内不变色时,说明达到滴定终点;滴定完成后仰视读取KMnO4溶液体积会导致高锰酸钾溶液体积偏大,则导致测定溶液浓度偏大;
故答案为:5H2C2O4+2MnO4-+6H+=2Mn2++10CO2↑+8H2O;从无色变为浅紫红色;偏大;
(4)根据流程图知,酸性高锰酸钾被还原生成二价锰离子,导致溶液褪色,且开始时既有锰离子参加反应,只有实验I中加入硫酸锰,所以实验I可证明这个历程是可信的,
故答案为:I.
(2)①根据实验II、III知,温度不同其褪色时间不同,说明温度对该反应速率有影响,故①正确;
②根据实验III知,混合溶液中硫酸浓度不同其褪色时间不同,说明硫酸对草酸和KMnO4溶液的反应有影响,故②正确;
③根据实验III知,加入少量硫酸,可促进草酸和KMnO4溶液反应,褪色时间变短,而加入大量硫酸,反应速率比较小,褪色时间加长,故③正确;
④根据实验三知,在酸性范围内,pH值越小褪色时间越长,则对反应越不利,故④错误;
故答案为:①②③;
(3)酸性条件下,高锰酸钾具有强氧化性,能氧化还原性物质,所以草酸和高锰酸钾发生氧化还原反应生成硫酸锰、二氧化碳和水,离子方程式为5H2C2O4+2MnO4-+6H+=2Mn2++10CO2↑+8H2O,导致溶液褪色,所以当溶液由无色变为紫红色且半分钟内不变色时,说明达到滴定终点;滴定完成后仰视读取KMnO4溶液体积会导致高锰酸钾溶液体积偏大,则导致测定溶液浓度偏大;
故答案为:5H2C2O4+2MnO4-+6H+=2Mn2++10CO2↑+8H2O;从无色变为浅紫红色;偏大;
(4)根据流程图知,酸性高锰酸钾被还原生成二价锰离子,导致溶液褪色,且开始时既有锰离子参加反应,只有实验I中加入硫酸锰,所以实验I可证明这个历程是可信的,
故答案为:I.
看了草酸(H2C2O4)溶液与酸性...的网友还看了以下:
硝酸溶液(1+4)和硝酸溶液(1+9)有什么区别?今天看了一本食品分析的书上面的硝酸溶液有(1+4 2020-05-17 …
PH=13的强碱和PH=2的强酸混合所得的溶液PH=11那么强酸与强碱的体积之比PH=4的盐酸和P 2020-05-23 …
请问:pH3.0和pH7.4的磷酸-柠檬酸缓冲液如何配制?最好是同种浓度的磷酸/柠檬酸分别配制这两 2020-06-03 …
将氯水分别加入到下列溶液中,观察有何现象?写出有关反应的离子方程式。(1)紫色石蕊试液;(2)氯化 2020-06-12 …
区别下列有关物质的描述不正确的是[]A.用溴水区别甲烷和乙烯B.用碳酸钠溶液区别乙酸和乙酸乙酯C. 2020-06-27 …
下列鉴别物质的方法能达到目的是()A.用Ba(N03)2溶液鉴别CaCl2溶液和(NH4)2SO4 2020-06-29 …
下列物质的鉴别方法不可行的是()A.用燃烧法鉴别棉线和羊毛线B.用稀盐酸鉴别硫酸铵和硫酸钾C.用石蕊 2020-11-03 …
下列有关实验的叙述不正确的是()A.可用酸性高锰酸钾溶液检验中的醛基B.可用新制的银氨溶液鉴别乙酸甲 2020-11-03 …
勇往直前学习小组的同学到实验室完成《实验活动4溶液酸碱性的检验》.探究实验一自制指示剂如图所示,同学 2021-01-01 …
有甲、乙、丙、丁4瓶无色溶液,它们分别是(1)稀盐酸;(2)稀硫酸;(3)氢氧化钠溶液;(4)硫酸钠 2021-01-20 …