(1)下列六种晶体:①CO2,②NaCl,③Na,④Si,⑤CS2,⑥金刚石,它们的熔点从低到高的顺序为熔化时不需破坏化学键的是,熔化时只需破坏共价键的是
(1)下列六种晶体:①CO 2 ,②NaCl,③Na,④Si,⑤CS 2 ,⑥金刚石,它们的熔点从低到高的顺序为 熔化时不需破坏化学键的是 ,熔化时只需破坏共价键的是 (填序号).
(2)在①H 2 、②(NH 4 ) 2 SO 4 、③SiC、④CO 2 、⑤HF中,由极性键形成的非极性分子有 ,由非极性键形成的非极性分子有 ,能形成分子晶体的物质是 ,含有氢键的晶体的化学式是 ,属于离子晶体的是 ,属于原子晶体的是 .(填序号)
(3)如图表示一些晶体的结构中的某一部分.
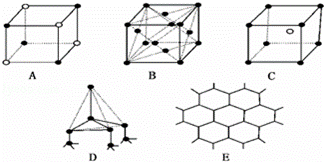
①代表金刚石的是(填编号字母,下同) ,其中每个碳原子与 个碳原子最接近且距离相等.
②代表NaCl的是 ,每个Na + 周围与它最接近且距离相等的Na + 有 个.
③代表CsCl的是 ,每个Cs + 与 个Cl ﹣ 紧邻.
④代表干冰的是 ,每个CO 2 分子与 个CO 2 分子紧邻.
⑤代表石墨的是 ,它属于 晶体.
考点 :
晶胞的计算;共价键的形成及共价键的主要类型;晶体的类型与物质熔点、硬度、导电性等的关系;不同晶体的结构微粒及微粒间作用力的区别.
专题 :
化学键与晶体结构.
分析:
(1)熔点高低顺序为:原子晶体>离子晶体>金属晶体>分子晶体,分子晶体中,其熔点与相对分子质量成正比,原子晶体熔点高低与其原子半径成反比;分子晶体熔化时不需破坏化学键,原子晶体熔化时只需破坏共价键;
(2)同种非金属元素之间形成非极性键,不同非金属元素之间易形成极性键,分子中正负电荷重心重合的分子为非极性键分子,正负电荷重心不重合的分子为非极性分子;由离子构成的晶体为离子晶体,由分子构成的晶体为分子晶体,由原子构成的晶体属于原子晶体;
(3)①金刚石中每个碳原子和其余四个原子形成正四面体结构;
②NaCl属于离子晶体,其阴阳离子配位数是6;
③CsCl属于离子晶体,其阴阳离子配位数是8;
④干冰属于分子晶体,根据晶胞结构判断;
⑤石墨晶体中,每一层中每个C原子和相邻3个C原子相连,层和层之间存在分子间作用力.
(1)晶体熔点高低顺序是:原子晶体>离子晶体>金属晶体>分子晶体,分子晶体的熔点与其相对分子质量成正比,二氧化碳属于分子晶体、NaCl属于离子晶体、Na属于金属晶体、Si属于原子晶体、二硫化碳属于分子晶体、金刚石属于原子晶体,原子晶体的熔点与其原子半径成反比,所以它们的熔点从低到高顺序是 ①<⑤<③<②<④<⑥;
分子晶体熔化时不需破坏化学键,所以熔化时不需破坏化学键①⑤,原子晶体熔化时只需破坏共价键,熔化时只需破坏共价键的是④⑥;
故答案为:①<⑤<③<②<④<⑥;①⑤;④⑥;
(2)①H 2 中只存在非极性键,属于非极性分子,为分子晶体;
②(NH 4 ) 2 SO 4 中存在离子键、极性键,为离子晶体;
③SiC中只存在极性键,为原子晶体;
④CO 2 中只存在极性键,属于非极性分子,为分子晶体;
⑤HF中只存在极性键,属于极性分子,为分子晶体,还含有氢键,
所以由极性键形成的非极性分子有④,由非极性键形成的非极性分子有①,能形成分子晶体的物质是①④⑤,含有氢键的晶体的化学式是⑤,属于离子晶体的是②,属于原子晶体的是③;
故答案为:④;①;①④⑤;⑤;②;③;
(3)①金刚石中每个碳原子和其余四个原子形成正四面体结构,代表金刚石的是D,故答案为:D;4;
②NaCl属于离子晶体,其阴阳离子配位数是6,A代表氯化钠,每个Na + 周围与它最接近且距离相等的Na + 有12,故答案为:A;12;
③CsCl属于离子晶体,其阴阳离子配位数是8,代表CsCl的是C,根据图片知,每个Cs + 与8个Cl ﹣ 紧邻,故答案为:C;8;
④干冰属于分子晶体,代表干冰的是B,每个CO 2 分子紧邻的CO 2 分子个数=3×8× ![]() =12,故答案为:B;12;
=12,故答案为:B;12;
⑤石墨晶体中,每一层中每个C原子和相邻3个C原子相连,层和层之间存在分子间作用力,代表石墨的是E,属于混合晶体,故答案为:E;混合晶体.
点评:
本题考查物质结构和性质,从晶胞的计算、熔点高低判断、晶体类型的判断方面考查,熟练掌握典型晶体结构,会根据物质构成微粒判断晶体类型,难点是配位数的计算,题目难度中等.
公安机关要依法坚决打击、制裁那些扰乱、破坏( )和人民群众生活秩序的违法犯罪行为。A.社会秩序B.生 2020-05-19 …
Windows中“磁盘碎片整理程序”的主要作用是_____。A.修复损坏的磁盘B.修复损坏的磁盘碎片 2020-05-23 …
用快速排序的方法对包含n个关键字的序列进行排序,最坏情况下执行的时间为A.O(n)B.O(log2n 2020-05-24 …
计算机病毒主要造成()A.磁盘损坏B.计算机用户的伤害C.CPU的损坏D.程序和数据的破坏 2020-05-26 …
产生系统更新的原因是______。A.对操作系统的漏洞进行修补B.某个应有程序的破坏进行修补C.要更 2020-05-26 …
()是指编制者在计算机程序中插入的破坏计算机功能或者毁坏数据,影响计算机使用,并能够自我复制的 2020-05-26 …
计算机病毒是指编造者在计算机程序中插入的破坏计算机功能或者毁坏数据、影响计算机使用,并能 2020-05-26 …
破坏金融管理秩序罪,是指违反国家金融管理法规,破坏国家对金融管理秩序的行为。 2020-05-27 …
()攻击是指通过向程序的缓冲区写入超出其长度的内容,从而破坏程序的堆栈,使程序转而去执行其他的指令, 2020-05-31 …
二叉树顺序遍历问题!找出所有二叉树,其节点在下列两种次序下恰好都以同样的次序出现.①先序和中序,② 2020-06-15 …