早教吧作业答案频道 -->化学-->
CuCl和CuCl2都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等.已知:①CuCl可以由CuCl2用适当的还原剂如SO2、SnCl2等还原制得:2Cu2++2Cl-+SO2+2H2O═2CuCl↓+4H++SO42-2CuCl+SnCl2═2CuCl↓+SnCl4
题目详情
CuCl和CuCl2都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等.已知:
①CuCl可以由CuCl2用适当的还原剂如SO2、SnCl2等还原制得:
2Cu2++2Cl-+SO2+2H2O═2CuCl↓+4H++SO42-
2CuCl+SnCl2═2CuCl↓+SnCl4
②CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子[Cu(En)2]2+(En是乙二胺的简写):
请回答下列问题:
(1)配离子[Cu(En)2]2+的中心原子基态外围电子排布式为___,H、N、O三种元素的电负性由大到小的顺序是___;
(2)SO2分子的空间构型为___;
(3)乙二胺分子中氮原子轨道的杂化类型为___,乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是___.
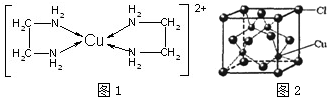
(4)如图1配离子[Cu(En)2]2+的配位数为___,该微粒含有的微粒间的作用力类型有___(填字母);
A.配位键 B.极性键 C.离子键 D.非极性键E.氢键 F.金属键
(5)CuCl的晶胞结构如图2所示,其中Cl-的配位数(即与Cl-最近距离的Cu+的个数)为___.
①CuCl可以由CuCl2用适当的还原剂如SO2、SnCl2等还原制得:
2Cu2++2Cl-+SO2+2H2O═2CuCl↓+4H++SO42-
2CuCl+SnCl2═2CuCl↓+SnCl4
②CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子[Cu(En)2]2+(En是乙二胺的简写):

请回答下列问题:
(1)配离子[Cu(En)2]2+的中心原子基态外围电子排布式为___,H、N、O三种元素的电负性由大到小的顺序是___;
(2)SO2分子的空间构型为___;
(3)乙二胺分子中氮原子轨道的杂化类型为___,乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是___.
(4)如图1配离子[Cu(En)2]2+的配位数为___,该微粒含有的微粒间的作用力类型有___(填字母);
A.配位键 B.极性键 C.离子键 D.非极性键E.氢键 F.金属键
(5)CuCl的晶胞结构如图2所示,其中Cl-的配位数(即与Cl-最近距离的Cu+的个数)为___.
▼优质解答
答案和解析
(1)Cu原子的核外电子排布式为1s22s22p63s23p63d104s1,故Cu2+的外围电子排布式为3d9;
同周期自左而右,电负性增大,电负性O>N,H元素与O、N元素化合时,H元素表现正化合价,H元素的电负性比O、N元素小,故电负性O>N>H;
故答案为:3d9;O>N>H;
(2)SO2分子的中心原子S原子的杂化轨道数为
=3,采取sp2杂化,含有1对孤对电子对,故SO2为V型结构;
故答案为:V型;
(3)乙二胺(H2N-CH2-CH2-NH2)中N原子呈3个σ键,含有1对孤对电子,杂化轨道数为4,采取sp3杂化;
乙二胺(H2N-CH2-CH2-NH2)分子之间可以形成氢键,三甲胺[N(CH3)3]分子之间不能形成氢键,故乙二胺的沸点较高;
故答案为:sp3杂化;乙二胺分子之间可以形成氢键,三甲胺分子之间不能形成氢键;
(4)由图1可知配离子[Cu(En)2]2+的配位数为4;
离子中存在配位键、C-N键、C-H键、N-H键、C-C键,其中C-N键、C-H键、N-H键为极性键,C-C键为非极性键,故离子含有配位键、极性键、非极性键,故选ABD;
故答案为:4;ABD;
(5)由CuCl的晶胞结构图可知,每个Cu+周围有4个Cl-,故每个Cl-周围有4个Cu+;故答案为:4.
同周期自左而右,电负性增大,电负性O>N,H元素与O、N元素化合时,H元素表现正化合价,H元素的电负性比O、N元素小,故电负性O>N>H;
故答案为:3d9;O>N>H;
(2)SO2分子的中心原子S原子的杂化轨道数为
| 6 |
| 2 |
故答案为:V型;
(3)乙二胺(H2N-CH2-CH2-NH2)中N原子呈3个σ键,含有1对孤对电子,杂化轨道数为4,采取sp3杂化;
乙二胺(H2N-CH2-CH2-NH2)分子之间可以形成氢键,三甲胺[N(CH3)3]分子之间不能形成氢键,故乙二胺的沸点较高;
故答案为:sp3杂化;乙二胺分子之间可以形成氢键,三甲胺分子之间不能形成氢键;
(4)由图1可知配离子[Cu(En)2]2+的配位数为4;
离子中存在配位键、C-N键、C-H键、N-H键、C-C键,其中C-N键、C-H键、N-H键为极性键,C-C键为非极性键,故离子含有配位键、极性键、非极性键,故选ABD;
故答案为:4;ABD;
(5)由CuCl的晶胞结构图可知,每个Cu+周围有4个Cl-,故每个Cl-周围有4个Cu+;故答案为:4.
看了CuCl和CuCl2都是重要的...的网友还看了以下:
要求:1、写出化学方应方程式;2、氧化还原反应,标出氧化剂还原剂;3、是离子反应的写出离子方程式1 2020-04-08 …
什么东西和氢氧化铝+硼酸能被水溶解这种试剂用做分析熔剂,里面有氢氧化铝还有硼酸,好像还有什么东西, 2020-05-14 …
请问:汽车喷漆用的油漆里需要添加什么呀!听说需要加固化剂和稀释剂,还需要加别的吗?添加比例是多少? 2020-05-16 …
对于化学反应,我们不但要考虑加入的试剂,还要考虑环境中的其他物质对化学反应的影响.教材中“木炭还原 2020-06-07 …
关于铁及铁的氧化物的转化1.请问是不是Fe3加强还原剂还原成Fe,加若还原剂还原成Fe2+?Fe2 2020-06-27 …
双氧水加洗涤剂还要加二氧化锰,请问实验过程是什么?二氧化锰可以用日常生活的什么代替? 2020-07-03 …
某城市污水处理厂进水流量Q=0.3m3/l、BOD=225mg/l、SS=230mg/l,还含有一 2020-07-09 …
羟胺(NH2OH)是一种还原剂,能将某些氧化剂还原.现用25.00ml0.049mol/L羟胺的酸 2020-07-25 …
关于氧化还原反应的一些问题1、氧化剂和还原剂指一个物质还是指这个物质里的某个元素?2、除了氧化剂> 2020-07-25 …
在进行除杂试验方案设计时除了要考虑所加试剂还要考虑什么 2021-01-04 …