早教吧作业答案频道 -->化学-->
实验室常用二氧化锰与浓盐酸来制备氯气,反应原理为:MnO2+4HCl(浓)△.MnCl2+Cl2↑+2H2O,实验
题目详情
实验室常用二氧化锰与浓盐酸来制备氯气,反应原理为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,实验装置如图1所示.
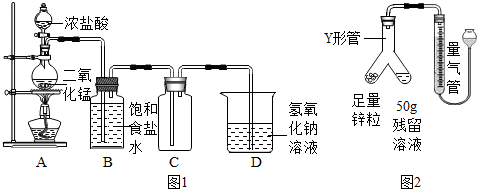
【查阅资料】
①氯气是黄绿色且有毒的气体,难溶于饱和食盐水;
②氯气能与氢氧化钠溶液反应,生成氯化钠、次氯酸钠(NaClO)和水;
③常温常压下,氢气的密度为0.09g/L.
【回答问题】
(1)装置B的作用为___;
(2)根据装置C判断,氯气的密度比空气___(填“大”或“小”);
(3)装置D的作用为___(用化学方程式表示)
【发现问题】
制备过程中,因盐酸浓度下降导致反应停止,某化学兴趣小组同学为测定装置A中反应后残余液中HCl的质量分数,提出两套测定方案如图3所示
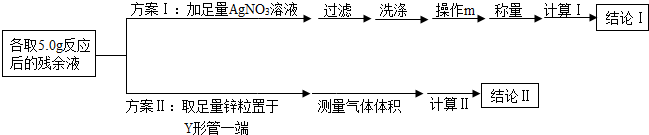
(4)方案Ⅰ中操作m的名称为___,通过称量生成沉淀的质量,计算出残余液中HCl的质量分数,此测定方案是___(填“可行”或“不可行”)的,原因是___;
(5)方案Ⅱ利用图2装置(固定仪器的装置已略)进行测定.
①实验过程中观察到锌粒表面有气泡产生,反应的化学方程式为___;
③当装置恢复至常温时,测得反应生成气体的体积为183.5mL,根据化学方程式计算,残余液中HCl的质量分数为多少?
【反思讨论】
(6)为了保证方案Ⅱ测定结果的准确性,正确操作是:倾斜Y形管,___(填标号)
A.将残余溶液转移到锌粒中 B.将锌粒转移到残余溶液中
(7)Y形管内空气对气体体积的测量___(填“有”或“没有”)影响.
| ||

【查阅资料】
①氯气是黄绿色且有毒的气体,难溶于饱和食盐水;
②氯气能与氢氧化钠溶液反应,生成氯化钠、次氯酸钠(NaClO)和水;
③常温常压下,氢气的密度为0.09g/L.
【回答问题】
(1)装置B的作用为___;
(2)根据装置C判断,氯气的密度比空气___(填“大”或“小”);
(3)装置D的作用为___(用化学方程式表示)
【发现问题】
制备过程中,因盐酸浓度下降导致反应停止,某化学兴趣小组同学为测定装置A中反应后残余液中HCl的质量分数,提出两套测定方案如图3所示

(4)方案Ⅰ中操作m的名称为___,通过称量生成沉淀的质量,计算出残余液中HCl的质量分数,此测定方案是___(填“可行”或“不可行”)的,原因是___;
(5)方案Ⅱ利用图2装置(固定仪器的装置已略)进行测定.
①实验过程中观察到锌粒表面有气泡产生,反应的化学方程式为___;
③当装置恢复至常温时,测得反应生成气体的体积为183.5mL,根据化学方程式计算,残余液中HCl的质量分数为多少?
【反思讨论】
(6)为了保证方案Ⅱ测定结果的准确性,正确操作是:倾斜Y形管,___(填标号)
A.将残余溶液转移到锌粒中 B.将锌粒转移到残余溶液中
(7)Y形管内空气对气体体积的测量___(填“有”或“没有”)影响.
▼优质解答
答案和解析
(1)二氧化锰与浓盐酸来制备氯气,制取的气体中常混有挥发出的氯化氢气体,装置B的作用为除去氯化氢气体;
(2)根据装置C判断,气体长进短出,说明气体的密度比空气大;
(3)氯气有毒,排放在空气中会造成污染,故用氢氧化钠溶液吸收,反应的方程式为:Cl2+2NaOH═NaCl+NaClO+H2O;
(4)方案Ⅰ:方案Ⅰ中操作m的名称为干燥;二氧化锰与浓盐酸反应生成氯化锰,也会与硝酸银反应,故不能用来测定残余液中盐酸的质量,反应不可行;
(5)①方案Ⅱ:将锌转移到残留溶液中,反应的方程式为:Zn+2HCl=ZnCl2+H2↑;
③ 设残余液中的HCl的质量为x
Zn+2HCl=ZnCl2+H2↑
73 2
x 0.09 g/L×0.1835 L
=
X=0.6 g
残余液中HCl的质量分数:
×100%=12.0%
答:残余液中的HCl的质量分数为12.0%;
(6)将锌转移到残留溶液中,反应完毕后,每间隔1分钟读取气体体积.气体体积逐渐减小,气体体积逐渐减小的原因是气体未冷却到室温,当温度冷却到室温后,气体体积不再改变;
(7)氢气的密度比空气小,故Y形管内空气对气体体积的测量没有影响.
故答案为:(1)除去氯气中混有的氯化氢气体
(2)大
(3)Cl2+2NaOH═NaCl+NaClO+H2O
(4)干燥(或烘干) 不可行
残余液中的MnCl2也能与AgNO3溶液反应生成沉淀,造成测量值偏大
(5)①Zn+2HCl=ZnCl2+H2↑
③ 设残余液中的HCl的质量为x
Zn+2HCl=ZnCl2+H2↑
73 2
x 0.09 g/L×0.1835 L
=
X=0.6 g
残余液中HCl的质量分数:
×100%=12.0%
答:残余液中的HCl的质量分数为12.0%.
(6)B (7)没有
(2)根据装置C判断,气体长进短出,说明气体的密度比空气大;
(3)氯气有毒,排放在空气中会造成污染,故用氢氧化钠溶液吸收,反应的方程式为:Cl2+2NaOH═NaCl+NaClO+H2O;
(4)方案Ⅰ:方案Ⅰ中操作m的名称为干燥;二氧化锰与浓盐酸反应生成氯化锰,也会与硝酸银反应,故不能用来测定残余液中盐酸的质量,反应不可行;
(5)①方案Ⅱ:将锌转移到残留溶液中,反应的方程式为:Zn+2HCl=ZnCl2+H2↑;
③ 设残余液中的HCl的质量为x
Zn+2HCl=ZnCl2+H2↑
73 2
x 0.09 g/L×0.1835 L
| 73 |
| x |
| 2 |
| 0.09g/l×0.1835l |
X=0.6 g
残余液中HCl的质量分数:
| 0.6g |
| 5g |
答:残余液中的HCl的质量分数为12.0%;
(6)将锌转移到残留溶液中,反应完毕后,每间隔1分钟读取气体体积.气体体积逐渐减小,气体体积逐渐减小的原因是气体未冷却到室温,当温度冷却到室温后,气体体积不再改变;
(7)氢气的密度比空气小,故Y形管内空气对气体体积的测量没有影响.
故答案为:(1)除去氯气中混有的氯化氢气体
(2)大
(3)Cl2+2NaOH═NaCl+NaClO+H2O
(4)干燥(或烘干) 不可行
残余液中的MnCl2也能与AgNO3溶液反应生成沉淀,造成测量值偏大
(5)①Zn+2HCl=ZnCl2+H2↑
③ 设残余液中的HCl的质量为x
Zn+2HCl=ZnCl2+H2↑
73 2
x 0.09 g/L×0.1835 L
| 73 |
| x |
| 2 |
| 0.09g/l×0.1835l |
X=0.6 g
残余液中HCl的质量分数:
| 0.6g |
| 5g |
答:残余液中的HCl的质量分数为12.0%.
(6)B (7)没有
看了实验室常用二氧化锰与浓盐酸来制...的网友还看了以下:
现用13.05G二氧化锰和100ML36.5%的弄盐酸反应实验室用二氧化锰和弄盐酸反应制取氧气,现 2020-04-26 …
过氧化钠(Na2O2)在常温下能与人呼出的二氧化碳反应生成氧气,化学方程式为:2Na2O2+2CO 2020-05-14 …
过氧化钠(Na2O2)在常温下能与人呼出的二氧化碳反应生成氧气,化学方程式为:2Na2O2+2CO 2020-05-14 …
实验室里通常用MnO2与浓盐酸反应制取氯气其反应的化学方程式为MnO2+4HCl(浓)加热=Cl2 2020-05-15 …
氧化还原反应实际上包含氧化反应和还原反应两个过程,11.(7分)(2011·南昌市高三年级一模)氧 2020-05-16 …
CO2是否与NaOH发生了化学反应?实验一:软塑料瓶变瘪;实验二:瓶吞鸡蛋;有人认为这两个实验不足 2020-07-02 …
在化学反应过程中有变化的化学反应是氧化还原反应;其中,反应物所含元素化合价的反应称为氧化反应,是氧化 2020-12-02 …
下列实验所用实验药品和实验器材,与相应实验一致的是()实验实验药品实验器材(省略加持装置)A制备氧气 2020-12-19 …
在木炭还原氧化铜的实验中.下列有关说法错误的是()A.装置中使用铁丝网罩是为了集中火焰提高温度B.反 2020-12-21 …
到底高氯酸铵的受热分解方程式是什么我知道高氯酸铵的受热分解方程式有2NH4ClO4==高温==Cl2 2021-01-23 …