早教吧作业答案频道 -->化学-->
某研究性学习小组利用下列装置制备漂白粉,并进行漂白粉有效成分的质量分数测定(1)装置④中的x试剂为.(2)装置③中发生反应的化学方程式为.该反应是放热反应,反应温度较
题目详情
某研究性学习小组利用下列装置制备漂白粉,并进行漂白粉有效成分的质量分数测定
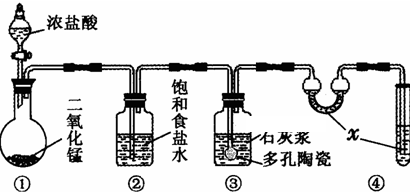
(1)装置④中的x试剂为___.
(2)装置③中发生反应的化学方程式为___.该反应是放热反应,反应温度较高时有副反应发生.改进该实验装置以减少副反应发生的方法是___
___.
(3)测定漂白粉有效成分的质量分数
称取1.000g漂白粉于锥形瓶中,加水溶解,调节溶液的pH,以淀粉为指示剂,用0.1000mol•L-1KI溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点.反应原理为:
3ClO-+I-═3Cl-+IO3- IO3-+5I-+3H2O═6OH-+3l2
实验测得数据如下表所示.
该漂白粉中有效成分的质量分数为___.若滴定过程中未充分振荡溶液局部变浅蓝色时就停止滴定,则测定结果将___(填“偏高”、“偏低”或“无影响”).

(1)装置④中的x试剂为___.
(2)装置③中发生反应的化学方程式为___.该反应是放热反应,反应温度较高时有副反应发生.改进该实验装置以减少副反应发生的方法是___
___.
(3)测定漂白粉有效成分的质量分数
称取1.000g漂白粉于锥形瓶中,加水溶解,调节溶液的pH,以淀粉为指示剂,用0.1000mol•L-1KI溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点.反应原理为:
3ClO-+I-═3Cl-+IO3- IO3-+5I-+3H2O═6OH-+3l2
实验测得数据如下表所示.
| 滴定次数 | 1 | 2 | 3 |
| KI溶液体积/mL | 19.98 | 20.02 | 20.00 |
▼优质解答
答案和解析
(1)氯气有毒,所以不能直接排空;氯气能和氢氧化钠溶液反应生成氯化钠和次氯酸钠、水,所以有毒物质转变为无毒物质,所以x试剂为氢氧化钠溶液.
故答案为:NaOH溶液.
(2)氯气和氢氧化钙反应生成氯化钙、次氯酸钙和水,反应方程式为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;该反应是放热反应,反应温度较高时有副反应发生.改进该实验装置以减少副反应发生的方法是降低温度.
故答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;将装置③置于冷水浴中进行实验.
(3)3ClO-+I-=3Cl-+IO3- ①; IO3-+5I-+3H2O=6OH-+3I2②
将方程式①+②得:ClO-+2I-+H2O=Cl-+2OH-+I2
KI溶液的总体积=(19.98+20.02+20.00)mL=60.00mL,平均体积为
=20.00mL.
设次氯酸根离子的物质的量为x.
ClO-+2I-+H2O=Cl-+2OH-+I2
1mol 2mol
x 0.1000mol•L-1×0.020L
所以x=0.001mol
次氯酸钙的质量为:143g×0.001mol×0.5=0.0715g
所以质量分数为:
=7.15%;
若滴定过程中未充分振荡溶液局部变浅蓝色时就停止滴定,导致碘化钾的物质的量偏少,所以测定结果将偏低.
故答案为:7.15%;偏低.
故答案为:NaOH溶液.
(2)氯气和氢氧化钙反应生成氯化钙、次氯酸钙和水,反应方程式为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;该反应是放热反应,反应温度较高时有副反应发生.改进该实验装置以减少副反应发生的方法是降低温度.
故答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;将装置③置于冷水浴中进行实验.
(3)3ClO-+I-=3Cl-+IO3- ①; IO3-+5I-+3H2O=6OH-+3I2②
将方程式①+②得:ClO-+2I-+H2O=Cl-+2OH-+I2
KI溶液的总体积=(19.98+20.02+20.00)mL=60.00mL,平均体积为
| 60.00mL |
| 3 |
设次氯酸根离子的物质的量为x.
ClO-+2I-+H2O=Cl-+2OH-+I2
1mol 2mol
x 0.1000mol•L-1×0.020L
所以x=0.001mol
次氯酸钙的质量为:143g×0.001mol×0.5=0.0715g
所以质量分数为:
| 0.0715 |
| 1.000 |
若滴定过程中未充分振荡溶液局部变浅蓝色时就停止滴定,导致碘化钾的物质的量偏少,所以测定结果将偏低.
故答案为:7.15%;偏低.
看了某研究性学习小组利用下列装置制...的网友还看了以下:
下列反应不属于还原反应的是甲醛转化为甲醇1.下列变化中有机物发生的反应不属于还原反应的是[]A.甲 2020-04-11 …
这道题怎么做:下列反应为吸热反应且下列反应为吸热反应且能自发进行的是[]A.4Fe(OH)2(s) 2020-04-11 …
以下关于ARM处理器的叙述中,错误的是()。A.ARM7~ARM11为经典ARM处理器B.Corte 2020-05-23 …
以石油裂解得到的乙烯和1,3-丁二烯为原料,经过下列反应合成高分子化合物H,该物质可用于制造以玻璃 2020-06-20 …
27,16,5,(),17.A.16B.1C.0D.2B解析27=33,16=42,5=51,1/ 2020-07-17 …
sumif函数格式问题求教在用sumif函数时出现如下问题:A列为时间(定义为Time),B列为数 2020-07-23 …
excel,如下所述,写公式?给出两列数据:A列B列为给出数据,A1对应着B1,A2对应着B2,根 2020-07-23 …
甲表有A、B二列,同列内为不重复数值;乙表有C、D二列,C列为不规则重复的数值,B列空白.求:如果 2020-07-23 …
当今在众多的招聘启事中,用工单位几乎都把“具有合作意识”列为应聘者必备的素质之一.这是因为()①合 2020-07-26 …
在密闭容器中进行下列反应:M(g)+N(g)═R(g)+2L.此反应符合下列图象,R%为R在平衡混合 2020-11-02 …