早教吧作业答案频道 -->化学-->
催化还原CO2是解决温室效应及能源问题的重要手段之一.研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个平衡反应,分别生成CH3OH和CO.反应的热化学方程式如下:CO2(g)+3H2(g)⇌CH3OH
题目详情
催化还原CO2是解决温室效应及能源问题的重要手段之一.研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个平衡反应,分别生成CH3OH和CO.反应的热化学方程式如下:
CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H1=-53.7kJ•mol-1 I
CO2(g)+H2(g)⇌CO(g)+H2O(g)△H2 II
某实验室控制CO2和H2初始投料比为1:2.2,经过相同反应时间测得如下实验数据:
【备注】Cat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片;甲醇选择性:转化的CO2中生成甲醛的百分比
已知:①CO和H2的标准燃烧热分别为-283.0kJ•mol-1和-285.8kJ•mol-1
②H2O(l)═H2O(g)△H3=44.0kJ•mol-1
请回答(不考虑温度对△H的影响):

(1)反应I的平衡常数表达式K=___;反应II的△H2=___kJ•mol-1.
(2)有利于提高CO2转化为CH3OH平衡转化率的措施有___.
A.使用催化剂Cat.1B.使用催化剂Cat.2C.降低反应温度
D.投料比不变,增加反应物的浓度 E.增大CO2和H2的初始投料比
(3)表中实验数据表明,在相同温度下不同的催化剂对CO2转化成CH3OH的选择性有显著的影响,其原因是___.
(4)在图中分别画出I在无催化剂、有Cat.1和由Cat.2三种情况下“反应过程-能量”示意图.
(5)研究证实,CO2也可在酸性水溶液中通过电解生成甲醇,则生成甲醇的反应发生在___极,该电极反应式是___.
CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H1=-53.7kJ•mol-1 I
CO2(g)+H2(g)⇌CO(g)+H2O(g)△H2 II
某实验室控制CO2和H2初始投料比为1:2.2,经过相同反应时间测得如下实验数据:
| T(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) |
| 543 | Cat.1 | 12.3 | 42.3 |
| 543 | Cat.2 | 10.9 | 72.7 |
| 553 | Cat.1 | 15.3 | 39.1 |
| 553 | Cat.2 | 12.0 | 71.6 |
已知:①CO和H2的标准燃烧热分别为-283.0kJ•mol-1和-285.8kJ•mol-1
②H2O(l)═H2O(g)△H3=44.0kJ•mol-1
请回答(不考虑温度对△H的影响):

(1)反应I的平衡常数表达式K=___;反应II的△H2=___kJ•mol-1.
(2)有利于提高CO2转化为CH3OH平衡转化率的措施有___.
A.使用催化剂Cat.1B.使用催化剂Cat.2C.降低反应温度
D.投料比不变,增加反应物的浓度 E.增大CO2和H2的初始投料比
(3)表中实验数据表明,在相同温度下不同的催化剂对CO2转化成CH3OH的选择性有显著的影响,其原因是___.
(4)在图中分别画出I在无催化剂、有Cat.1和由Cat.2三种情况下“反应过程-能量”示意图.
(5)研究证实,CO2也可在酸性水溶液中通过电解生成甲醇,则生成甲醇的反应发生在___极,该电极反应式是___.
▼优质解答
答案和解析
(1)平衡常数为生成物浓度幂之积与反应物浓度幂之积的比值,该反应的平衡常数为:K=
,
已知:CO和H2的标准燃烧热分别为-283.0kJ•mol-1和-285.8kJ•mol-1,②H2O(1)═H2O(g)△H3=44.0kJ•mol-1,可知热化学方程式a.CO(g)+
O2(g)=CO2(g)△H=-283.0kJ•mol-1,b.H2(g)+
O2(g)=H2O(1)△H=-285.8kJ•mol-1,c.H2O(1)═H2O(g)△H3=44.0kJ•mol-1,
由盖斯定律将b-a+c可得:CO2(g)+H2(g)⇌CO(g)+H2O(g)△H2 =(-285.8+283.0+44)kJ•mol-1=+41.2kJ•mol-1,
故答案为:
;+41.2;
(2)A.使用催化剂Cat.1,平衡不移动,不能提高转化率,故A错误;
B、使用催化剂Cat.2,不能提高转化率,故B错误;
C、降低反应温度,平衡正向移动,可增大转化率,故C正确;
D、投料比不变,增加反应物的浓度,衡正向移动,可增大转化率,故D正确;
E、增大 CO2和H2的初始投料比,可增大氢气的转化率,二氧化碳的转化率减小,故E错误.
故答案为:CD;
(3)从表中数据分析,在相同温度下,不同的催化剂二氧化碳的转化率不同,说明不同的催化剂的催化能力不同,相同的催化剂不同的温度,二氧化碳的转化率不同,且温度高的转化率大,因为正反应为放热反应,说明表中数据是未达到平衡数据,
故答案为:表中数据表明此时未达到平衡,不同的催化剂对反应Ⅰ的催化能力不同,因而在该时刻下对甲醇选择性有影响;
(4)从表中数据分析,在催化剂Cat.2的作用下,甲醇的选择性更大,说明催化剂Cat.2对反应Ⅰ催化效果更好,催化剂能降低反应的活化能,说明使用催化剂Cat.2的反应过程中活化能更低,故图为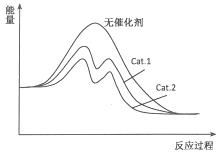 ,
,
故答案为: ;
;
(5)CO2也可在酸性水溶液中通过电解生成甲醇,C元素化合价降低,被还原,应为电解池的阴极反应,电极方程式为:CO2+6H++6e-=CH3OH+H2O,
故答案为:阴;CO2+6H++6e-=CH3OH+H2O.
| c(CH3OH)•c(H2O) |
| c(CO2)•c3(H2) |
已知:CO和H2的标准燃烧热分别为-283.0kJ•mol-1和-285.8kJ•mol-1,②H2O(1)═H2O(g)△H3=44.0kJ•mol-1,可知热化学方程式a.CO(g)+
| 1 |
| 2 |
| 1 |
| 2 |
由盖斯定律将b-a+c可得:CO2(g)+H2(g)⇌CO(g)+H2O(g)△H2 =(-285.8+283.0+44)kJ•mol-1=+41.2kJ•mol-1,
故答案为:
| c(CH3OH)•c(H2O) |
| c(CO2)•c3(H2) |
(2)A.使用催化剂Cat.1,平衡不移动,不能提高转化率,故A错误;
B、使用催化剂Cat.2,不能提高转化率,故B错误;
C、降低反应温度,平衡正向移动,可增大转化率,故C正确;
D、投料比不变,增加反应物的浓度,衡正向移动,可增大转化率,故D正确;
E、增大 CO2和H2的初始投料比,可增大氢气的转化率,二氧化碳的转化率减小,故E错误.
故答案为:CD;
(3)从表中数据分析,在相同温度下,不同的催化剂二氧化碳的转化率不同,说明不同的催化剂的催化能力不同,相同的催化剂不同的温度,二氧化碳的转化率不同,且温度高的转化率大,因为正反应为放热反应,说明表中数据是未达到平衡数据,
故答案为:表中数据表明此时未达到平衡,不同的催化剂对反应Ⅰ的催化能力不同,因而在该时刻下对甲醇选择性有影响;
(4)从表中数据分析,在催化剂Cat.2的作用下,甲醇的选择性更大,说明催化剂Cat.2对反应Ⅰ催化效果更好,催化剂能降低反应的活化能,说明使用催化剂Cat.2的反应过程中活化能更低,故图为
 ,
,故答案为:
 ;
;(5)CO2也可在酸性水溶液中通过电解生成甲醇,C元素化合价降低,被还原,应为电解池的阴极反应,电极方程式为:CO2+6H++6e-=CH3OH+H2O,
故答案为:阴;CO2+6H++6e-=CH3OH+H2O.
看了催化还原CO2是解决温室效应及...的网友还看了以下:
某研究性学习小组根据元素非金属性与其最高价氧化物对应的水化物之间的关系,设计了如图装置来一次性完成 2020-05-02 …
气雾剂中氟里昂(如F12)主要作用是()A.潜溶剂B.抛射剂C.防腐剂D.稳定剂E.消泡剂 2020-05-31 …
散剂按医疗用途可分为()A.倍散与普通散剂B.内服散剂与外用散剂C.单散剂与复散剂D.分剂量散剂和不 2020-05-31 …
属于含醇浸出剂型是()A.中药合剂B.酊剂C.煎膏剂D.颗粒剂E.糖浆剂 2020-05-31 …
阳离子表面活性剂常用作()A.杀菌剂B.乳化剂C.助溶剂D.助悬剂E.填充剂 2020-05-31 …
中药合剂和口服剂一般不必加入( )A、矫味剂B、防腐剂C、着色剂D、乙醇E、芳香剂 2020-06-07 …
研磨中起调制磨料、冷却和润滑作用是( )。A.磨料B.研磨液C.研磨剂 2020-06-07 …
研磨平面中出现表面不光洁时,是()。A.研磨剂太厚B.研磨时没调头C.研磨剂混入杂质D.磨料太厚 2020-06-07 …
17.可用于区分葡萄糖和果糖的试剂是A.托伦试剂B.斐林试剂C.莫立许17.可用于区分葡萄糖和果糖 2020-06-10 …
如果要研究牛奶中是否含有蛋白质、油脂和还原糖,需要分别准备的试剂是A.斐林试剂、斐林试剂、苏丹ⅢB 2020-06-10 …