早教吧作业答案频道 -->化学-->
联氨(又称联肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:(1)联氨分子的电子式为,其中氮的化合价为.(2)实验室可用次氯酸钠溶液与氨反
题目详情
联氨(又称联肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(1)联氨分子的电子式为___,其中氮的化合价为___.
(2)实验室可用次氯酸钠溶液与氨反应制备联氨,反应的离子方程式为____.
(3)①2O2(g)+N2(g)=N2O4(l)△H1
②N2(g)+2H2(g)=N2H4(l)△H2
③O2(g)+2H2(g)=2H2O(g)△H3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g)△H4
上述反应热效应之间的关系式为△H4=___(用△H1、△H2、△H3表示).
(4)联氨为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的平衡常数值为___
(已知:N2H4+H+⇌N2H5+ K=8.5×107;Kw=1.0×10-14).联氨与硫酸形成的酸式盐的化学式为___.
(1)联氨分子的电子式为___,其中氮的化合价为___.
(2)实验室可用次氯酸钠溶液与氨反应制备联氨,反应的离子方程式为____.
(3)①2O2(g)+N2(g)=N2O4(l)△H1
②N2(g)+2H2(g)=N2H4(l)△H2
③O2(g)+2H2(g)=2H2O(g)△H3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g)△H4
上述反应热效应之间的关系式为△H4=___(用△H1、△H2、△H3表示).
(4)联氨为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的平衡常数值为___
(已知:N2H4+H+⇌N2H5+ K=8.5×107;Kw=1.0×10-14).联氨与硫酸形成的酸式盐的化学式为___.
▼优质解答
答案和解析
(1)肼的分子式为N2H4,是氮原子和氢原子形成四个共价键,氮原子和氮原子之间形成一个共价键形成的共价化合物,电子式为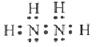 ;其中氢元素化合价为+1价,则氮元素化合价为-2价;
;其中氢元素化合价为+1价,则氮元素化合价为-2价;
故答案为额: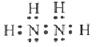 ;-2;
;-2;
(2)(2)氨气被次氯酸钠溶液氧化生成肼,次氯酸钠被还原生成氯化钠,结合原子守恒配平书写反应的化学方程式为:ClO-+2NH3=N2H4+Cl-+H2O;
故答案为:ClO-+2NH3=N2H4+Cl-+H2O;
(3)已知:①2O2(g)+N2(g)═N2O4(l)△H1
②N2(g)+2H2(g)═N2H4(l)△H2
③O2(g)+2H2(g)═2H2O(g)△H3
依据盖斯定律计算③×2-②×2-①得到④2N2H4(l)+N2O4(l)═3N2(g)+4H2O(g)△H4=2△H3-2△H2-△H1;
故答案为:△H4=2△H3-2△H2-△H1;
(4)联氨为二元弱碱,在水中的电离方式与氨相似.联氨第一步电离方程式为N2H4+H2O⇌N2H5++OH-,平衡常数Kb=
=
×
=K×Kw=8.7×107×1.0×10-14=8.7×10-7,第二步电离方程式为N2H5++H2O⇌N2H62++OH-,因此联氨与硫酸形成的酸式盐为N2H6(HSO4)2;
故答案为:8.5×10-7;N2H6(HSO4)2.
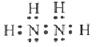 ;其中氢元素化合价为+1价,则氮元素化合价为-2价;
;其中氢元素化合价为+1价,则氮元素化合价为-2价;故答案为额:
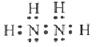 ;-2;
;-2;(2)(2)氨气被次氯酸钠溶液氧化生成肼,次氯酸钠被还原生成氯化钠,结合原子守恒配平书写反应的化学方程式为:ClO-+2NH3=N2H4+Cl-+H2O;
故答案为:ClO-+2NH3=N2H4+Cl-+H2O;
(3)已知:①2O2(g)+N2(g)═N2O4(l)△H1
②N2(g)+2H2(g)═N2H4(l)△H2
③O2(g)+2H2(g)═2H2O(g)△H3
依据盖斯定律计算③×2-②×2-①得到④2N2H4(l)+N2O4(l)═3N2(g)+4H2O(g)△H4=2△H3-2△H2-△H1;
故答案为:△H4=2△H3-2△H2-△H1;
(4)联氨为二元弱碱,在水中的电离方式与氨相似.联氨第一步电离方程式为N2H4+H2O⇌N2H5++OH-,平衡常数Kb=
| c(N2H5+)•c(OH-) |
| c(N2H4) |
| c(N2H5+)•c(OH-) |
| c(N2H4) |
| c(H+) |
| c(H+) |
故答案为:8.5×10-7;N2H6(HSO4)2.
看了联氨(又称联肼,N2H4,无色...的网友还看了以下:
氨气是一种富氢燃料,可以直接用于燃料电池,如图是供氨水式燃料电池工作原理:(1)氨气燃料电池的电解 2020-04-07 …
科学研究表明,氨气在常压下就可液化为液氨,液氨可用作汽车的清洁燃料,其燃烧时的主要反应为。下列说法 2020-05-15 …
(1)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视.它在安全性、价格等方面较化石燃料和氢燃 2020-06-27 …
氨作为一种富氢化合物,具有各种优点,特别是氨有着良好的产业基础,价格低廉,氨作为燃料电池燃料具有很 2020-07-03 …
请问有没有工业氨气尾气处理的方法?99.9999%氨气排放量为1500kg/月,根据氨气燃烧可以生 2020-07-22 …
下列叙述正确的是()A.用湿润的蓝色石蕊试纸检验氨气B.当浓氨水与浓硫酸反应会产生白烟C.只用BaC 2020-11-02 …
在一定条件下,氨气容易液化而成为液氨,液氨可以燃烧,其燃烧的化学方程式为:4NH3+3O2点燃.2X 2020-11-03 …
用水鉴别氯化钾和碳酸氨是否可行?为什么?燃烧法鉴别真假毛线是否可行为什么?化学分类.用水鉴别氯化钾和 2020-12-05 …
科学研究表明,氨气在常压下就可以液化为液氨。液氨具有可燃性,可用作汽车的清洁燃料。氨气在一定条件下可 2021-02-16 …
科学研究表明,氨气在常压下就可以液化为液氨.液氨具有可燃性,可用作汽车的清洁燃料.氨气在一定条件下可 2021-02-16 …