早教吧作业答案频道 -->化学-->
Cl2、漂白液(有效成分为NaClO)在生产、生活中广泛用于杀菌、消毒.(1)电解NaCl溶液生成Cl2的化学方程式是(2)①Cl2溶于H2O、NaOH溶液即获得氯水、漂白液.干燥的氯气不能漂白物质,
题目详情
Cl2、漂白液(有效成分为NaClO)在生产、生活中广泛用于杀菌、消毒.
(1)电解NaCl溶液生成Cl2的化学方程式是___
(2)①Cl2溶于H2O、NaOH溶液即获得氯水、漂白液.
干燥的氯气不能漂白物质,但氯水却有漂白作用,说明起漂白作用的物质是___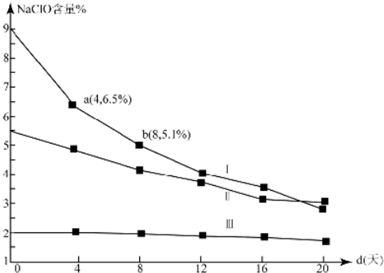
②25℃,Cl2与H2O、NaOH的反应如下:
不直接使用氯水而使用漂白液做消毒剂的原因是___
(3)家庭使用漂白液时,不宜直接接触铁制品,漂白液腐蚀铁的电极反应为:Fe-2e-=Fe2+:ClO-发生的电极反应式是___
(4)研究漂白液的稳定性对其生产和保存有实际意义.30℃时,pH=11的漂白液中NaClO的质量百分含量随时间变化如下:
①分解速v(Ⅰ)、v(Ⅱ)的大小关系是___,原因是___
②NaClO分解的化学方程式是___
③4d~8d,Ⅰ中v(NaClO)=___mol/(L.d)(常温下漂白液的密度约为1g/cm3,且变化忽略不计)
(1)电解NaCl溶液生成Cl2的化学方程式是___
(2)①Cl2溶于H2O、NaOH溶液即获得氯水、漂白液.
干燥的氯气不能漂白物质,但氯水却有漂白作用,说明起漂白作用的物质是___

②25℃,Cl2与H2O、NaOH的反应如下:
| 反应Ⅰ | Cl2+H2O⇌Cl-+H++HClO K1=4.5×10-4 |
| 反应Ⅱ | Cl2+2OH-⇌Cl-+ClO-+H2O K2=7.5×1015 |
(3)家庭使用漂白液时,不宜直接接触铁制品,漂白液腐蚀铁的电极反应为:Fe-2e-=Fe2+:ClO-发生的电极反应式是___
(4)研究漂白液的稳定性对其生产和保存有实际意义.30℃时,pH=11的漂白液中NaClO的质量百分含量随时间变化如下:
①分解速v(Ⅰ)、v(Ⅱ)的大小关系是___,原因是___
②NaClO分解的化学方程式是___
③4d~8d,Ⅰ中v(NaClO)=___mol/(L.d)(常温下漂白液的密度约为1g/cm3,且变化忽略不计)
▼优质解答
答案和解析
(1)电解NaCl溶液可生成氢气、氯气和氢氧化钠,方程式为2NaCl+2H2O
2NaOH+H2↑+Cl2↑,故答案为:2NaCl+2H2O
2NaOH+H2↑+Cl2↑;
(2)①氯水中含有盐酸和次氯酸,氯气和盐酸都不具有漂白性,具有漂白性的为HClO,故答案为:HClO;
②氯水和漂白液的漂白成分为HClO,根据平衡常数K2>K1,确定漂白液的有效成分次氯酸更多,并且次氯酸钠比次氯酸更稳定,
故答案为:K2>K1,反应Ⅱ的有效成分比反应Ⅰ的有效成分大,氯气转化为HClO更充分,次氯酸钠比次氯酸更稳定;
(3)Fe-2e-=Fe2+应为负极反应,则正极反应为ClO-得电子被还原,方程式为ClO-+2e-+H2O=Cl-+2OH-,故答案为:ClO-+2e-+H2O=Cl-+2OH-;
(4)①根据图可知次氯酸钠的其实含量Ⅰ大于Ⅱ,浓度越大反应速率越大,则v(Ⅰ)>v(Ⅱ),
故答案为:>;在相同条件下,次氯酸钠的浓度越大,其分解速率越大;
②NaClO分解的最终产物为NaCl和氧气,方程式为2NaClO
2NaCl+O2↑,故答案为:2NaClO
2NaCl+O2↑;
③4d~8d,NaClO的含量由6.5%变为5.1%,假设溶液体积为1L,v(NaClO)=[(6.5%-5.1%)×1g/mL×103÷74.5g/mol]÷4d=0.047mol/(L.d),故答案为:0.047.
| ||
| ||
(2)①氯水中含有盐酸和次氯酸,氯气和盐酸都不具有漂白性,具有漂白性的为HClO,故答案为:HClO;
②氯水和漂白液的漂白成分为HClO,根据平衡常数K2>K1,确定漂白液的有效成分次氯酸更多,并且次氯酸钠比次氯酸更稳定,
故答案为:K2>K1,反应Ⅱ的有效成分比反应Ⅰ的有效成分大,氯气转化为HClO更充分,次氯酸钠比次氯酸更稳定;
(3)Fe-2e-=Fe2+应为负极反应,则正极反应为ClO-得电子被还原,方程式为ClO-+2e-+H2O=Cl-+2OH-,故答案为:ClO-+2e-+H2O=Cl-+2OH-;
(4)①根据图可知次氯酸钠的其实含量Ⅰ大于Ⅱ,浓度越大反应速率越大,则v(Ⅰ)>v(Ⅱ),
故答案为:>;在相同条件下,次氯酸钠的浓度越大,其分解速率越大;
②NaClO分解的最终产物为NaCl和氧气,方程式为2NaClO
| ||
| ||
③4d~8d,NaClO的含量由6.5%变为5.1%,假设溶液体积为1L,v(NaClO)=[(6.5%-5.1%)×1g/mL×103÷74.5g/mol]÷4d=0.047mol/(L.d),故答案为:0.047.
看了Cl2、漂白液(有效成分为Na...的网友还看了以下:
初一数学37精确到10,有几个有效数字?37精确到10是40,但是习题上的答案是:有2个有效数字.疑 2020-03-30 …
0.0238(精确到0.001)的近似数是多少?2.605(保留2个有效数字)的近似数是多少?2. 2020-05-13 …
9.请你从修辞的角度,来说说下面两个句子的表达效果。⑴你读书的样子好像打仗似的,好快好快地翻,读完 2020-05-13 …
无水硫酸钠干燥甲苯后,抽滤的无水硫酸钠再用含有少量水的甲苯淋洗,后合并!是不是起不到脱水干燥的效果 2020-07-07 …
34567精确到千位.6034001精确到百万位.10亿是精确到了哪一位?203500精确到千位. 2020-07-08 …
近似数2.0万的有效数字个数及精确度分别是()A.有1个有效数字,精确到个位B.有2个有效数字,精 2020-07-29 …
由四舍五入法得到的近似数6.8×103,下列说法中正确的是()A.精确到十分位,有2个有效数字B. 2020-08-02 …
低段语文教学中,生字词的教学比较重要,这一关也是同学们难掌握,也比较枯燥,有效有趣的识记方法? 2021-01-23 …
如何保留有效数字呢?大题最后一问:保留三位有效数字,我印象中是保留三位小数,这个对不?在对照课本上的 2021-02-02 …
大肠干燥速效解决方案 2021-04-02 …