早教吧作业答案频道 -->化学-->
自从1985年发现了富勒烯以来,由于其具有独特的物理和化学性质,越来越受到人们的关注.(1)富勒烯(C60)在液相中用FeCl3催化可生成二聚体,过程见图.①Fe3+基态时M能层电子排布式为
题目详情
自从1985年发现了富勒烯以来,由于其具有独特的物理和化学性质,越来越受到人们的关注.
(1)富勒烯(C60)在液相中用FeCl3催化可生成二聚体,过程见图.
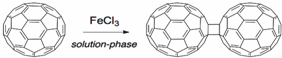
①Fe3+基态时M能层电子排布式为___.
②富勒烯二聚体中碳原子杂化轨道类型有___.
(2)下列有关说法正确的是___.
A.C3H8中碳原子都采用的是sp3杂化
B.O2、CO2、NH3都是非极性分子
C.每个N2中,含有2个π键
(3)CO的一种等电子体为NO+,NO+的电子式为___
(4)ClO2-的立体构型是___,该离子中两种元素的电负性由小到大的顺序为___.
(5)Zr原子序数为40,价电子排布式为4d25s2,它在周期表中的位置是___.
(6)关于化合物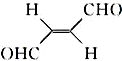 ,下列叙述正确的有___.
,下列叙述正确的有___.
A.该分子在水中的溶解度大于2-丁烯
B.分子中只有极性键
C.分子中有7个σ键和1个π键
D.该化合物既能发生还原反应又能发生氧化反应
E.分子间可形成氢键.
(1)富勒烯(C60)在液相中用FeCl3催化可生成二聚体,过程见图.

①Fe3+基态时M能层电子排布式为___.
②富勒烯二聚体中碳原子杂化轨道类型有___.
(2)下列有关说法正确的是___.
A.C3H8中碳原子都采用的是sp3杂化
B.O2、CO2、NH3都是非极性分子
C.每个N2中,含有2个π键
(3)CO的一种等电子体为NO+,NO+的电子式为___
(4)ClO2-的立体构型是___,该离子中两种元素的电负性由小到大的顺序为___.
(5)Zr原子序数为40,价电子排布式为4d25s2,它在周期表中的位置是___.
(6)关于化合物
 ,下列叙述正确的有___.
,下列叙述正确的有___.A.该分子在水中的溶解度大于2-丁烯
B.分子中只有极性键
C.分子中有7个σ键和1个π键
D.该化合物既能发生还原反应又能发生氧化反应
E.分子间可形成氢键.
▼优质解答
答案和解析
(1)①铁是26号元素,铁原子核外有26个电子,铁原子失去3个电子变成铁离子,根据构造原理可知铁离子核外电子排布式为1s22s22p63s23p63d5 或[Ar]3d5;
故答案为:3s23p63d5;
②从富勒烯二聚体中可以看出大多数碳原子每个C原子和其它三个C原子成键,为三个δ键和一个π键,故杂化类型为sp2杂化,有4个碳原子每个C原子和其它四个C原子成键,为四个δ键,故杂化类型为sp3杂化;
故答案为:sp2、sp3;
(2)A.C3H8分子中每个C原子含有4个σ键,所以每个C原子价层电子对个数是4,则C原子采用sp3杂化,故A正确;
B.O2是以非极性键结合的双原子一定为非极性分子,CO2中含有极性键,为直线形分子,结构对称,分子中正负电荷重心重叠,为非极性分子,NH3的立体构型为三角锥型,结构不对称,分子中正负电荷重心不重叠,为极性分子,故B错误;
C.1个氮氮三键中含有2个π键,故C正确;
故答案为:AC;
(3)CO的一种等电子体为NO+,CO的结构为C≡O,则NO+的电子式为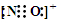 ,
,
故答案为: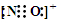 ;
;
(4)ClO2-中价层电子对个数=2+
(7+1-2×2)=2,且含有2个孤电子对,所以是V型;元素的非金属性越强,其电负性越强,则电负性:Cl<O;
故答案为:Cl<O;
(5)Zr原子序数为40,价电子排布式为4d25s2,含有5个电子层,在第五周期,价电子数为4,为第IVB族;
故答案为:第5周期第ⅣB族;
(6)A.2-丁烯不溶于水,而该物质属于烯醛类物质,可溶于水,则该分子在水中的溶解度大于2-丁烯,故A正确;
B.C、H与C、O之间形成极性键,而C、C之间形成非极性键,则分子中既有极性键又有非极性键,故B错误;
C.双键中含1个σ键和1个π键,单键均为σ键,则分子中有9个σ键和3个π键,故C错误;
D.-CHO能被氧化成羧基、被还原成羟基,碳碳双键,既能被酸性高锰酸钾等氧化剂氧化,又能加氢被还原,故D正确;
E.含-CHO,没有O-H键,则不能形成氢键,故E错误;
故答案为:AD.
故答案为:3s23p63d5;
②从富勒烯二聚体中可以看出大多数碳原子每个C原子和其它三个C原子成键,为三个δ键和一个π键,故杂化类型为sp2杂化,有4个碳原子每个C原子和其它四个C原子成键,为四个δ键,故杂化类型为sp3杂化;
故答案为:sp2、sp3;
(2)A.C3H8分子中每个C原子含有4个σ键,所以每个C原子价层电子对个数是4,则C原子采用sp3杂化,故A正确;
B.O2是以非极性键结合的双原子一定为非极性分子,CO2中含有极性键,为直线形分子,结构对称,分子中正负电荷重心重叠,为非极性分子,NH3的立体构型为三角锥型,结构不对称,分子中正负电荷重心不重叠,为极性分子,故B错误;
C.1个氮氮三键中含有2个π键,故C正确;
故答案为:AC;
(3)CO的一种等电子体为NO+,CO的结构为C≡O,则NO+的电子式为
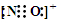 ,
,故答案为:
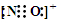 ;
;(4)ClO2-中价层电子对个数=2+
| 1 |
| 2 |
故答案为:Cl<O;
(5)Zr原子序数为40,价电子排布式为4d25s2,含有5个电子层,在第五周期,价电子数为4,为第IVB族;
故答案为:第5周期第ⅣB族;
(6)A.2-丁烯不溶于水,而该物质属于烯醛类物质,可溶于水,则该分子在水中的溶解度大于2-丁烯,故A正确;
B.C、H与C、O之间形成极性键,而C、C之间形成非极性键,则分子中既有极性键又有非极性键,故B错误;
C.双键中含1个σ键和1个π键,单键均为σ键,则分子中有9个σ键和3个π键,故C错误;
D.-CHO能被氧化成羧基、被还原成羟基,碳碳双键,既能被酸性高锰酸钾等氧化剂氧化,又能加氢被还原,故D正确;
E.含-CHO,没有O-H键,则不能形成氢键,故E错误;
故答案为:AD.
看了自从1985年发现了富勒烯以来...的网友还看了以下:
关于如何判断反应类型加成反应取代反应消去反应氧化反应加聚反应缩聚反应水解反应酯化反应等等这些反应如 2020-05-17 …
聚氯乙烯绝缘和聚氯乙烯护套是什么意思聚氯乙烯绝缘是护套里的导线的绝缘层吗,聚氯乙烯护套是护套的材料 2020-05-17 …
下列说法中正确的是:A.不粘锅的涂层是聚四氟乙烯,聚四氟乙烯可以发生加成反应B.只有与卤原子相连的 2020-06-18 …
读地球圈层结构示意图,回答18-19题.有关图中地球圈层特点的叙述,正确的是()A.水圈都分布在海 2020-06-26 …
不粘锅内壁涂有一薄层聚四氟乙烯涂层,聚四氟乙烯商品名为“特氟隆”(如图).下列关于聚四氟乙烯的说法 2020-06-26 …
火箭在飞行时,外壳与空气发生摩擦而产生高温,为防止火箭舱内温度过高,在外层涂有一层特殊材料,这层特 2020-07-04 …
如图所示,有一塑石英正方体,内有一空气层,当一束平行光垂直通过石英正方体时,光在空气层中发生的现象 2020-07-07 …
某学校有体育特长生人,美术特长生人,音乐特长生人.用分层抽样的方法从中抽取人,则抽取的体育特长生、美 2020-11-21 …
读某地地层剖面示意图,完成7-8题.对该地地层特征的描述正确的是()A.P地层的岩石为变质岩B.N地 2020-12-02 …
对该地地层特征的描述正确的是()A、P地层的岩石为变质岩B、N地层中含有大量油气资源C、M地层中可能 2020-12-02 …