早教吧作业答案频道 -->化学-->
实施以节约能源和减少废气排放为基本内容的节能减排政策,是应对全球气候问题、建设资源节约型、环境友好型社会的必然选择.化工行业的发展必须符合国家节能减排的总体要求.试运
题目详情
实施以节约能源和减少废气排放为基本内容的节能减排政策,是应对全球气候问题、建设资源节约型、环境友好型社会的必然选择.化工行业的发展必须符合国家节能减排的总体要求.试运用所学知识,回答下列问题:
(1)已知某温度下某反应的化学平衡常数表达式为:K=
,所对应的化学反应方程式为:___.
(2)已知在一定温度下,
①C(s)+CO2(g)⇌2CO(g)△H1=a kJ/mol 平衡常数K1;
②CO(g)+H2O(g)⇌H2(g)+CO2(g)△H2=b kJ/mol 平衡常数K2;
③C(s)+H2O(g)⇌CO(g)+H2(g)△H3 平衡常数K3.
则K1、K2、K3之间的关系是:___,△H3=___(用含a、b的代数式表示).
(3)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题.已知等体积的一氧化碳和水蒸气进入反应器时,发生如下反应:CO(g)+H2O(g)⇌H2(g)+CO2(g),该反应平衡常数随温度的变化如表所示:
该反应的正反应方向是___反应(填“吸热”或“放热”),若在500℃时进行,设起始时CO和H2O的起始浓度均为0.020mol•L-1,在该条件下,CO的平衡转化率为:___.
(4)在催化剂存在条件下反应:H2O(g)+CO(g)⇌CO2(g)+H2(g),CO转化率随蒸气添加量的压强比及温度变化关系如图1所示:
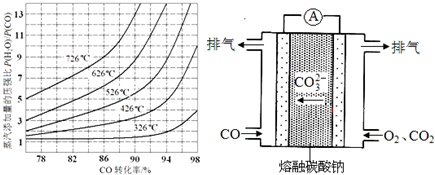
对于气相反应,用某组分(B)的平衡分压强(PB)代替物质的量浓度(cB)也可以表示平衡常数(记作Kp),则该反应的Kp=___,提高p[H2O(g)]/p(CO)比,则Kp___(填“变大”、“变小”或“不变”).实际上,在使用铁镁催化剂的工业流程中,一般采用400℃左右、p[H2O(g)]/p(CO)=3~5.其原因可能是___.
(5)工业上可利用原电池原理除去工业尾气中的CO并利用其电能,反应装置如图2所示,请写出负极的电极反应式:___.
(1)已知某温度下某反应的化学平衡常数表达式为:K=
| c(H2O) |
| c(CO)•c(H2) |
(2)已知在一定温度下,
①C(s)+CO2(g)⇌2CO(g)△H1=a kJ/mol 平衡常数K1;
②CO(g)+H2O(g)⇌H2(g)+CO2(g)△H2=b kJ/mol 平衡常数K2;
③C(s)+H2O(g)⇌CO(g)+H2(g)△H3 平衡常数K3.
则K1、K2、K3之间的关系是:___,△H3=___(用含a、b的代数式表示).
(3)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题.已知等体积的一氧化碳和水蒸气进入反应器时,发生如下反应:CO(g)+H2O(g)⇌H2(g)+CO2(g),该反应平衡常数随温度的变化如表所示:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
(4)在催化剂存在条件下反应:H2O(g)+CO(g)⇌CO2(g)+H2(g),CO转化率随蒸气添加量的压强比及温度变化关系如图1所示:

对于气相反应,用某组分(B)的平衡分压强(PB)代替物质的量浓度(cB)也可以表示平衡常数(记作Kp),则该反应的Kp=___,提高p[H2O(g)]/p(CO)比,则Kp___(填“变大”、“变小”或“不变”).实际上,在使用铁镁催化剂的工业流程中,一般采用400℃左右、p[H2O(g)]/p(CO)=3~5.其原因可能是___.
(5)工业上可利用原电池原理除去工业尾气中的CO并利用其电能,反应装置如图2所示,请写出负极的电极反应式:___.
▼优质解答
答案和解析
(1)平衡常数为生成物的浓度幂之积除以反应物的浓度幂之积,平衡常数中,分子为生成物,分母为反应物,再结合元素守恒,生成物中应有碳元素,在平衡常数表达式中没有,则说明是碳固体单质,所以该反应的方程式为CO(g)+H2(g)⇌C(s)+H2O(g),
故答案为:CO(g)+H2(g)⇌C(s)+H2O(g);
(2)根据化学方程式可知:K1=
,K2=
,K3=
,所以:K3=K1×K2;由①+②可得方程式C(s)+H2O(g)⇌CO(g)+H2(g),所以△H3=(a+b)kJ/mol,
故答案为:K3=K1×K2;(a+b)kJ/mol;
(3)由图可知温度越高K值越小,说明正反应为放热反应,
对于反应 CO(g)+H2O(g)⇌H2(g)+CO2(g),
开始(mol/L):0.02 0.02 0 0
变化(mol/L):c c c c
平衡(mol/L):0.02-c 0.02-c c c
所以
=9,解得c=0.015
所以CO的转化率为
×100%=75%,
故答案为:放热;75%;
(4)对于气相反应,用某组分(B)的平衡压强(pB)代替物质的量浓度也可以表示平衡常数(记作Kp),反应的平衡常数=
;平衡常数只与温度有关,与浓度无关,所以提高
比,则KP不变;由图象可知,投料比太低,CO的转化率不太高,而投料比3~5:1时转化率已经很高达到96%~98%,再增加投料比,需要大大的增加蒸汽添加量,这样在在经济上不合算,催化剂的活性温度在400℃左右,所以一般采用400℃左右,H2O(气):CO=3~5;
故答案为:
;不变;投料比太低,CO的转化率不太高,而投料比3~5时转化率已经很高达到96%~98%,再增加投料比,需要大大的增加蒸汽添加量,这样在在经济上不合算,催化剂的活性温度在400℃左右;
(5)负极发生氧化反应,CO-2e-+CO32-=2CO2,
故答案为:CO-2e-+CO32-=2CO2.
故答案为:CO(g)+H2(g)⇌C(s)+H2O(g);
(2)根据化学方程式可知:K1=
| c 2(CO) |
| c(CO 2) |
| c(H 2)×c(CO 2) |
| c(CO)×c(H 2O) |
| c(CO)×c(H 2) |
| c(H 2O) |
故答案为:K3=K1×K2;(a+b)kJ/mol;
(3)由图可知温度越高K值越小,说明正反应为放热反应,
对于反应 CO(g)+H2O(g)⇌H2(g)+CO2(g),
开始(mol/L):0.02 0.02 0 0
变化(mol/L):c c c c
平衡(mol/L):0.02-c 0.02-c c c
所以
| c×c |
| (0.02-c)×(0.02-c) |
所以CO的转化率为
| 0.015mol/L |
| 0.02mol/L |
故答案为:放热;75%;
(4)对于气相反应,用某组分(B)的平衡压强(pB)代替物质的量浓度也可以表示平衡常数(记作Kp),反应的平衡常数=
| P(CO 2)P(H 2) |
| P(CO)P(H 2O) |
| H 2O(g) |
| CO |
故答案为:
| P(CO 2)P(H 2) |
| P(CO)P(H 2O) |
(5)负极发生氧化反应,CO-2e-+CO32-=2CO2,
故答案为:CO-2e-+CO32-=2CO2.
看了实施以节约能源和减少废气排放为...的网友还看了以下:
某同学在探究废干电池内的黑色固体回收利用时,进行如图所示实验:查阅教材可知,普通锌锰电池的黑色物质 2020-05-13 …
某同学在探究废干电池内的黑色固体回收利用时,进行如图所示实验:查阅教材可知,普通锌锰电池的黑色物质 2020-05-13 …
某工厂的废金属屑中主要成分为Cu、Fe和Al,此外还含有少量Al2O3和Fe2O3,该厂用上述废金 2020-05-13 …
某工厂的废金属屑中主要成分为Cu、Fe和Al,此外还含有少量Al2O3和Fe2O3,为探索工业废料 2020-05-13 …
关于生物体内水和无机盐的叙述,不正确的是()A.体内参与运输营养物质和代谢废物的水是自由水B.无机 2020-05-14 …
某工厂的废金属屑中主要成分为Cu、Fe和Al,此外还含有少量Al2O3和Fe2O3,为探索工业废料 2020-05-17 …
碱式碳酸铜[Cu2(OH)2CO3]是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的 2020-05-17 …
化学与生产、生活、社会密切相关.下列说法中不正确的是()A.合金材料中可能含有非金属元素B.用CO 2020-05-17 …
【求助】如何利用有机废水的COD(化学需氧量)计算出其浓度?急需“有机废水的COD(化学需氧量)与 2020-05-17 …
“远芳侵古道,晴翠接荒城”是白居易《赋得古原草送别》诗中的一句,错误的说法是()A.废弃的古道和城 2020-06-12 …