早教吧作业答案频道 -->化学-->
小亮同学在实验室中制取CO2气体后,对废液进行后续探究,他向101.2g的含CaCl2和HCl的废液中逐滴加入溶质质量分数为10%的Na2CO3溶液.实验过程中加入Na2CO3溶液的质量与溶液的pH变化关系如图1
题目详情
小亮同学在实验室中制取CO2气体后,对废液进行后续探究,他向101.2g的含CaCl2和HCl的废液中逐滴加入溶质质量分数为10%的Na2CO3溶液.实验过程中加入Na2CO3溶液的质量与溶液的pH变化关系如图1所示,加入Na2CO3溶液质量与产生沉淀或气体的质量关系如图2所示.
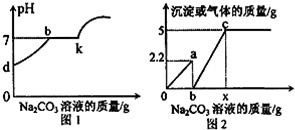
(1)图1中db段化学方程式为___;K点表示的意义是___;
(2)图2中,b=___,x=___;a时溶液中的溶质是___,c点时溶液中的溶质是___.
(3)计算图2中c点时溶液中的溶质质量分数(写出解题步骤).

(1)图1中db段化学方程式为___;K点表示的意义是___;
(2)图2中,b=___,x=___;a时溶液中的溶质是___,c点时溶液中的溶质是___.
(3)计算图2中c点时溶液中的溶质质量分数(写出解题步骤).
▼优质解答
答案和解析
(1)db段的反应是碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑,K点表示的意义是:碳酸钠与氯化钙、稀盐酸完全反应;
(2)设b点时消耗碳酸钠的质量为x,生成氯化钠的质量为y,
Na2CO3+2HCl═2NaCl+H2O+CO2↑,
106 117 44
x y 2.2g
=
=
x=5.3g
y=5.85g
图1中b点消耗碳酸钠溶液的质量为:
=53g,
设与氯化钙反应的碳酸钠的质量为m,生成氯化钠的质量为n
Na2CO3+CaCl2═CaCO3↓+2NaCl,
106 100 117
m 5.0g n
=
=
m=5.3g
n=5.85g
所以参加反应的碳酸钠溶液质量为:
=53g,所以x=106g;
a时溶液中的溶质是氯化钠、氯化钙,c点时溶液中的溶质是氯化钠;
(3)滤液质量为:101.2g+53g+53g-2.2g-5.0g=200g,
滤液中的溶质质量分数为:
×100%=5.85%.
故答案为:(1)Na2CO3+2HCl═2NaCl+H2O+CO2↑,碳酸钠与氯化钙、稀盐酸完全反应;
(2)53g,106g;氯化钠、氯化钙,氯化钠;
(3)5.85%.
(2)设b点时消耗碳酸钠的质量为x,生成氯化钠的质量为y,
Na2CO3+2HCl═2NaCl+H2O+CO2↑,
106 117 44
x y 2.2g
| 106 |
| x |
| 117 |
| y |
| 44 |
| 2.2g |
x=5.3g
y=5.85g
图1中b点消耗碳酸钠溶液的质量为:
| 5.3g |
| 10% |
设与氯化钙反应的碳酸钠的质量为m,生成氯化钠的质量为n
Na2CO3+CaCl2═CaCO3↓+2NaCl,
106 100 117
m 5.0g n
| 106 |
| m |
| 100 |
| 5g |
| 117 |
| n |
m=5.3g
n=5.85g
所以参加反应的碳酸钠溶液质量为:
| 5.3g |
| 10% |
a时溶液中的溶质是氯化钠、氯化钙,c点时溶液中的溶质是氯化钠;
(3)滤液质量为:101.2g+53g+53g-2.2g-5.0g=200g,
滤液中的溶质质量分数为:
| 5.85g×2 |
| 200g |
故答案为:(1)Na2CO3+2HCl═2NaCl+H2O+CO2↑,碳酸钠与氯化钙、稀盐酸完全反应;
(2)53g,106g;氯化钠、氯化钙,氯化钠;
(3)5.85%.
看了 小亮同学在实验室中制取CO2...的网友还看了以下:
与集合有关的几个问题1.A是B的子集与A是B的真子集有什么区别?遇到A{1,2,3}和B{1,2,3 2020-03-31 …
1——————电源————.11+-1如果开关断开,A处有电流吗?B处呢?AB1开关1------ 2020-05-15 …
集合{1,2},{(1,2)}有什么区别和关系?主要想知道有什么关系?老师让我们预习原题如下:集合 2020-06-08 …
1.设集合x={0,1,2,3}中的两个关系,R={|i,j∈x∧(j=i+1∨j=i/2)},S 2020-06-12 …
如图:1图和2图示皮肤中血管的舒张、收缩与散热的关系,3图和4图示汗液蒸发与散热的关系,据图回答: 2020-06-13 …
如图是关节的模式图,请回答:(1)关节的基本结构包括:,和三部分.(2)这样的关节即灵活又牢固.其 2020-06-20 …
如图为关节示意图,据图回答问题:(1)关节是由关节头、关节窝、以及关节囊.(2关节的牢固性与图中的 2020-06-21 …
如果关于x的不等式(a-1)x<a+5和2x<4的解集相同,则a的值为.(1)一变:如果(a−1) 2020-07-07 …
如图所示,电源电压不变,当开关S1断开,S2接通时,电压表示数为4.5V,当开关S1接通,S2断开 2020-07-08 …
麻烦给我讲讲呵呵.1、若关于X的一元二次方程ax^2+2x-5=0的两跟中有且仅有一根在0和1之间 2020-07-22 …