早教吧作业答案频道 -->化学-->
某化学兴趣小组制取氯酸钾和氯水并进行有关探究实验.实验一制取氯酸钾和氯水利用如图1所示的实验装置进行实验.(1)制取实验结束后,取出B中试管冷却结晶、过滤、洗涤.该实验操
题目详情
某化学兴趣小组制取氯酸钾和氯水并进行有关探究实验.实验一制取氯酸钾和氯水利用如图1所示的实验装置进行实验.
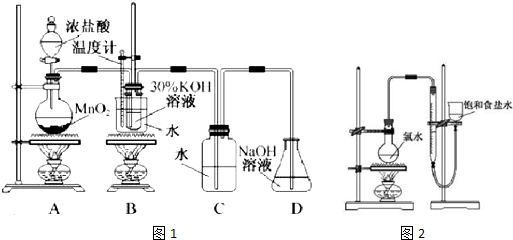
(1)制取实验结束后,取出B中试管冷却结晶、过滤、洗涤.该实验操作过程需要的玻璃仪器有胶头滴管、烧杯外,还需要的玻璃仪器是___.
(2)若对调B和C装置的位置,___(填“能”或“不能”)提高B中氯酸钾的产率.
实验二 氯酸钾与碘化钾反应的探究
(3)在不同条件下KClO3可将KI氧化为I2或KIO3.该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录表如下(实验在室温下进行):
①系列a实验的实验目的是___.
②设计1号试管实验的作用是___.
③若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色;假设氧化产物唯一,还原产物为KCl,则此反应的离子方程式为___.
实验三 测定饱和氯水中氯元素的总量
(4)该小组设计的实验方案为:使用图2装置,加热15.0ml饱和氯水试样,测定产生气体的体积.此方案是否可行___(填“是”或“否”)
(5)另一小组研究出的方案是,量取一定量的试样,加入足的H2O2溶液,加热除去过量的H2O2,冷却,再加入足量的硝酸银溶液,还需进行的操作是___
已知:次氯酸或氯水可被SO2、H2O2、FeCl2等物质还原成Cl-.

(1)制取实验结束后,取出B中试管冷却结晶、过滤、洗涤.该实验操作过程需要的玻璃仪器有胶头滴管、烧杯外,还需要的玻璃仪器是___.
(2)若对调B和C装置的位置,___(填“能”或“不能”)提高B中氯酸钾的产率.
实验二 氯酸钾与碘化钾反应的探究
(3)在不同条件下KClO3可将KI氧化为I2或KIO3.该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录表如下(实验在室温下进行):
| 试管编号 | 1 | 2 | 3 | 4 |
| 0.20mol•L-1KI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
| KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
| 6.0mol•L-1H2SO4/mL | 0 | 3.0 | 6.0 | 9.0 |
| 蒸馏水 | 9.0 | 6.0 | 3.0 | 0 |
| 实验现象 |
②设计1号试管实验的作用是___.
③若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色;假设氧化产物唯一,还原产物为KCl,则此反应的离子方程式为___.
实验三 测定饱和氯水中氯元素的总量
(4)该小组设计的实验方案为:使用图2装置,加热15.0ml饱和氯水试样,测定产生气体的体积.此方案是否可行___(填“是”或“否”)
(5)另一小组研究出的方案是,量取一定量的试样,加入足的H2O2溶液,加热除去过量的H2O2,冷却,再加入足量的硝酸银溶液,还需进行的操作是___
已知:次氯酸或氯水可被SO2、H2O2、FeCl2等物质还原成Cl-.
▼优质解答
答案和解析
实验一制取氯酸钾和氯水
(1)制取实验结束后,取出B中试管,进行冷却结晶操作需要烧杯、过滤需要漏斗和玻璃棒,洗涤需要玻璃仪器烧杯盛放液体,需用玻璃棒引流、需用胶头滴管移取少量液体,制取实验结束后,取出B中试管冷却结晶、过滤、洗涤.该实验操作过程需要的玻璃仪器有胶头滴管、烧杯外,还需要的玻璃仪器是漏斗、玻璃棒,
故答案为:漏斗、玻璃棒;
(2)实验室用二氧化锰和浓盐酸来制取氯气,制得的氯气中含有氯化氢,HCl极易溶于水,能和KOH反应生成KCl杂质,若对调B和C装置,可以除去氯化氢杂质,能提高B中氯酸钾的产率,
故答案为:能;
实验二氯酸钾与碘化钾反应的探究
(3)①根据表格数据分析:对照试管1、2、3、4中数据发现都是0.20mol•L-1KI/mL,KClO3(s)0.10g,改变的只有硫酸的体积和水的量,所以研究的目的是研究反应体系中硫酸浓度对反应产物的影响,
故答案为:研究反应体系中硫酸浓度对反应产物的影响;
②1号试管硫酸浓度为0,设计1号试管实验的作用是做对照实验,比较硫酸浓度影响反应产物,
故答案为:硫酸浓度为0的对照实验;
③若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色说明有碘单质生成,假设氧化产物唯一,还原产物为氯化钾,Cl(+5→-1)I(-1→0),根据氧化还原反应中电子守恒和原子守恒,该反应的离子方程式为:ClO3-+6I-+6H+=Cl-+3I2+3H2O,
故答案为:ClO3-+6I-+6H+=Cl-+3I2+3H2O;
实验三测定饱和氯水中氯元素的总量
(4)氯气能溶于水且能和水反应Cl2+H2O⇌HCl+HClO,次氯酸不稳定易分解2HClO
2HCl+O2↑,因存在氯气的重新溶解以及次氯酸分解等,此方案无法测算试样含氯总量,
故答案为:否;
(5)根据题干信息次氯酸会破坏酸碱指示剂,因此实验设计时不用酸碱指示剂,可以利用氯水的强氧化性,向该溶液中加入足量的H2O2溶液,发生氧化还原,H2O2被氧化变为O2,氯气被还原成Cl-,充分反应,再加入足量的硝酸银溶液,发生沉淀反应Ag++Cl-=AgCl↓产生沉淀,称量沉淀质量,根据氯元素守恒确定氯元素的质量,量取一定量的试样,加入足的H2O2溶液,加热除去过量的H2O2,冷却,再加入足量的硝酸银溶液,还需进行的操作是过滤、洗涤、干燥、称量沉淀质量,
故答案为:过滤、洗涤、干燥、称量沉淀质量.
(1)制取实验结束后,取出B中试管,进行冷却结晶操作需要烧杯、过滤需要漏斗和玻璃棒,洗涤需要玻璃仪器烧杯盛放液体,需用玻璃棒引流、需用胶头滴管移取少量液体,制取实验结束后,取出B中试管冷却结晶、过滤、洗涤.该实验操作过程需要的玻璃仪器有胶头滴管、烧杯外,还需要的玻璃仪器是漏斗、玻璃棒,
故答案为:漏斗、玻璃棒;
(2)实验室用二氧化锰和浓盐酸来制取氯气,制得的氯气中含有氯化氢,HCl极易溶于水,能和KOH反应生成KCl杂质,若对调B和C装置,可以除去氯化氢杂质,能提高B中氯酸钾的产率,
故答案为:能;
实验二氯酸钾与碘化钾反应的探究
(3)①根据表格数据分析:对照试管1、2、3、4中数据发现都是0.20mol•L-1KI/mL,KClO3(s)0.10g,改变的只有硫酸的体积和水的量,所以研究的目的是研究反应体系中硫酸浓度对反应产物的影响,
故答案为:研究反应体系中硫酸浓度对反应产物的影响;
②1号试管硫酸浓度为0,设计1号试管实验的作用是做对照实验,比较硫酸浓度影响反应产物,
故答案为:硫酸浓度为0的对照实验;
③若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色说明有碘单质生成,假设氧化产物唯一,还原产物为氯化钾,Cl(+5→-1)I(-1→0),根据氧化还原反应中电子守恒和原子守恒,该反应的离子方程式为:ClO3-+6I-+6H+=Cl-+3I2+3H2O,
故答案为:ClO3-+6I-+6H+=Cl-+3I2+3H2O;
实验三测定饱和氯水中氯元素的总量
(4)氯气能溶于水且能和水反应Cl2+H2O⇌HCl+HClO,次氯酸不稳定易分解2HClO
| ||
故答案为:否;
(5)根据题干信息次氯酸会破坏酸碱指示剂,因此实验设计时不用酸碱指示剂,可以利用氯水的强氧化性,向该溶液中加入足量的H2O2溶液,发生氧化还原,H2O2被氧化变为O2,氯气被还原成Cl-,充分反应,再加入足量的硝酸银溶液,发生沉淀反应Ag++Cl-=AgCl↓产生沉淀,称量沉淀质量,根据氯元素守恒确定氯元素的质量,量取一定量的试样,加入足的H2O2溶液,加热除去过量的H2O2,冷却,再加入足量的硝酸银溶液,还需进行的操作是过滤、洗涤、干燥、称量沉淀质量,
故答案为:过滤、洗涤、干燥、称量沉淀质量.
看了某化学兴趣小组制取氯酸钾和氯水...的网友还看了以下:
下列说法中正确的是()A.江河水有自净作用,因此河水不会被污染B.我国水资源非常丰富,无需节约用水 2020-04-09 …
下列关于水的说法中正确的是()A.水结成冰后体积变小B.生活中最常用的硬水软化方法是蒸馏C.水中加 2020-05-13 …
下列关于海水知识的叙述不正确的是()A.海水既苦又涩,不能直接利用B.海水资源的利用包括海水水资源 2020-05-16 …
身处偏远海岛,按图所示方法可获取少量的淡水.阳光的照射使池内海水加快,形成水蒸气;水蒸气在塑料膜上 2020-05-16 …
身处偏远海岛,按图所示方法可获取少量的淡水.阳光的照射使池内海水加快,形成水蒸气;水蒸气在塑料膜上 2020-05-16 …
如果一个池塘中,只放养鲢鱼和鳙鱼,从充分利用水域空间来说,不足之处()A.水的上层未被利用B.水的 2020-05-17 …
《本草纲目》中说西瓜甘寒无毒,不仅“消烦止渴、解暑热“,而且”宽中下气、利小水、治血痢、解酒毒、治 2020-06-19 …
小明在生物课上学习了“植物体对水的吸收、利用和散失”的知识后,利用食盐水、新鲜冬瓜和自制简易“密度 2020-07-10 …
某学习小组的同学发现利用矿泉水瓶可以做许多小实验:(1)小方用一满瓶纯净水和放在水平桌面上的海绵做 2020-07-30 …
阅读下列材料,回答下列小题。材料一:天荒坪电站位于浙江安吉。该电站分上下水库,晚上利用其它电厂过剩电 2020-11-30 …