早教吧作业答案频道 -->化学-->
BaCl2常用作分析试剂,也常直接用于制造钡盐以及电子、仪表、冶金等工业.我国目前比较成熟的生产BaCl2•xH2O的工艺是以重晶石(主要成分BaSO4,杂质为Fe2O3)、无烟煤粉和盐酸为原料生产
题目详情
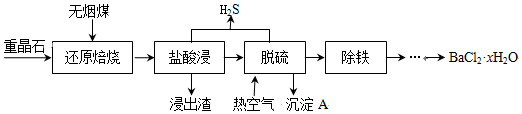
BaCl2常用作分析试剂,也常直接用于制造钡盐以及电子、仪表、冶金等工业.我国目前比较成熟的生产BaCl2•xH2O的工艺是以重晶石(主要成分BaSO4,杂质为Fe2O3)、无烟煤粉和盐酸为原料生产,流程如图所示(部分产物已略去).
(1)写出BaCl2的电子式___.
(2)“还原焙烧”时,使过量的无烟煤粉和重晶石粉混合物在高温下发生反应,该反应的化学方程式为___.
(3)“盐酸浸”得到的是氯化钡粗液,其中残余的含硫化合物会影响产品质量,必须通过鼓入热空气吹除.鼓入热空气能有效去杂的原理是___.
(4)生产过程中所产生的尾气含有毒性较高的H2S,为防止环境污染,必须进行吸收处理,下列不可行的吸收液是___.
A.CuSO4溶液B.浓硫酸C.NaHS溶液D.氨水
(5)随着工艺条件的不同,产品BaCl2•xH2O中的x数值有所不同.产品检验部门通常采用的操作是:Ⅰ称取样品a g;Ⅱ充分加热;Ⅲ置于___中冷却;Ⅳ称量质量为b g.由此可得出x=___(请写出计算表达式).
(6)工业检测MgCl2•xH2O中的x值时不用以上加热法,而多采用沉淀滴定法,其原因是(用化学方程式表示)___.沉淀滴定的测定步骤为:称取0.5000g待测产品,用适量硝酸溶解,滴加指示剂,用AgNO3标准溶液滴定.
根据上表数据分析,该滴定可选用___作指示剂.使用该指示剂时,判断滴定达到终点的现象是___.

(1)写出BaCl2的电子式___.
(2)“还原焙烧”时,使过量的无烟煤粉和重晶石粉混合物在高温下发生反应,该反应的化学方程式为___.
(3)“盐酸浸”得到的是氯化钡粗液,其中残余的含硫化合物会影响产品质量,必须通过鼓入热空气吹除.鼓入热空气能有效去杂的原理是___.
(4)生产过程中所产生的尾气含有毒性较高的H2S,为防止环境污染,必须进行吸收处理,下列不可行的吸收液是___.
A.CuSO4溶液B.浓硫酸C.NaHS溶液D.氨水
(5)随着工艺条件的不同,产品BaCl2•xH2O中的x数值有所不同.产品检验部门通常采用的操作是:Ⅰ称取样品a g;Ⅱ充分加热;Ⅲ置于___中冷却;Ⅳ称量质量为b g.由此可得出x=___(请写出计算表达式).
(6)工业检测MgCl2•xH2O中的x值时不用以上加热法,而多采用沉淀滴定法,其原因是(用化学方程式表示)___.沉淀滴定的测定步骤为:称取0.5000g待测产品,用适量硝酸溶解,滴加指示剂,用AgNO3标准溶液滴定.
| AgCl | AgI | Ag2CrO4 | |
| Ksp | 2×10-10 | 8.3×10-17 | 2×10-12 |
| 颜色 | 白 | 黄 | 砖红 |
▼优质解答
答案和解析
(1)氯化钡是离子晶体,钡离子和氯离子之间以离子键结合,氯化钡的电子式为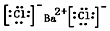 ,
,
故答案为: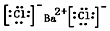 ;
;
(2)使过量的无烟煤粉和重晶石粉(BaSO4)混合物在高温下发生反应生产BaS和碳的氧化物,无烟煤粉过量,则为CO,反应为:BaSO4+4C
BaS+4CO↑;
故答案为:BaSO4+4C
BaS+4CO↑;
(3)升高温度可降低H2S的溶解度,利于吹出;升高温度,利于使H2S氧化成S沉淀除去,则含硫化合物通过鼓入热空气吹除去;
故答案为:升高温度可降低H2S的溶解度,利于吹出;升高温度,利于使H2S氧化成S沉淀除去;
(4)A.CuSO4溶液与H2S气体生成CuS沉淀,A正确;
B.浓硫酸与H2S气体可能生成二氧化硫气体,污染环境,B错误;
C.NaHS溶液不能吸收H2S气体,C错误;
D.H2S气体为酸性气体,氨水可吸收生成铵盐,D正确;
故答案为:BC;
(5)BaCl2•xH2O中
=
,则需要其中水和BaCl2的质量,故方法为:称取样品a g;Ⅱ充分加热;Ⅲ置于干燥器中冷却;Ⅳ称量质量为b g,其中m(BaCl2)=bg,m(H2O)=(a-b)g,故
=
=
=
;
故答案为:干燥器;
;
(6)检测MgCl2•xH2O中的x值时不用加热法,因为镁离子水 MgCl2•xH2O
MgO+2HCl+(x-1)H2O;根据数据可知,先沉淀生成AgCl,加入Na2CrO4,计量点时,氯离子反应完全,继续滴加AgNO3标准溶液,生成砖红色沉淀Ag2CrO4,故终点为:当滴入最后一滴AgNO3溶液出现砖红色沉淀,放置30s砖红色不消失;
故答案为:MgCl2•xH2O
MgO+2HCl+(x-1)H2O;Na2CrO4;当滴入最后一滴AgNO3溶液出现砖红色沉淀,放置30s砖红色不消失.
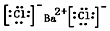 ,
,故答案为:
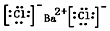 ;
;(2)使过量的无烟煤粉和重晶石粉(BaSO4)混合物在高温下发生反应生产BaS和碳的氧化物,无烟煤粉过量,则为CO,反应为:BaSO4+4C
| ||
故答案为:BaSO4+4C
| ||
(3)升高温度可降低H2S的溶解度,利于吹出;升高温度,利于使H2S氧化成S沉淀除去,则含硫化合物通过鼓入热空气吹除去;
故答案为:升高温度可降低H2S的溶解度,利于吹出;升高温度,利于使H2S氧化成S沉淀除去;
(4)A.CuSO4溶液与H2S气体生成CuS沉淀,A正确;
B.浓硫酸与H2S气体可能生成二氧化硫气体,污染环境,B错误;
C.NaHS溶液不能吸收H2S气体,C错误;
D.H2S气体为酸性气体,氨水可吸收生成铵盐,D正确;
故答案为:BC;
(5)BaCl2•xH2O中
| 1 |
| n |
| n(BaCl2) |
| n(H2O) |
| 1 |
| n |
| n(BaCl2) |
| n(H2O) |
| b÷208 |
| (a-b)÷18 |
| 208(a-b) |
| 18b |
故答案为:干燥器;
| 208(a-b) |
| 18b |
(6)检测MgCl2•xH2O中的x值时不用加热法,因为镁离子水 MgCl2•xH2O
| ||
故答案为:MgCl2•xH2O
| ||
看了BaCl2常用作分析试剂,也常...的网友还看了以下:
某厂生产A与B两种产品,每公斤的产值分别为600元与400元,又知每生产1公斤A产品需要电力2千瓦 2020-05-14 …
设10件产品有4件不合格,从中任取2件.已知所取2件产品中有1件不合格品,求另一件也不合格的概率. 2020-06-23 …
有关概率的几个问题1.设10件产品中有4件不合格品,从中任取两件,已知所取的2件产品中有一件事不合 2020-06-23 …
用A型和B型机器生产同样产品,已知5台A型机器一天的产品装满8箱后还剩6个,7台B型机器一天的产品 2020-06-28 …
数学奥林匹克小丛书设S为非空数集,且满足:2不属于S补充条件:若a属于S,则1/(2-a)也属于S 2020-07-11 …
关于保护文化遗产的英语作文.80%的学生认为保护文化遗产很重要.他们有三个理由.1文化遗产是古代文 2020-07-17 …
判断题!1.一条绳子长1/2米,用去1/2后,还剩下1/2.()2.生产一批产品中100件合格,1 2020-08-01 …
双酚A,也称BPA,用来生产防碎塑料的原料。欧盟认为含双酚A奶瓶会诱发性早熟,从2011年3月2日起 2020-11-02 …
下表是abc三类投资理财产品2015年各时段的收益率情况,下列分析比较可靠的是()时间a产品b产品c 2020-11-03 …
下列是A、B、C三类投资理财产品2015年的收益率情况,下列分析比较可靠的是()产品类型时间A类产品 2020-11-03 …