纳米氧化镁具有特殊的热、光、电、力学等性能,下图是利用海水制备纳米氧化镁的流程图。已知:Ksp(MgCO3)=6.8×10-6,Ksp[Mg(OH)2]=1.8×10-11。回答下列问题
纳米氧化镁具有特殊的热、光、电、力学等性能,下图是利用海水制备纳米氧化镁的流程图。已知: K sp (MgCO 3 )=6.8×10 - 6 , K sp [Mg(OH) 2 ]=1.8×10 - 11 。
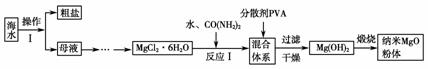
回答下列问题:
(1)操作Ⅰ后在室温下测得母液中镁离子浓度为1.8×10 - 3 mol·L - 1 ,要使镁离子产生沉淀,溶液的pH最低应为________。
(2)反应Ⅰ中CO(NH 2 ) 2 与H 2 O反应生成CO 2 和NH 3 ·H 2 O,还发生的另一主要化学反应的离子方程式为____ ___________________________。
___________________________。
(3)某科研小组研究反应Ⅰ在温度为378~398 K时的反应时间、反应物配比等因素对制备纳米氧化镁产率的影响。请完成以下实验设计表(表中不要留空格):
| 实验 编号 | T /K | 反应 时间/h | 反应物的物质的量配比 n [CO(NH 2 ) 2 ]∶ n (MgCl 2 ·6H 2 O) | 实验目的 |
| ① | 378 | 3 | 3∶1 | (1)实验①和③探究________。 (2)实验②和④探究________。 (3)实验②和________探究反应时间对产率的影响。 |
| ② | 378 | 4 | 4∶1 | |
| ③ | 378 | 3 | ||
| ④ | 398 | 4 | 4∶1 |
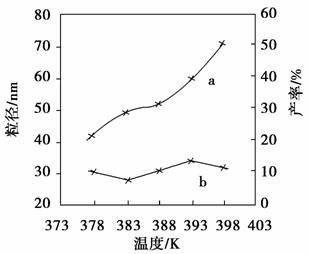
(4)如图为反应Ⅰ的温度对纳米MgO产率(曲线a)和粒径(曲线b)的影响,请你归纳出温度对纳米MgO的制备有何影响(至少写出一条):___________________________________。
“尔辈亦鹰犬”中的若等是什么意思?昔有一少年,家甚贫,伐薪自食,夜则映月读书.邻村有富者,衣锦肉食 2020-06-15 …
心无障则所学蜡等中的“蜡等”是什么意思? 2020-07-06 …
179×4的约等是多少? 2020-07-18 …
哲学中的平等是什么 2020-11-02 …
在我国,任何公民,不分民族、种族、性别、职业、家庭出身、宗教信仰、财产状况、居住期限,都一律享有平等 2020-11-02 …
在我国,公民权利的平等是多方面的,他包括()①政治权利上的平等②人身权利、经济权利平等③依法纳税、服 2020-11-07 …
人与人之间是平等的,这里所说的平等是指()A.人格和法律地位上的平等B.担任社会职务上的平等C.取得 2020-11-17 …
“人生而平等”,这里的“平等”是指()A.与人的天赋是无差别的B.与人后天的生活环境是无差别的C.生 2020-11-22 …
为什么?金星的星等是-3.81,而木星星等-2.78,但看起来好像金星没有木星亮?这几天,天一黑,在 2020-12-16 …
“只有人中人,没有人上人,也就没有人下人。”陶行知先生的这句名言精辟地说明了人与人之间应该是平等的, 2021-01-31 …