早教吧作业答案频道 -->化学-->
电解食盐水可制取NaOH和二氧化氯(ClO2)I:氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如图1:依据如图完成下列问题:(1)在电解过程中,阴极上生成气体的电子式为.精制过程中
题目详情
电解食盐水可制取NaOH和二氧化氯(ClO2)
I:氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如图1:
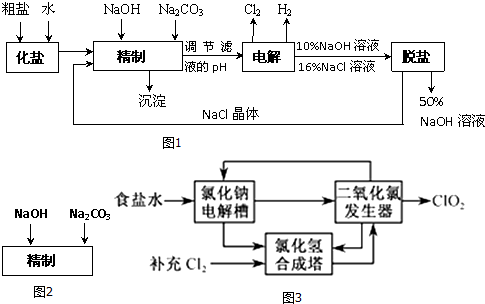
依据如图完成下列问题:
(1)在电解过程中,阴极上生成气体的电子式为___.精制过程中除去溶液中的Ca2+、Mg2+、SO42-等杂质,除去SO42-、Mg2+的最佳试剂为___.
(2)精制过程要除去SO42-,可选择下列溶液中的___(填字母序号),并将加入的顺序以箭头符号(↓)的形式画在图2(精制过程中加入试剂从左到右的顺序为先后顺序).
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
在实际生产中也可以用BaCO3除去SO42-(已知溶解度BaSO4小),试用平衡移动原理加以解释:___.
(3)脱盐工作中,利用NaOH和NaCl在溶解度上的差异,通过蒸发、冷却、___、___(填操作名称)而制得50%的NaOH溶液.
II:二氧化氯(ClO2)是一种高效、广谱、安全的杀菌、消毒剂.
氯化钠电解法是一种可靠的工业生产ClO2方法.该法工艺原理如图3.
其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2.
(4)工艺中可以利用的单质有___(填化学式),发生器中生成ClO2的化学方程式为___.
(5)纤维素还原法制ClO2是一种新方法,其原理是:纤维素水解得到的最终产物D与NaClO3反应生成ClO2.完成反应的化学方程式:
□___+24NaClO3+12H2SO4═□ClO2↑+□CO2↑+18H2O+□___
ClO2和Cl2均能将电镀废水中的CN-氧化为无毒的物质,自身被还原为Cl-.处理含CN-相同时的电镀废水,所需Cl2的物质的量是ClO2的___倍.
I:氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如图1:

依据如图完成下列问题:
(1)在电解过程中,阴极上生成气体的电子式为___.精制过程中除去溶液中的Ca2+、Mg2+、SO42-等杂质,除去SO42-、Mg2+的最佳试剂为___.
(2)精制过程要除去SO42-,可选择下列溶液中的___(填字母序号),并将加入的顺序以箭头符号(↓)的形式画在图2(精制过程中加入试剂从左到右的顺序为先后顺序).
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
在实际生产中也可以用BaCO3除去SO42-(已知溶解度BaSO4小),试用平衡移动原理加以解释:___.
(3)脱盐工作中,利用NaOH和NaCl在溶解度上的差异,通过蒸发、冷却、___、___(填操作名称)而制得50%的NaOH溶液.
II:二氧化氯(ClO2)是一种高效、广谱、安全的杀菌、消毒剂.
氯化钠电解法是一种可靠的工业生产ClO2方法.该法工艺原理如图3.
其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2.
(4)工艺中可以利用的单质有___(填化学式),发生器中生成ClO2的化学方程式为___.
(5)纤维素还原法制ClO2是一种新方法,其原理是:纤维素水解得到的最终产物D与NaClO3反应生成ClO2.完成反应的化学方程式:
□___+24NaClO3+12H2SO4═□ClO2↑+□CO2↑+18H2O+□___
ClO2和Cl2均能将电镀废水中的CN-氧化为无毒的物质,自身被还原为Cl-.处理含CN-相同时的电镀废水,所需Cl2的物质的量是ClO2的___倍.
▼优质解答
答案和解析
Ⅰ.(1)电解饱和食盐水的反应:2NaCl+2H2O
2NaOH+Cl2↑+H2↑,与正极相连为阳极,生成氯气,该电极反应为2Cl--2e-═Cl2↑,与电源负极相连为阴极,生成氢气,电极反应式为2H++2e-=H2↑,氢气的电子式为H:H,精制过程中除去溶液中的Mg2+可加入碱,除去SO42-可加入钡盐或碱,则除去SO42-、Mg2+的最佳试剂为Ba(OH)2溶液,
故答案为:H:H;Ba(OH)2溶液;
(2)添加钡试剂除去SO42-,注意不能引入新的杂质,选Ba(NO3)2会引入杂质硝酸根离子,所以选ac,SO42-、Ca2+、Mg2+等分别与BaCl2溶液、Na2CO3溶液、NaOH溶液反应生成沉淀,可再通过过滤除去,Na2CO3溶液能除去过量的BaCl2溶液,最后加入盐酸调节pH,除去过量的Na2CO3溶液和NaOH溶液,除去SO42-,则顺序为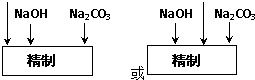 ,除去SO42-,也可加入BaCO3,因BaSO4比BaCO3的溶解度小,SO42-促使BaCO3(s)⇌Ba2+(aq)+CO32-(aq)平衡正向移动,
,除去SO42-,也可加入BaCO3,因BaSO4比BaCO3的溶解度小,SO42-促使BaCO3(s)⇌Ba2+(aq)+CO32-(aq)平衡正向移动,
故答案为:a.c; ;由于BaSO4比BaCO3的溶解度小,SO42-促使BaCO3(s)⇌Ba2+(aq)+CO32-(aq)平衡正向移动,生成更难溶的BaSO4沉淀;
;由于BaSO4比BaCO3的溶解度小,SO42-促使BaCO3(s)⇌Ba2+(aq)+CO32-(aq)平衡正向移动,生成更难溶的BaSO4沉淀;
(3)氢氧化钠的溶解度随温度的升高而增大,但是氯化钠的溶解度受温度的影响不大,所以氢氧化钠和氯化钠分离的方法是:通过加热蒸发、冷却、结晶、过滤除去NaCl,故答案为:结晶、过滤;
Ⅱ.(4)电解饱和食盐水生成H2、Cl2和NaOH;故可以利用的单质为H2、Cl2,合成HCl,根据流程图可知加入物质为NaClO3和HCl,生成ClO2;发生氧化还原反应,NaClO3被还原生成ClO2,HCl被氧化生成Cl2,同时生成水,反应的化学方程式为2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O,
故答案为:H2、Cl2; 2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O;
(5)纤维素为多糖,水解最终产物为葡萄糖(C6H12O6),具有还原性,可将NaClO3还原得到ClO2.Cl从+5到+4价,降低1价,葡萄糖(C6H12O6)C均价为0,到+4价,升高4价,则配平后的化学方程式为1 C6H12O6+24 NaClO3+12H2SO4=24 ClO2↑+6 CO2↑+18H2O+12 Na2SO4,
每摩尔Cl2得到2mol电子,而每摩尔ClO2得到5mol电子,则所需Cl2的物质的量是ClO2的2.5倍,
故答案为:1;C6H12O6;24;6;12;Na2SO4;2.5.
| ||
故答案为:H:H;Ba(OH)2溶液;
(2)添加钡试剂除去SO42-,注意不能引入新的杂质,选Ba(NO3)2会引入杂质硝酸根离子,所以选ac,SO42-、Ca2+、Mg2+等分别与BaCl2溶液、Na2CO3溶液、NaOH溶液反应生成沉淀,可再通过过滤除去,Na2CO3溶液能除去过量的BaCl2溶液,最后加入盐酸调节pH,除去过量的Na2CO3溶液和NaOH溶液,除去SO42-,则顺序为
 ,除去SO42-,也可加入BaCO3,因BaSO4比BaCO3的溶解度小,SO42-促使BaCO3(s)⇌Ba2+(aq)+CO32-(aq)平衡正向移动,
,除去SO42-,也可加入BaCO3,因BaSO4比BaCO3的溶解度小,SO42-促使BaCO3(s)⇌Ba2+(aq)+CO32-(aq)平衡正向移动,故答案为:a.c;
 ;由于BaSO4比BaCO3的溶解度小,SO42-促使BaCO3(s)⇌Ba2+(aq)+CO32-(aq)平衡正向移动,生成更难溶的BaSO4沉淀;
;由于BaSO4比BaCO3的溶解度小,SO42-促使BaCO3(s)⇌Ba2+(aq)+CO32-(aq)平衡正向移动,生成更难溶的BaSO4沉淀;(3)氢氧化钠的溶解度随温度的升高而增大,但是氯化钠的溶解度受温度的影响不大,所以氢氧化钠和氯化钠分离的方法是:通过加热蒸发、冷却、结晶、过滤除去NaCl,故答案为:结晶、过滤;
Ⅱ.(4)电解饱和食盐水生成H2、Cl2和NaOH;故可以利用的单质为H2、Cl2,合成HCl,根据流程图可知加入物质为NaClO3和HCl,生成ClO2;发生氧化还原反应,NaClO3被还原生成ClO2,HCl被氧化生成Cl2,同时生成水,反应的化学方程式为2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O,
故答案为:H2、Cl2; 2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O;
(5)纤维素为多糖,水解最终产物为葡萄糖(C6H12O6),具有还原性,可将NaClO3还原得到ClO2.Cl从+5到+4价,降低1价,葡萄糖(C6H12O6)C均价为0,到+4价,升高4价,则配平后的化学方程式为1 C6H12O6+24 NaClO3+12H2SO4=24 ClO2↑+6 CO2↑+18H2O+12 Na2SO4,
每摩尔Cl2得到2mol电子,而每摩尔ClO2得到5mol电子,则所需Cl2的物质的量是ClO2的2.5倍,
故答案为:1;C6H12O6;24;6;12;Na2SO4;2.5.
看了 电解食盐水可制取NaOH和二...的网友还看了以下:
任何离子键在形成的过程中必定有电子的得与失铵根离子是氨中的N原子提供孤对电子给氢离子,整个体系带一 2020-05-17 …
已知某植物基因行为Dd,若该职务连续多代自交,则子代群体中纯合子所占比例f(n)的数学模型为Af( 2020-06-08 …
(1)如图所示,物体A重5N,物体B重2N,A、B均处于静止状态,则绳子对物体A的拉力为N,物体A 2020-06-24 …
现有一豌豆种群(个体足够多),所有个体的基因型均为Aa,已知隐性纯合子产生的配子均没有活性,该种群 2020-06-30 …
P型半导体中的硼原子,为何是带负电的离子n型半导体中磷的原子,为何是带正电的离子?P型半导体中的硼 2020-07-05 …
一道物理题,我做了N遍,还不是很明白,希望能够得到详细的讲解用运动传感器可以测量运动物体的速度,这个 2020-11-05 …
传统的:惯例的(adj.)秋天;秋季(n.)漂泊者;旅行者;游客(n.)庆祝;庆贺(v.)甜椒;柿子 2020-11-28 …
若ABn的中心原子A上没有孤对电子,运用价层电子对互斥模型,下列说法正确的是()A、若n=2,则分子 2020-12-01 …
按要求回答下列问题:(1)气态SeO3分子的立体构型为,SO32-离子的立体构型为;(2)H+可与N 2020-12-21 …
有机立体化学中分子绕某轴转过360/n能与原分子重合,称该轴为该分子n重对称轴,n=1行吗 2020-12-26 …