早教吧作业答案频道 -->化学-->
氯元素(Cl)是最重要的“成盐元素”,主要以NaCl的形式存在于海水和陆地的盐矿中.食盐不仅是人体必需的物质,而且是重要的化工原料,从海水中提取氯并应用于工农业生产中的图示如
题目详情
氯元素(Cl)是最重要的“成盐元素”,主要以NaCl的形式存在于海水和陆地的盐矿中.食盐不仅是人体必需的物质,而且是重要的化工原料,从海水中提取氯并应用于工农业生产中的图示如下.
海水
粗盐
饱和NaCl
烧碱和氢气、氯气
(1)粗盐中含有Ca2+、Mg2+、SO42-等杂质、精制后可得饱和NaCl溶液.精制时通常在溶液中依次加入的试剂及操作正确的是___;
A.过量的BaCl2→过量NaOH→过量Na2CO3→过滤→过量HCl
B.过量的NaOH→过量Na2CO3→过量BaCl2过滤→过量HCl
C.过量的BaCl2→过量Na2CO3→过量NaOH 过滤→过量HCl
D.过量的NaOH→过量 BaCl2→过量Na2CO3过量HCl→过滤
写出加入盐酸后可能发生的化学反应的离子方程式___.
(2)工业上用电解饱和食盐水的方法制取烧碱和氢气、氯气.图E是电解饱和食盐水装置的一部分,请将装置补充完整,并标出阴阳极和通电时溶液中离子移动的方向.阴极反应式为___;反应类型___(填氧化或还原反应),总电极反应式为___.
(3)在实验室中用浓盐酸与MnO2共热可制取Cl2.
①下列收集Cl2的装置正确的是___;
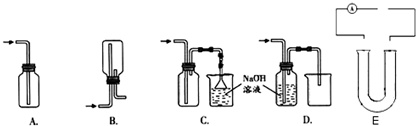
②检验是否有氯气生成可采用的方法是___;
A.用干燥的蓝色石蕊试纸 B.用干燥的有色布条
C.用湿润的淀粉碘化钾试 D.将气体通入硝酸银溶液
③将制得的Cl2与Ca(OH)2充分反应,可制得漂粉精,写出反应的化学方程式___.
海水
| 结晶 |
| |
| 精制 |
| |
| 电解 |
| |
(1)粗盐中含有Ca2+、Mg2+、SO42-等杂质、精制后可得饱和NaCl溶液.精制时通常在溶液中依次加入的试剂及操作正确的是___;
A.过量的BaCl2→过量NaOH→过量Na2CO3→过滤→过量HCl
B.过量的NaOH→过量Na2CO3→过量BaCl2过滤→过量HCl
C.过量的BaCl2→过量Na2CO3→过量NaOH 过滤→过量HCl
D.过量的NaOH→过量 BaCl2→过量Na2CO3过量HCl→过滤
写出加入盐酸后可能发生的化学反应的离子方程式___.
(2)工业上用电解饱和食盐水的方法制取烧碱和氢气、氯气.图E是电解饱和食盐水装置的一部分,请将装置补充完整,并标出阴阳极和通电时溶液中离子移动的方向.阴极反应式为___;反应类型___(填氧化或还原反应),总电极反应式为___.
(3)在实验室中用浓盐酸与MnO2共热可制取Cl2.
①下列收集Cl2的装置正确的是___;

②检验是否有氯气生成可采用的方法是___;
A.用干燥的蓝色石蕊试纸 B.用干燥的有色布条
C.用湿润的淀粉碘化钾试 D.将气体通入硝酸银溶液
③将制得的Cl2与Ca(OH)2充分反应,可制得漂粉精,写出反应的化学方程式___.
▼优质解答
答案和解析
(1)要先除硫酸根离子,然后再除钙离子,Na2CO3可以除去过量的钡离子,否则过量的钡离子不能完全除尽,至于加NaOH除去镁离子顺序不受限制,可放在加入BaCl2之前或之后,因为过量的NaOH加HCl就可以调节了,只要将三...
看了氯元素(Cl)是最重要的“成盐...的网友还看了以下:
有些化学变化可用“A+B→C+D”的式子来表示.(1)在四种基本反应类型中,可用上式表示的是反应和 2020-05-13 …
10Gbps Ethernet 工作在A 单工方式B 半双工方式C 全双工方式D 自动协商方式 2020-05-23 …
et工作在( )。A)单工方式 B)半双工方式C)全双工方式 D)自动协商方式 2020-05-23 …
10Gbps Ethernet工作在( )。A)单工方式B)半双工方式 C)全双工方式D)自动协商方 2020-05-23 …
10Gbit/s Ethernet工作在______。A.单工方式B.半双工方式C. 全双工方式D. 2020-05-23 …
10 Gbps Ethernet采用的通信方式是______。A.半双工方式B.全双工方式C. 单工 2020-05-23 …
10Gbps Ethernet工作在()。A.单工方式B.半双工方式C.全双工方式D.自动协商方式 2020-05-23 …
Intel 8251A不可以工作在______( )A.同步方式B.异步方式C.全双工方式D.半双工 2020-05-24 …
Intel 825lA可以工作在( )。A.同步方式B.异步方式C.全双工方式D.以上都对 2020-05-24 …
IPSEC密钥协商方式有()。A、一种手工方式B、两种手工方式IKE自动协商C、一种IKE自动协商D 2020-05-26 …