早教吧作业答案频道 -->化学-->
水资源与我们的生产、生活息息相关.(1)硬水软化常用离子交换法,NaR型离子交换树脂使用一段时间后,逐渐失去交换能力,将树脂置于中浸泡一段时间都可再生,当洗涤用水硬度较大
题目详情
水资源与我们的生产、生活息息相关.
(1)硬水软化常用离子交换法,NaR型离子交换树脂使用一段时间后,逐渐失去交换能力,将树脂置于___中浸泡一段时间都可再生,当洗涤用水硬度较大时,洗衣粉与肥皂相比洗涤效果更好,其原因是___.
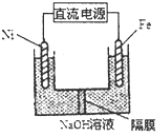
(2)Na2FeO4是一种既能杀菌、消毒,又能净水的水处理剂,其原理是___,Na2FeO4的电解制法如图所示,请写出阳极的电极反应式___.
(3)生活污水常含有大量的含氯化合物,可用生物膜脱氯工艺进行处理,首先在硝化细菌的作用下,将NH4+氧化成NO3-,其原理为aNH4++bO2=cH++dNO3-+eH2O,反应化学方程式b=___,该过程需要控制水温为20℃~36℃,其原因是___.硝化后加入甲醇与NO3-生成N3,该过程中甲醇的作用是___.
(4)锂铜废水中含有Cr2O72-,常加入Na2S2O3溶液进行处理后排放,加入Na2S2O3溶液之前将废水调整至较强的酸性环境,原因是___.取少量处理后的水样于试管中,加入NaOH溶液产生蓝色沉淀,要使该蓝色沉淀溶解,除了加入酸之外,还可以加入氨水生成[Cu(NH3)4]2+,该反应的离子方程式为___.
(1)硬水软化常用离子交换法,NaR型离子交换树脂使用一段时间后,逐渐失去交换能力,将树脂置于___中浸泡一段时间都可再生,当洗涤用水硬度较大时,洗衣粉与肥皂相比洗涤效果更好,其原因是___.
(2)Na2FeO4是一种既能杀菌、消毒,又能净水的水处理剂,其原理是___,Na2FeO4的电解制法如图所示,请写出阳极的电极反应式___.

(3)生活污水常含有大量的含氯化合物,可用生物膜脱氯工艺进行处理,首先在硝化细菌的作用下,将NH4+氧化成NO3-,其原理为aNH4++bO2=cH++dNO3-+eH2O,反应化学方程式b=___,该过程需要控制水温为20℃~36℃,其原因是___.硝化后加入甲醇与NO3-生成N3,该过程中甲醇的作用是___.
(4)锂铜废水中含有Cr2O72-,常加入Na2S2O3溶液进行处理后排放,加入Na2S2O3溶液之前将废水调整至较强的酸性环境,原因是___.取少量处理后的水样于试管中,加入NaOH溶液产生蓝色沉淀,要使该蓝色沉淀溶解,除了加入酸之外,还可以加入氨水生成[Cu(NH3)4]2+,该反应的离子方程式为___.
▼优质解答
答案和解析
(1)硬水软化的方法离子交换法中用磺化煤(NaR)作离子交换剂:2NaR+Ca2+=CaR2+2Na+,2NaR+Mg2+=MgR2+2Na+,用5%-8%的食盐水浸泡可使失去软化能力的磺化煤再生:CaR2+2Na+=2NaR+Ca2+,MgR2+2Na+=2NaR+Mg2+;肥皂易与Ca2+,Mg2+生成硬脂酸钙、硬脂酸镁沉淀,洗涤效果不好,洗衣粉不与Ca2+,Mg2+生成沉淀,洗涤效果较好,
故答案为:5%-8%的食盐水;肥皂的主要成分是硬脂酸钠,电离出的硬脂酸根离子易与Ca2+,Mg2+结合成沉淀,而主要成分为表面活性剂的洗衣粉可以避免这种情况;
(2)电解时阳极发生氧化反应,电极反应方程式为Fe+8OH--6e-═FeO42-+4H2O;Na2FeO4能消毒、净水的原因高价铁具有氧化性,能消毒杀菌,生成Fe3+形成胶体,具有吸附悬浮物的净水的作用;
故答案为:Na2FeO4具有强氧化性,能起到杀菌、消毒作用;高价的铁被还原成的Fe3+水解生成Fe(OH)3胶体,能吸附水中杂质;Fe+8OH--6e-=FeO42-+4H2O;
(3)反应中,N元素的化合价升高了8价,O的化合价降低了4价,所以氧气的前边时系数2,根据电子守恒和元素守恒,得到NH4++2O2=NO3-+2H++H2O,该过程需要控制水温为20℃~36℃,因为:温度过高或过低对硝化菌均有抑制作用,甲醇与NO3-生成N3,氮元素的化合价降低了,所以甲醇中元素的化合价会升高,即甲醇做还原剂,故答案为:2;温度过高或过低对硝化菌均有抑制作用;做还原剂;
(5)Cr2O72-、S2O32-之间可以发生氧化还原反应,加入Na2S2O3溶液之前将废水调整至较强的酸性环境,是因为酸性环境下,氧化剂的氧化性更强,处理后的水样于试管中,加入NaOH溶液产生蓝色氢氧化铜沉淀,向该蓝色沉淀加入氨水生成[Cu(NH3)4]2+,发生反应的离子方程式为:Cu(OH)2+4NH3•H2O=[Cu(NH3)4]2++4H2O+2OH-.故答案为:酸性条件下Cr2O72-氧化性更强,有利于反应的进行;Cu(OH)2+4NH3•H2O=[Cu(NH3)4]2++4H2O+2OH-.
故答案为:5%-8%的食盐水;肥皂的主要成分是硬脂酸钠,电离出的硬脂酸根离子易与Ca2+,Mg2+结合成沉淀,而主要成分为表面活性剂的洗衣粉可以避免这种情况;
(2)电解时阳极发生氧化反应,电极反应方程式为Fe+8OH--6e-═FeO42-+4H2O;Na2FeO4能消毒、净水的原因高价铁具有氧化性,能消毒杀菌,生成Fe3+形成胶体,具有吸附悬浮物的净水的作用;
故答案为:Na2FeO4具有强氧化性,能起到杀菌、消毒作用;高价的铁被还原成的Fe3+水解生成Fe(OH)3胶体,能吸附水中杂质;Fe+8OH--6e-=FeO42-+4H2O;
(3)反应中,N元素的化合价升高了8价,O的化合价降低了4价,所以氧气的前边时系数2,根据电子守恒和元素守恒,得到NH4++2O2=NO3-+2H++H2O,该过程需要控制水温为20℃~36℃,因为:温度过高或过低对硝化菌均有抑制作用,甲醇与NO3-生成N3,氮元素的化合价降低了,所以甲醇中元素的化合价会升高,即甲醇做还原剂,故答案为:2;温度过高或过低对硝化菌均有抑制作用;做还原剂;
(5)Cr2O72-、S2O32-之间可以发生氧化还原反应,加入Na2S2O3溶液之前将废水调整至较强的酸性环境,是因为酸性环境下,氧化剂的氧化性更强,处理后的水样于试管中,加入NaOH溶液产生蓝色氢氧化铜沉淀,向该蓝色沉淀加入氨水生成[Cu(NH3)4]2+,发生反应的离子方程式为:Cu(OH)2+4NH3•H2O=[Cu(NH3)4]2++4H2O+2OH-.故答案为:酸性条件下Cr2O72-氧化性更强,有利于反应的进行;Cu(OH)2+4NH3•H2O=[Cu(NH3)4]2++4H2O+2OH-.
看了水资源与我们的生产、生活息息相...的网友还看了以下:
物体运动速度越快,质量越大,时间变慢.达到多快的速度才能做到正常空间下已过1年,特殊空间下才过1秒 2020-05-16 …
高难度(植树问题,高难度)沿高速公路一旁种杨树,每隔3米种一棵,一共种了251棵,后来,由于实际需 2020-06-13 …
在一条笔直的公路上,有一些树和灯,每相邻的两盏灯之间有3棵树,相邻树与树、树与灯之间的距离是10m 2020-06-18 …
卷尾猴性情温顺,平时喜欢生活在树上,常常夜间外出,捕食昆虫、蜗牛等小型无脊椎动物,也吃一些植物性食物 2020-11-02 …
1.开头引用故事有什么好处?2.先将括号里的句子改为陈述句,再体会变换后的表达效果有何不同?一个男孩 2020-11-11 …
下列关于种群特征描述不正确的是()A.大量诱杀雄性个体会影响种群的密度B.橡树种子常在母树附近形成集 2020-12-23 …
在一条笔直的公路边,有一些树和路灯,每相邻的两盏灯之间有3棵树,相邻的树与树,树与灯间的距离是10c 2020-12-27 …
在一条笔直的公路边,有一些树和路灯,每相邻的两盏灯之间有3棵树,相邻的树与树、树与灯间的距离都是10 2020-12-27 …
在一条笔直的公路边,有一些树和路灯,每相邻的两盏灯之间有3棵树,相邻的树与树,树与灯间的距离是10m 2020-12-27 …
电影《致我们终将逝去的青春》放映后激起了很多人对青春的回忆,青春期是人生的关键时期.下列选项中,有利 2020-12-30 …