已知某温度下CH3COOH和NH3·H2O的电离常数相等,现向10mL浓度为0.1mol·L-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中A.水的电离程度先减小再增大B.始终增大C.n(CH3COOH)
已知某温度下CH3COOH和NH3·H2O的电离常数相等,现向10 mL浓度为0.1 mol·L-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中
A.水的电离程度先减小再增大
B.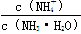 始终增大
始终增大
C.n (CH3COOH)与n (CH3COO-)之和始终保持不变
D.当加入氨水的体积为10 mL时,溶液的PH一定为7
分 析:
A. 醋酸电离:CH3COOH CH3COO-+H+,一水合氨电离:NH3H2O NH4++OH-,H2O的电离:H2O H++OH-,所以开始滴加氨水时,中和了醋酸电离出的H+使水的电离程度增大,当二者恰好完全反应后,再滴加氨水,会抑制水的电离,使其电离程度减小,A错误;B、因为NH3H2O的电离常数Kb= c(OH-)c(NH4+)/c(NH3H2O),所以c(NH4+)/c(NH3H2O)=Kb/c(OH-),因为Kb不变,c(OH-)逐渐增大,所以c(NH4+)/c(NH3H2O)始终减小,故B错误;C、根据原子守恒,n(CH3COOH)与n(CH3COO)之和是定值,故C正确;D、当加入氨水的体积为10mL时,CH3COOH和NH3H2O恰好完全反应,因为CH3COOH和NH3H2O 的电离常数相等, 则同浓度NH4+和CH3COO的水解程度相等,所以CH3COONH4呈中性,但由于不知温度,PH不能确定,故D错误。
考点:
了解水的电离,离子积常数。了解弱电解质在水中的电离平衡及影响因素和电离常数的意义。
下列说法正确的是()A.已知0.1mol•L-1的醋酸溶液中存在电离平衡:CH3COOH⇌CH3C 2020-05-14 …
变限积分求道问题对函数f(t+h)-f(t-h)在[-h,h]上的积分对h求导.F(h)=∫[-h 2020-05-23 …
什么是译音用字?我在字典里查“呵”字,出现下面结果:您查询的字是:呵?多音字:hē,hā,ā(一) 2020-06-12 …
已知0.1mol/L的醋酸溶液中存在电离平衡:CH3COOH⇌CH3COO-+H+,要使溶液中c( 2020-06-27 …
收入的增长,一个是绝对增长,取决于微观领域内企业内部的机制,国家可以考虑为企业员工工资增长制定基本的 2020-11-03 …
收入的增长,一个是绝对增长,取决于微观领域内企业内部的机制,国家可以考虑为企业员工工资增长制定基本的 2020-11-03 …
读下图,该国2010年人口增长的特点是2010年某国人口年龄人数统计图A.高出生率,高死亡率,高增长 2020-11-11 …
人口的急剧增长为人类生存和发展带来一系列的问题.读漫画“愁”,完成38-40题:人口增长过快带来的问 2020-12-19 …
,,我道理哪里理解错了.例如CH3COOH↔CH3COO-+H+若增大H+的浓度,则反应向逆反应方向 2021-01-12 …
收入的增长,一个是绝对增长,取决于微观领域内企业内部的机制,国家可以考虑为企业员工工资增长制定基本的 2021-01-13 …