早教吧作业答案频道 -->化学-->
(1)基态铬原子的价电子排布式为.(2)CrO2Cl2和NaClO均可作化工生产的氧化剂或氯化剂.制备CrO2Cl2的反应为:K2Cr2O7+3CCl4═2KCl+2CrO2Cl2+3COCl2↑.上述反应式中非金属元素电负性由大到小的
题目详情
(1)基态铬原子的价电子排布式为___.
(2)CrO2Cl2和NaClO均可作化工生产的氧化剂或氯化剂.制备CrO2Cl2的反应为:K2Cr2O7+3CCl4═2KCl+2CrO2Cl2+3COCl2↑.上述反应式中非金属元素电负性由大到小的顺序是___(用元素符号表示).
(3)随着人们生活质量的提高,室内的环境安全和食品安全越来越为人们所关注.甲醛(HCHO)是室内主要空气污染物之一(其沸点是-19.5℃),甲醇(CH3OH)是“假酒”中的主要有害物质(其沸点是64.65℃),甲醇的沸点明显高于甲醛的主要原因是___
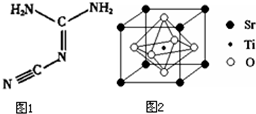
(4)双氰胺结构简式如图1所示.
①双氰胺分子中σ键和π键数目之比为___.
②双氰胺分子碳原子的杂化类型为___.
(5)镍元素能形成多种配合物,配离子[Ni(CN)4]2+中不含有的作用力是___(填选项编号).
A.离子键 B.配位键 C.键 D.键 E.氢键
(6)科研人员研究出以钛酸锶为电极的光化学电池,用紫外线照射钛酸锶电极,使水分解产生氢气.已知钛酸锶晶胞结构如图2所示,则其化学式为___.
(2)CrO2Cl2和NaClO均可作化工生产的氧化剂或氯化剂.制备CrO2Cl2的反应为:K2Cr2O7+3CCl4═2KCl+2CrO2Cl2+3COCl2↑.上述反应式中非金属元素电负性由大到小的顺序是___(用元素符号表示).
(3)随着人们生活质量的提高,室内的环境安全和食品安全越来越为人们所关注.甲醛(HCHO)是室内主要空气污染物之一(其沸点是-19.5℃),甲醇(CH3OH)是“假酒”中的主要有害物质(其沸点是64.65℃),甲醇的沸点明显高于甲醛的主要原因是___
(4)双氰胺结构简式如图1所示.
①双氰胺分子中σ键和π键数目之比为___.
②双氰胺分子碳原子的杂化类型为___.
(5)镍元素能形成多种配合物,配离子[Ni(CN)4]2+中不含有的作用力是___(填选项编号).
A.离子键 B.配位键 C.键 D.键 E.氢键
(6)科研人员研究出以钛酸锶为电极的光化学电池,用紫外线照射钛酸锶电极,使水分解产生氢气.已知钛酸锶晶胞结构如图2所示,则其化学式为___.

▼优质解答
答案和解析
(1)根据核外电子排布规律可以写出基态铬价电子排布式为1s22s22p63s23p63s23p63d54s1,所以基态铬(Cr)原子的价电子排布式是3d54s1;
故答案为:3d54s1;
(2)反应式中非金属元素有三种:O、C、Cl,CCl4中C表现正化合价、Cl表现负化合价,NaClO中Cl为+1价,O为-2价,电负性越大,对键合电子吸引力越大,元素相互化合时该元素表现负价,故电负性:O>Cl>C,
故答案为:O>Cl>C;
(3)甲醇分子间存在氢键,熔沸点增大,而甲醛分子间不存在氢键,故甲醇的沸点较高;
故答案为:甲醇分子间存在氢键,而甲醛分子间不存在氢键;
(4)①单键为σ键和,双键含有1个σ键、1个π键数,三键含有1个σ键、2个π键,双氰胺分子有9个σ键键、3个π键,双氰胺分子中σ键和π键数目之比为9:3=3:1;
故答案为:3:1;
②-C≡N中C原子形成2个σ键,连接氨基的C原子成3个σ键,均没有孤电子对,C原子杂化发生分别为sp、sp2;
故答案为:sp和sp2;
(5)配离子[Ni(CN)4]2-含有1个σ键,2个π键,氮镍间为配位键,不含有离子键、氢键;
故选:AE;
(6)由晶胞结构可知,晶胞中Sr原子数目为8×
=1、Ti原子数目为1、氧原子形成正八面体结构,O原子数目为6×
=3,故该物质化学式为:SrTiO3;
故答案为:SrTiO3.
故答案为:3d54s1;
(2)反应式中非金属元素有三种:O、C、Cl,CCl4中C表现正化合价、Cl表现负化合价,NaClO中Cl为+1价,O为-2价,电负性越大,对键合电子吸引力越大,元素相互化合时该元素表现负价,故电负性:O>Cl>C,
故答案为:O>Cl>C;
(3)甲醇分子间存在氢键,熔沸点增大,而甲醛分子间不存在氢键,故甲醇的沸点较高;
故答案为:甲醇分子间存在氢键,而甲醛分子间不存在氢键;
(4)①单键为σ键和,双键含有1个σ键、1个π键数,三键含有1个σ键、2个π键,双氰胺分子有9个σ键键、3个π键,双氰胺分子中σ键和π键数目之比为9:3=3:1;
故答案为:3:1;
②-C≡N中C原子形成2个σ键,连接氨基的C原子成3个σ键,均没有孤电子对,C原子杂化发生分别为sp、sp2;
故答案为:sp和sp2;
(5)配离子[Ni(CN)4]2-含有1个σ键,2个π键,氮镍间为配位键,不含有离子键、氢键;
故选:AE;
(6)由晶胞结构可知,晶胞中Sr原子数目为8×
| 1 |
| 8 |
| 1 |
| 2 |
故答案为:SrTiO3.
看了(1)基态铬原子的价电子排布式...的网友还看了以下:
1.下列加点字读音和字形全部正确的一项是()A.腌制(yān)倘若(tǎng)拧成(níng)手腕 2020-05-13 …
1.下列加点字读音和字形全部正确的一项是()A.腌制(yān)倘若(tǎng)拧成(níng)手腕 2020-05-13 …
英语单词辨音找出画()部分读音与其余不同的单词()1.A .kn(ee) B.n(e)ck C.r 2020-05-17 …
如果向量a=(1,0,1),b=(O,1,1)分别平行于平面c与d,且都与这两个平面的交线L垂直, 2020-06-27 …
下列各题中加下划线字的注音全都正确的一项是A.鞭挞tà叨光tāo体已tī孝悌tìB.殷红yīn奶酪 2020-07-02 …
这个通达信指标是什么意思内外盘差}PJ:=(H+L+C)/3;V1:=IF(H=L,1,H-MAX 2020-07-09 …
如图,直线l与O相离,过点O作OA⊥l,垂足为A,OA交O于点B,点C在直线l上,连接CB并延长交 2020-07-21 …
推断题:现有如下反应(反应条件均不给),推断物质⑴A→B+C+D⑵C+E→C+F+D⑶D+G→H⑷ 2020-07-30 …
请在下列句子中选出字音有错误的一项A.屹立yì缜密zhěn渲染xuàn慰藉jiè熨帖yùB.红绡xi 2020-11-07 …
英语:下1.将下联打乱的字母组成单词,并写出汉语意思1.a,e,h,g,c,n[]2.e,i,s,t 2020-12-10 …