早教吧作业答案频道 -->化学-->
2013年6月,我国“蛟龙”号再次刷新“中国深度”--下潜7062米,为我国深海矿物资源的开发奠定了基础.海洋深处有丰富的锰结核矿,锰结核的主要成分是MnO2,同时还含有黄铜矿.Ⅰ、“蛟
题目详情
2013年6月,我国“蛟龙”号再次刷新“中国深度”--下潜7062米,为我国深海矿物资源的开发奠定了基础.海洋深处有丰富的锰结核矿,锰结核的主要成分是MnO2,同时还含有黄铜矿.
Ⅰ、“蛟龙”号外壳是用特殊的钛合金材料制成,它可以在7000m的深海中承受重压,Ti是以钛白粉(TiO2)为原料进行生产,钛白粉是利用TiO2+发生水解生成钛酸(H2TiO3)沉淀,再煅烧沉淀制得的.TiO2+发生水解的离子方程式为___.
Ⅱ、MnO2是一种重要的无机功能材料,工业上从锰结核中制取纯净的MnO2工艺流程如图所示:
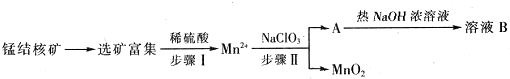
(1)步骤Ⅱ中以NaClO3为氧化剂,当生成0.05molMnO2时,消耗0.1mol/L的NaClO3溶液200ml,该反应离子方程式为___.
(2)已知溶液B的溶质之一可循环用于上述生产,此物质的名称是___.
Ⅲ、利用黄铜矿炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3等)可制备Fe2O3,方法为:
(A)用过量的稀盐酸浸取炉渣、过滤;
(B)向滤液中加入5%的H2O2,再向其中加入过量的NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得到Fe2O3
根据以上信息回答下列问题:
(1)(B)中向滤液中加入5%的H2O2,其目的是___.
(2)设计实验证明炉渣中含有FeO___.
(3)将煅烧得到的Fe2O3还原为Fe单质,再将质量为m g的Fe单质分成相等的四份,分别与50mL、100mL、150mL、200mL的等浓度的稀硝酸反应,反应产物NO在标况下的体积见附表:
则:①m=___g ②写出实验②发生反应后溶液中Fe2+与Fe3+物质的量之比为:___.
Ⅰ、“蛟龙”号外壳是用特殊的钛合金材料制成,它可以在7000m的深海中承受重压,Ti是以钛白粉(TiO2)为原料进行生产,钛白粉是利用TiO2+发生水解生成钛酸(H2TiO3)沉淀,再煅烧沉淀制得的.TiO2+发生水解的离子方程式为___.
Ⅱ、MnO2是一种重要的无机功能材料,工业上从锰结核中制取纯净的MnO2工艺流程如图所示:
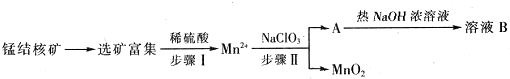
(1)步骤Ⅱ中以NaClO3为氧化剂,当生成0.05molMnO2时,消耗0.1mol/L的NaClO3溶液200ml,该反应离子方程式为___.
(2)已知溶液B的溶质之一可循环用于上述生产,此物质的名称是___.
Ⅲ、利用黄铜矿炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3等)可制备Fe2O3,方法为:
(A)用过量的稀盐酸浸取炉渣、过滤;
(B)向滤液中加入5%的H2O2,再向其中加入过量的NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得到Fe2O3
根据以上信息回答下列问题:
(1)(B)中向滤液中加入5%的H2O2,其目的是___.
(2)设计实验证明炉渣中含有FeO___.
(3)将煅烧得到的Fe2O3还原为Fe单质,再将质量为m g的Fe单质分成相等的四份,分别与50mL、100mL、150mL、200mL的等浓度的稀硝酸反应,反应产物NO在标况下的体积见附表:
| 实验 | ① | ② | ③ | ④ |
| V(HNO3)/mL | 50 | 100 | 150 | 200 |
| V(NO)/L | 1.344 | 2.688 | 3.36 | 3.36 |
▼优质解答
答案和解析
Ⅰ、TiO2+发生水解生成钛酸(H2TiO3)沉淀,则根据原子守恒可知,还有氢离子产生,因此TiO2+发生水解的离子方程式为TiO2++2H2O=H2TiO3↓+2H+,
故答案为:TiO2++2H2O=H2TiO3↓+2H+;
Ⅱ、(1)0.1mol/L的NaClO3溶液200ml的物质的量是0.02mol,当生成0.05molMnO2时,转移电子的物质的量是0.05mol×(4-2)=0.1mol,根据电子得失守恒可知0.02mol氯酸钠得到0.1mol电子,因此氯元素的化合价变化5价,即从+5价降低到0价,因此还原产物是氯气,所以该反应离子方程式为2ClO3-+5Mn2++4H2O=5MnO2+8H++Cl2↑,
故答案为:2ClO3-+5Mn2++4H2O=5MnO2+8H++Cl2↑;
(2)氯气与热的氢氧化钠溶液反应生成氯酸钠、氯化钠和水,因此可以循环的物质B是氯酸钠,
故答案为:氯酸钠;
Ⅲ、(1)滤液中含有亚铁离子,双氧水有氧化性将亚铁离子氧化为铁离子,且不会引入新的杂质,
故答案为:氧化亚铁离子;
(2)亚铁离子具有还原性,因此检验炉渣中含有FeO的实验方法是取炉渣少许,用稀硫酸浸取后的溶液使KMnO4溶液褪色,
故答案为:取炉渣少许,用稀硫酸浸取后的溶液使KMnO4溶液褪色;
(3)①根据表中数据可知实验③后硝酸是过量的,则铁与足量稀硝酸反应最多生成3.36LNO,NO的物质的量是
=0.15mol,反应中转移电子的物质的量是0.15mol×(5-2)=0.45mol,因此根据电子得失守恒可知消耗铁的物质的量是
=0.15mol,因此原铁的物质的量是0.15mol×4=0.6mol,质量是0.6mol×56g/mol=33.6g.
故答案为:33.6;
②实验②中产生NO的物质的量是
=0.12mol,转移电子的物质的量是0.36mol.设生成硝酸铁和硝酸亚铁的物质的量是xmol和ymol,则
x+y=0.15
3x+2y=0.36
解得x=0.06、y=0.09,
即硝酸铁与硝酸亚铁的物质的量之比是2:3,所以溶液中Fe2+与Fe3+物质的量之比为3:2,
故答案为:3:2.
故答案为:TiO2++2H2O=H2TiO3↓+2H+;
Ⅱ、(1)0.1mol/L的NaClO3溶液200ml的物质的量是0.02mol,当生成0.05molMnO2时,转移电子的物质的量是0.05mol×(4-2)=0.1mol,根据电子得失守恒可知0.02mol氯酸钠得到0.1mol电子,因此氯元素的化合价变化5价,即从+5价降低到0价,因此还原产物是氯气,所以该反应离子方程式为2ClO3-+5Mn2++4H2O=5MnO2+8H++Cl2↑,
故答案为:2ClO3-+5Mn2++4H2O=5MnO2+8H++Cl2↑;
(2)氯气与热的氢氧化钠溶液反应生成氯酸钠、氯化钠和水,因此可以循环的物质B是氯酸钠,
故答案为:氯酸钠;
Ⅲ、(1)滤液中含有亚铁离子,双氧水有氧化性将亚铁离子氧化为铁离子,且不会引入新的杂质,
故答案为:氧化亚铁离子;
(2)亚铁离子具有还原性,因此检验炉渣中含有FeO的实验方法是取炉渣少许,用稀硫酸浸取后的溶液使KMnO4溶液褪色,
故答案为:取炉渣少许,用稀硫酸浸取后的溶液使KMnO4溶液褪色;
(3)①根据表中数据可知实验③后硝酸是过量的,则铁与足量稀硝酸反应最多生成3.36LNO,NO的物质的量是
| 3.36L |
| 22.4L/mol |
| 0.45mol |
| 3 |
故答案为:33.6;
②实验②中产生NO的物质的量是
| 2.688L |
| 22.4L/mol |
x+y=0.15
3x+2y=0.36
解得x=0.06、y=0.09,
即硝酸铁与硝酸亚铁的物质的量之比是2:3,所以溶液中Fe2+与Fe3+物质的量之比为3:2,
故答案为:3:2.
看了2013年6月,我国“蛟龙”号...的网友还看了以下:
下列有关该国M、N两海域洋流的说法正确的是A.夏半年M海域洋流向北流B.冬半年M海域洋流向南流C. 2020-05-16 …
装订精良的大书,书上印着金灿灿的烫金字的组成[]A.锌锰合金B.铜锌合金C.铜锰合金D.铜铁合金 2020-06-17 …
选择绿色电池中不肯能含有的一组金属是?A:锌锰铜B:锂镍铜C:汞镉铅D:镍铜锰 2020-07-01 …
某校同学要比较锰、铁、铜三种金属的活动性顺序.作出猜想:猜想一:锰>铁>铜猜想二:铁>铜>锰猜想三: 2020-11-01 …
装订精良的大书,书上装订精良的大书,书上印着金灿灿的烫金字的组成[]A.锌锰合金B.铜锌合金C.铜锰 2020-11-01 …
下表是上海开往铜陵的列车时刻表:车次T7055047站点上海--铜陵上海--铜陵始发点7:504:2 2020-11-12 …
17.上海宝山钢铁厂从巴西进口的矿产资源和经济合理的运输方式是()A.锰矿铁路运输B.锰矿海洋运输C 2020-11-30 …
上海宝山钢铁厂从巴西进口的矿产资源和经济合理的运输方式是()A.锰矿铁路运输B.锰矿海洋运输C.铁矿 2020-11-30 …
金属锰具有广泛的用途,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO 2021-02-19 …
金属锰具有广泛的用途,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO 2021-02-19 …