早教吧作业答案频道 -->化学-->
草酸铜(CuC2O4•2H2O)是制备纳米CuO的前驱体,可利用草酸和印刷线路板的酸性蚀刻废液为原料制取.(1)7.6gCuC2O4在350℃灼烧完全分解生成CuO和气体,产生气体的体积为L(标准状况).
题目详情
草酸铜(CuC2O4•2H2O)是制备纳米CuO的前驱体,可利用草酸和印刷线路板的酸性蚀刻废液为原料制取.
(1)7.6gCuC2O4在350℃灼烧完全分解生成CuO和气体,产生气体的
体积为___L(标准状况).
(2)已知pKa=-lgKa,25℃时,H2C2O4的pKa1=1.2,pKa2=4.19,
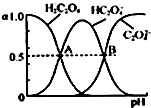
草酸溶液中含碳各物种的分布分数α(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系如右图所示.A点溶液的PH为___;0.1mol•L-1NaHC2O4与0.1mol•L-1Na2 C2O4溶液等体积混合,所得溶液中微粒浓度从大到小的顺序为___(填序号).
①c(H+)②c(HC2O4-)③c (H2C2O4)④c (C2O42-)
(3)某合作学习小组的同学按下列步骤检测原料中酸性蚀刻废液中铜的含量:
Ⅰ.取100.00mL澄清的“酸性蚀刻废液”,加H2O2,然后调节pH约为3,过滤除去Fe(OH)3.
Ⅱ.取Ⅰ的滤液加入NH4HF2排除微量的Fe3+干扰,然后将溶液稀释定容到250mL容量瓶中,得溶液A.
Ⅲ.取25.00mL溶液A于锥形瓶中,加入稍过量的KI溶液(2Cu2++5I-=2Cul↓+I3),用0.1000mol/LNa2S2O3溶液滴定(2S2O32-+I3-=S4O62-+3I-)到近终点时,加入淀粉继续滴定,再加入KSCN溶液[Cul(s)+SCN-(aq)⇌CuSCN(s)+I-(aq)],振荡后继续滴定至极点,共消耗Na2S2O3标准溶液20.00mL.
①若缺少步骤Ⅰ、Ⅱ会导致测定的铜的含量___(填“偏大”“偏小”或“不变”).
②已知Cul能吸附I2不能被滴定,CuSCN不吸附碘,向Cul悬浊液中加入KSCN溶液,达到平衡后溶液中c(SCN-)=___[用c(I-)、Ksp(Cul)和Ksp(CuSCN)].
③计算原“酸性蚀刻废液”中铜离子浓度(用每升蚀刻废液中含铜的质量表示,单位g•L-1)(请给出计算过程).

(1)7.6gCuC2O4在350℃灼烧完全分解生成CuO和气体,产生气体的
体积为___L(标准状况).
(2)已知pKa=-lgKa,25℃时,H2C2O4的pKa1=1.2,pKa2=4.19,
草酸溶液中含碳各物种的分布分数α(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系如右图所示.A点溶液的PH为___;0.1mol•L-1NaHC2O4与0.1mol•L-1Na2 C2O4溶液等体积混合,所得溶液中微粒浓度从大到小的顺序为___(填序号).
①c(H+)②c(HC2O4-)③c (H2C2O4)④c (C2O42-)
(3)某合作学习小组的同学按下列步骤检测原料中酸性蚀刻废液中铜的含量:
Ⅰ.取100.00mL澄清的“酸性蚀刻废液”,加H2O2,然后调节pH约为3,过滤除去Fe(OH)3.
Ⅱ.取Ⅰ的滤液加入NH4HF2排除微量的Fe3+干扰,然后将溶液稀释定容到250mL容量瓶中,得溶液A.
Ⅲ.取25.00mL溶液A于锥形瓶中,加入稍过量的KI溶液(2Cu2++5I-=2Cul↓+I3),用0.1000mol/LNa2S2O3溶液滴定(2S2O32-+I3-=S4O62-+3I-)到近终点时,加入淀粉继续滴定,再加入KSCN溶液[Cul(s)+SCN-(aq)⇌CuSCN(s)+I-(aq)],振荡后继续滴定至极点,共消耗Na2S2O3标准溶液20.00mL.
①若缺少步骤Ⅰ、Ⅱ会导致测定的铜的含量___(填“偏大”“偏小”或“不变”).
②已知Cul能吸附I2不能被滴定,CuSCN不吸附碘,向Cul悬浊液中加入KSCN溶液,达到平衡后溶液中c(SCN-)=___[用c(I-)、Ksp(Cul)和Ksp(CuSCN)].
③计算原“酸性蚀刻废液”中铜离子浓度(用每升蚀刻废液中含铜的质量表示,单位g•L-1)(请给出计算过程).
▼优质解答
答案和解析
(1)CuC2O4在350℃灼烧完全分解方程式为CuC2O4
CuO+CO+CO2↑,n(CuC2O4)=
=005mol,则气体的总物质的量为0.1mol,所以其体积为2.24L;
故答案为:2.24;
(2)A点时Ka=
,由图象可知,c(HC2O4-)=c(H2C2O4),则c(H+)=Ka1,所以pH=pKa1=1.2;0.1mol•L-1NaHC2O4与0.1mol•L-1Na2 C2O4溶液等体积混合,HC2O4-的电离程度大于C2O42-的水解程度,溶液显酸性,则c (C2O42-)>c(HC2O4-),由于电离和水解程度均较小,所以c(HC2O4-)>c(H+),所以溶液中离子浓度关系:c (C2O42-)>c(HC2O4-)>c(H+)>c(H2C2O4),即液中微粒浓度从大到小的顺序为④②①③;
故答案为:1.2;④②①③;
(3)①若缺少步骤Ⅰ、Ⅱ,溶液中存在Fe3+,则Fe3+能消耗碘离子,使测定的Cu2+的物质的量偏大,导致测定的铜的含量偏大;
故答案为:偏大;
②混合溶液中
=
,则c(SCN-)=
•c(I-);
故答案为:
•c(I-);
③已知:2Cu2++5I-=2Cul↓+I3,2S2O32-+I3-=S4O62-+3I-,则n(Cu2+)=n(S2O32-)=0.1mol/L×0.02L=0.002mol,所以m(Cu)=0.128g,
则原“酸性蚀刻废液”中铜离子浓度=
=12.8g/L;
答:原“酸性蚀刻废液”中铜离子浓度为12.8g/L.
| ||
| 7.6g |
| 152g/mol |
故答案为:2.24;
(2)A点时Ka=
| c(HC2O4-)×c(H+) |
| c(H2C2O4) |
故答案为:1.2;④②①③;
(3)①若缺少步骤Ⅰ、Ⅱ,溶液中存在Fe3+,则Fe3+能消耗碘离子,使测定的Cu2+的物质的量偏大,导致测定的铜的含量偏大;
故答案为:偏大;
②混合溶液中
| c(SCN-) |
| c(I-) |
| Ks(CuSCN) |
| Ks(CuI) |
| Ksp(CuSCN) |
| Ksp(CuI) |
故答案为:
| Ksp(CuSCN) |
| Ksp(CuI) |
③已知:2Cu2++5I-=2Cul↓+I3,2S2O32-+I3-=S4O62-+3I-,则n(Cu2+)=n(S2O32-)=0.1mol/L×0.02L=0.002mol,所以m(Cu)=0.128g,
则原“酸性蚀刻废液”中铜离子浓度=
0.128g×
| ||
| 0.1L |
答:原“酸性蚀刻废液”中铜离子浓度为12.8g/L.
看了草酸铜(CuC2O4•2H2O...的网友还看了以下:
下列说法正确的是()A.硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物B.蔗糖、硝酸钾和硫酸 2020-05-12 …
在氯酸钾里加入少量高锰酸钾,加热制取氧气的速率大大加快,主要原因是:A高锰酸钾是氯化钠分解的催化剂 2020-05-13 …
(2014•鹤壁二模)下列实验方案可行的是()A.用水区分硝酸铵和生石灰B.用石蕊溶液区分稀硫酸和 2020-05-14 …
下列实验方案可行的是A.用水区分硝酸铵和生石灰B.用石蕊溶液区分稀硫酸和稀盐酸C.用酚酞试液区分纯 2020-05-14 …
ABCDEF分别代表:碳酸钠溶液硫酸锌氯化钡稀硫酸铁硝酸铜用线连接可以发生反应.则C、E分别代表B 2020-05-20 …
丙稀酸和2-丁稀酸的编号问题丙稀酸:C=C-COOH2-丁稀酸:C-C=C-COOH为什么丁稀酸的 2020-06-03 …
关于ATP的一个问题关于ADP变成ATP时消耗的能量和ATP变成ADP时释放的能量,叙述正确的是: 2020-07-26 …
分枝酸可用于生化研究,其结构简式如图.下列关于分枝酸的叙述正确的是()A.分枝酸的分子式为C10H8 2020-10-31 …
一.碳55氢70氧19氮10这个化学式是脱水缩合前用氨基酸的通式数的还是脱水缩合后?二.某蛋白质的分 2020-11-07 …
目前用于治疗甲型H1N1流感的特效药物达菲,是以我国特有的中药材八角的提取物--莽草酸为原料合成的. 2020-12-22 …