早教吧作业答案频道 -->化学-->
铬是一种银白色金属,化学性质稳定,以+2、+3和+6价为常见价态.工业上以铬铁矿(主要成分为FeO•Cr2O3,含有Al2O3、SiO2等杂质)为主要原料生产金属铬和重铬酸钠Na2Cr2O7•2H2O(已知Na2Cr2O7是
题目详情
铬是一种银白色金属,化学性质稳定,以+2、+3和+6价为常见价态.工业上以铬铁矿(主要成分为FeO•Cr2O3,含有Al2O3、SiO2等杂质)为主要原料生产金属铬和重铬酸钠Na2Cr2O7•2H2O(已知Na2Cr2O7是一种强氧化剂),其主要工艺流程如图1:
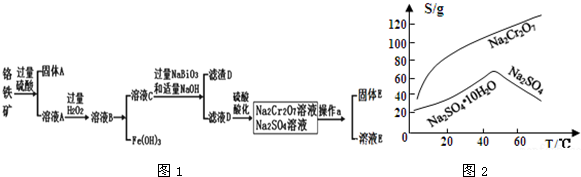
查阅资料得知:常温下,NaBiO3不溶于水,有强氧化性,在碱性条件下,能将Cr3+转化为CrO42-
回答下列问题:
(1)工业上常采用热还原法制备金属铬,写出以Cr2O3为原料,利用铝热反应制取金属铬的化学方程式___.
(2)酸化滤液D时,不选用盐酸的原因是___.
(3)固体E的主要成分是Na2SO4,根据图2分析操作a为___、___.
(4)已知含+6价铬的污水会污染环境,电镀厂产生的镀铜废水中往往含有一定量的Cr2O72-.电镀厂处理镀铜废水中的Cr2O72-,往往采用还原沉淀法,具体流程如下:
含Cr2O
的废水
含Cr3+的废水
Cr(OH)3沉淀
①Cr(OH)3的化学性质与Al(OH)3相似.在上述生产过程中加入NaOH溶液时要控制溶液的pH不能过高,是因为___(用方程式表示);
②下列溶液中可以代替上述流程中Na2S2O3溶液的是___(填选项序号);
A.FeSO4溶液 B.浓H2SO4 C.酸性KMnO4溶液 D.Na2SO3溶液
③上述流程中,每消耗0.1mol Na2S2O3转移0.8mol e-,则加入Na2S2O3溶液时发生反应的离子方程式为___.
(5)某厂废水中含1.00×10-3mol/L的Cr2O72-,某研究性学习小组为了变废为宝,将废水处理得到磁性材料Cr0.5Fe1.5FeO4 (Cr的化合价为+3,Fe的化合价依次为+3、+2).欲使1L该废水中的Cr2O72-完全转化为Cr0.5Fe1.5FeO4.理论上需要加入___g FeSO4•7H2O.(已知FeSO4•7H2O 摩尔质量为278g/mol)

查阅资料得知:常温下,NaBiO3不溶于水,有强氧化性,在碱性条件下,能将Cr3+转化为CrO42-
回答下列问题:
(1)工业上常采用热还原法制备金属铬,写出以Cr2O3为原料,利用铝热反应制取金属铬的化学方程式___.
(2)酸化滤液D时,不选用盐酸的原因是___.
(3)固体E的主要成分是Na2SO4,根据图2分析操作a为___、___.
(4)已知含+6价铬的污水会污染环境,电镀厂产生的镀铜废水中往往含有一定量的Cr2O72-.电镀厂处理镀铜废水中的Cr2O72-,往往采用还原沉淀法,具体流程如下:
含Cr2O
| 2- 7 |
| 调节pH至2-3 |
| |
| 加入Na2S2O3溶液 |
| 加入NaOH溶液 |
| |
| 控制PH |
①Cr(OH)3的化学性质与Al(OH)3相似.在上述生产过程中加入NaOH溶液时要控制溶液的pH不能过高,是因为___(用方程式表示);
②下列溶液中可以代替上述流程中Na2S2O3溶液的是___(填选项序号);
A.FeSO4溶液 B.浓H2SO4 C.酸性KMnO4溶液 D.Na2SO3溶液
③上述流程中,每消耗0.1mol Na2S2O3转移0.8mol e-,则加入Na2S2O3溶液时发生反应的离子方程式为___.
(5)某厂废水中含1.00×10-3mol/L的Cr2O72-,某研究性学习小组为了变废为宝,将废水处理得到磁性材料Cr0.5Fe1.5FeO4 (Cr的化合价为+3,Fe的化合价依次为+3、+2).欲使1L该废水中的Cr2O72-完全转化为Cr0.5Fe1.5FeO4.理论上需要加入___g FeSO4•7H2O.(已知FeSO4•7H2O 摩尔质量为278g/mol)
▼优质解答
答案和解析
(1)三氧化二铬与铝发生铝热反应的方程式为:Cr2O3+2Al 高温 . 2Cr+Al2O3,故答案为:Cr2O3+2Al 高温 . 2Cr+Al2O3 ;(2)盐酸中的氯是-1价具有还原性,会CrO42-被氧化成氯气,故答案为:盐酸中的Cl-会被氧化...
看了铬是一种银白色金属,化学性质稳...的网友还看了以下:
已知一种c(H+)=10-3mol/L的酸和一种c(OH-)=10-3mol/L的碱溶液等体积混合 2020-05-13 …
高中化学选择题常温下,分别将四块形状相同,质量均为7g的铁片同时放入下列四种溶液中,产生气体速率最 2020-05-16 …
科学家利用无土栽培培养名贵花卉,向培养液中添加多种必需化学元素,配方:钾离子1mol/l钠离子1m 2020-05-22 …
某小组以醋酸为例探究弱酸的性质.(1)实验一:探究酸的强弱对酸与镁条反应速率的影响.①设计实验方案 2020-06-20 …
请您跟我讲一下过量锌粉跟100ml4mol/L盐酸反应,在一定温度下,为加快反应速率但又不影响生成 2020-07-09 …
下列四种稀硫酸跟铁反应,其中最初反应速率最快的是()A.常温下,5ml,3mol/L的硫酸溶液B. 2020-07-14 …
甲酸(HCOOH)是一种一元弱酸,下列性质中可以证明它是弱电解质的是()A.常温下,1mol/L甲 2020-07-24 …
1.现有一个含L、K、E三种氨基酸的混合液,欲用阳离子交换树脂分离,用PH5.5的缓冲液洗脱,请问洗 2021-01-14 …
想请教下缓冲溶液的浓度与配制其的两种溶液的体积比有关系吗比如:用0.2mol/L的磷酸二氢钾87.7 2021-01-22 …
用18mol/L硫酸配制100ML1.0ml/L硫酸,则需要多少浓硫酸?若实验的仪器有:则实验时选用 2021-02-01 …