早教吧作业答案频道 -->化学-->
铬是一种银白色金属,化学性质稳定,以+2、+3和+6价为常见价态.工业上以铬铁矿(主要成分为FeO•Cr2O3,含有Al2O3、SiO2等杂质)为主要原料生产金属铬和重铬酸钠Na2Cr2O7•2H2O(已知Na2Cr2O7是
题目详情
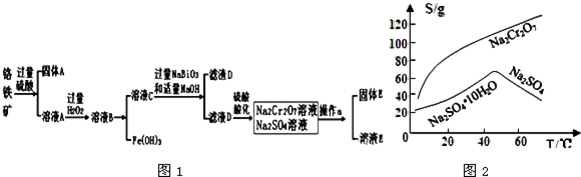
铬是一种银白色金属,化学性质稳定,以+2、+3和+6价为常见价态.工业上以铬铁矿(主要成分为FeO•Cr2O3,含有Al2O3、SiO2等杂质)为主要原料生产金属铬和重铬酸钠Na2Cr2O7•2H2O(已知Na2Cr2O7是一种强氧化剂),其主要工艺流程如图1:
查阅资料得知:常温下,NaBiO3不溶于水,有强氧化性,在碱性条件下,能将Cr3+转化为CrO42-
回答下列问题:
(1)工业上常采用热还原法制备金属铬,写出以Cr2O3为原料,利用铝热反应制取金属铬的化学方程式___.
(2)酸化滤液D时,不选用盐酸的原因是___.
(3)固体E的主要成分是Na2SO4,根据图2分析操作a为___、___.
(4)已知含+6价铬的污水会污染环境,电镀厂产生的镀铜废水中往往含有一定量的Cr2O72-.电镀厂处理镀铜废水中的Cr2O72-,往往采用还原沉淀法,具体流程如下:
含Cr2O72-的废水
含Cr3+的废水
Cr(OH)3沉淀
①Cr(OH)3的化学性质与Al(OH)3相似.在上述生产过程中加入NaOH溶液时要控制溶液的pH不能过高,是因为___(用方程式表示);
②下列溶液中可以代替上述流程中Na2S2O3溶液的是___(填选项序号);
A.FeSO4溶液 B.浓H2SO4 C.酸性KMnO4溶液 D.Na2SO3溶液
③上述流程中,每消耗0.1mol Na2S2O3转移0.8mol e-,则加入Na2S2O3溶液时发生反应的离子方程式为___.
(5)某厂废水中含1.00×10-3mol/L的Cr2O72-,某研究性学习小组为了变废为宝,将废水处理得到磁性材料Cr0.5Fe1.5FeO4 (Cr的化合价为+3,Fe的化合价依次为+3、+2).欲使1L该废水中的Cr2O72-完全转化为Cr0.5Fe1.5FeO4.理论上需要加入___g FeSO4•7H2O.(已知FeSO4•7H2O 摩尔质量为278g/mol)

查阅资料得知:常温下,NaBiO3不溶于水,有强氧化性,在碱性条件下,能将Cr3+转化为CrO42-
回答下列问题:
(1)工业上常采用热还原法制备金属铬,写出以Cr2O3为原料,利用铝热反应制取金属铬的化学方程式___.
(2)酸化滤液D时,不选用盐酸的原因是___.
(3)固体E的主要成分是Na2SO4,根据图2分析操作a为___、___.
(4)已知含+6价铬的污水会污染环境,电镀厂产生的镀铜废水中往往含有一定量的Cr2O72-.电镀厂处理镀铜废水中的Cr2O72-,往往采用还原沉淀法,具体流程如下:
含Cr2O72-的废水
| 调节pH至2-3 |
| |
| 加入Na2S2O3溶液 |
| 加入NaOH溶液 |
| |
| 控制pH |
①Cr(OH)3的化学性质与Al(OH)3相似.在上述生产过程中加入NaOH溶液时要控制溶液的pH不能过高,是因为___(用方程式表示);
②下列溶液中可以代替上述流程中Na2S2O3溶液的是___(填选项序号);
A.FeSO4溶液 B.浓H2SO4 C.酸性KMnO4溶液 D.Na2SO3溶液
③上述流程中,每消耗0.1mol Na2S2O3转移0.8mol e-,则加入Na2S2O3溶液时发生反应的离子方程式为___.
(5)某厂废水中含1.00×10-3mol/L的Cr2O72-,某研究性学习小组为了变废为宝,将废水处理得到磁性材料Cr0.5Fe1.5FeO4 (Cr的化合价为+3,Fe的化合价依次为+3、+2).欲使1L该废水中的Cr2O72-完全转化为Cr0.5Fe1.5FeO4.理论上需要加入___g FeSO4•7H2O.(已知FeSO4•7H2O 摩尔质量为278g/mol)
▼优质解答
答案和解析
(1)三氧化二铬与铝发生铝热反应的方程式为:Cr2O3+2Al
2Cr+Al2O3,
故答案为:Cr2O3+2Al
2Cr+Al2O3;
(2)盐酸中的氯是-1价具有还原性,会CrO42-被氧化成氯气,
故答案为:盐酸中的Cl-会被氧化,产生Cl2;
(3)由图2可知Na2Cr2O7的溶解度随温度的升高而增大,而硫酸钠的温度随温度的升高而降低,所以采用蒸发结晶、趁热过滤的方法分离硫酸钠,
故答案为:蒸发结晶、趁热过滤;
(4)①Cr(OH)3的化学性质与Al(OH)3相似,如果氢氧化钠过量Cr(OH)3会溶解,
故答案为:pH过高Cr(OH)3会与过量的NaOH 反应;
②可以代替上述流程中Na2S2O3溶液,需要具有还原性,能还原重铬酸根离子;
A.FeSO4溶液中亚铁离子具有还原性,可以还原Cr2O72-离子,但又引入新的杂质离子铁离子,故A不符合;
B.浓H2SO4 具有强氧化性,不能表现还原性,不能还原Cr2O72-,故B不符合;
C.酸性KMnO4 是强氧化剂不能还原Cr2O72-,故C不符合;
D.Na2SO3溶液中亚硫酸根离子具有还原性,可以还原Cr2O72-,故D符合;
故答案为:D;
③每消耗0.1mol Na2S2O3转移0.8mol e-,Na2S2O3~2SO42-~8e-,Cr2O72-~2Cr3+~6e-,依据氧化还原反应电子守恒配平书写,3Na2S2O3~6SO42-~24e-,4Cr2O72-~8Cr3+~24e-,得到的氧化还原反应的离子方程式为3S2O32-+4Cr2O72-+26H+═6SO42-+8Cr3++13H2O;
故答案为:3S2O32-+4Cr2O72-+26H+═6SO42-+8Cr3++13H2O;
(5)1L废水中含n(Cr2O72-)=1.00×10-3 mol,根据Cr原子、Fe原子守恒,可得:
Cr2O72-~~~4Cr0.5Fe1.5FeO4~~~10FeSO4•7H2O,
所以理论上n(FeSO4•7H2O)=10n(Cr2O72-)=1.00×10-3 mol×10=0.01mol,
所以m(FeSO4•7H2O)=0.01mol×278 g/mol=2.78g,
故答案为:2.78.
| ||
故答案为:Cr2O3+2Al
| ||
(2)盐酸中的氯是-1价具有还原性,会CrO42-被氧化成氯气,
故答案为:盐酸中的Cl-会被氧化,产生Cl2;
(3)由图2可知Na2Cr2O7的溶解度随温度的升高而增大,而硫酸钠的温度随温度的升高而降低,所以采用蒸发结晶、趁热过滤的方法分离硫酸钠,
故答案为:蒸发结晶、趁热过滤;
(4)①Cr(OH)3的化学性质与Al(OH)3相似,如果氢氧化钠过量Cr(OH)3会溶解,
故答案为:pH过高Cr(OH)3会与过量的NaOH 反应;
②可以代替上述流程中Na2S2O3溶液,需要具有还原性,能还原重铬酸根离子;
A.FeSO4溶液中亚铁离子具有还原性,可以还原Cr2O72-离子,但又引入新的杂质离子铁离子,故A不符合;
B.浓H2SO4 具有强氧化性,不能表现还原性,不能还原Cr2O72-,故B不符合;
C.酸性KMnO4 是强氧化剂不能还原Cr2O72-,故C不符合;
D.Na2SO3溶液中亚硫酸根离子具有还原性,可以还原Cr2O72-,故D符合;
故答案为:D;
③每消耗0.1mol Na2S2O3转移0.8mol e-,Na2S2O3~2SO42-~8e-,Cr2O72-~2Cr3+~6e-,依据氧化还原反应电子守恒配平书写,3Na2S2O3~6SO42-~24e-,4Cr2O72-~8Cr3+~24e-,得到的氧化还原反应的离子方程式为3S2O32-+4Cr2O72-+26H+═6SO42-+8Cr3++13H2O;
故答案为:3S2O32-+4Cr2O72-+26H+═6SO42-+8Cr3++13H2O;
(5)1L废水中含n(Cr2O72-)=1.00×10-3 mol,根据Cr原子、Fe原子守恒,可得:
Cr2O72-~~~4Cr0.5Fe1.5FeO4~~~10FeSO4•7H2O,
所以理论上n(FeSO4•7H2O)=10n(Cr2O72-)=1.00×10-3 mol×10=0.01mol,
所以m(FeSO4•7H2O)=0.01mol×278 g/mol=2.78g,
故答案为:2.78.
看了铬是一种银白色金属,化学性质稳...的网友还看了以下:
双缩脲试剂可以鉴定蛋白质,是因为A 蛋白质都有肽键B 蛋白质都含有氨基酸C 蛋白质都有羧基D 蛋白 2020-04-06 …
下列有关图中某蛋白质的叙述,不正确的是()A.该蛋白质含有两条肽链B.该蛋白质共有128个肽键C. 2020-05-13 …
1.20种氨基酸的平均分子质量是128,现有一蛋白质分子,由三条多肽链组成,共有肽键97个,则次蛋 2020-05-14 …
镁条在空气中点燃,反应结束后生成物全部收回称量,为什么所称得的质量比反应前质量增加了?但是根据质量 2020-05-20 …
以下有关蛋白质功能的描述,错误的是:[]A.有些蛋白质具有催化作用B.有些蛋白质可以作为载体C.有 2020-07-01 …
淀粉、核酸、脂肪、蛋白质共有的化学元素是()A.C、H、OB.C、H、O、NC.C、H、O、N、S 2020-07-03 …
下列与蛋白质有关的叙述正确的是A.有的蛋白质具有催化功能,如蛋白酶能催化氨基酸合成蛋白质B.蛋白质 2020-07-12 …
这是同位素吗O=C=O(1个O质量数为161个O质量数为18)O=O=O(1个O质量数为161个O 2020-07-18 …
如图甲所示,一根水平张紧弹性长绳上有等间距的A′、B′、O、B、A质点,相邻两质点间距离为lm,t 2020-07-31 …
有关人体内蛋白质的功能,下列叙述不正确的是()A.有些蛋白质具有信息传递的作用B.有些蛋白质具有运输 2020-12-09 …