早教吧作业答案频道 -->化学-->
二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的消毒剂,是一种黄绿色的气体,其熔点为-59℃,沸点为11.0℃,易溶于水.工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得.
题目详情
二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的消毒剂,是一种黄绿色的气体,其熔点为-59℃,沸点为11.0℃,易溶于水.工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得.某学生拟用图1所示装置模拟工业制取并收集ClO2.
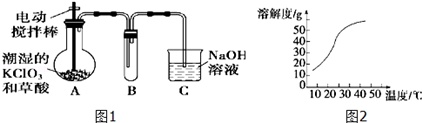
(1)A装置必须添加温度控制装置,除酒精灯外,还需要的玻璃仪器有烧杯、___.
(2)B装置必须放在冰水浴中,其原因是___.
(3)反应后在装置C中可得NaClO2溶液.已知:NaClO2饱和溶液在温度低于38℃时析出晶体是NaClO2•3H2O,高于38℃时析出晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl.NaClO2的溶解度曲线如图2,获得NaClO2晶体的操作步骤为:
①减压,55℃蒸发结晶;②趁热过滤;③___;④在55℃干燥,得到成品.
(4)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液.为测定所得溶液中
ClO2的浓度,进行了下列实验:
步骤1:准确量取ClO2溶液10.00mL,稀释成100.00mL试样,量取V1 mL试样加入到锥形瓶中;
步骤2:用稀硫酸调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;
步骤3:加入指示剂,用c mol•L-1Na2S2O3溶液滴定至终点.重复2次,测得消耗
Na2S2O3溶液平均值为V2mL(已知 2Na2S2O3+I2═Na2S4O6+2NaI ).
①配制100mL c mol•L-1Na2S2O3标准溶液时,用的玻璃仪器除烧杯、量筒、玻璃
棒外还有:___.
②若步骤2所得溶液放置时间太长,则测定结果___(填“偏高”、“偏低”或“不变”)
③原ClO2溶液的浓度为___ g•L-1(用含字母的代数式表示).

(1)A装置必须添加温度控制装置,除酒精灯外,还需要的玻璃仪器有烧杯、___.
(2)B装置必须放在冰水浴中,其原因是___.
(3)反应后在装置C中可得NaClO2溶液.已知:NaClO2饱和溶液在温度低于38℃时析出晶体是NaClO2•3H2O,高于38℃时析出晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl.NaClO2的溶解度曲线如图2,获得NaClO2晶体的操作步骤为:
①减压,55℃蒸发结晶;②趁热过滤;③___;④在55℃干燥,得到成品.
(4)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液.为测定所得溶液中
ClO2的浓度,进行了下列实验:
步骤1:准确量取ClO2溶液10.00mL,稀释成100.00mL试样,量取V1 mL试样加入到锥形瓶中;
步骤2:用稀硫酸调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;
步骤3:加入指示剂,用c mol•L-1Na2S2O3溶液滴定至终点.重复2次,测得消耗
Na2S2O3溶液平均值为V2mL(已知 2Na2S2O3+I2═Na2S4O6+2NaI ).
①配制100mL c mol•L-1Na2S2O3标准溶液时,用的玻璃仪器除烧杯、量筒、玻璃
棒外还有:___.
②若步骤2所得溶液放置时间太长,则测定结果___(填“偏高”、“偏低”或“不变”)
③原ClO2溶液的浓度为___ g•L-1(用含字母的代数式表示).
▼优质解答
答案和解析
(1)氯酸钾和草酸反应生成碳酸钾、二氧化碳、二氧化氯和水,反应方程式为:2KClO3+H2C2O4
K2CO3+CO2↑+2ClO2↑+H2O,制取温度是60℃,A需要温度控制,需要温度计,
故答案为:温度计;
(2)二氧化氯的熔点较低,为收集二氧化氯,应在较低温度下进行,所以应该采用冰水浴,
故答案为:使ClO2充分冷凝,减少挥发;
(3)从溶液中获得溶质,一般采用蒸发结晶、过滤、洗涤、干燥的方法,为防止析出晶体NaClO2•3H2O,应趁热过滤,NaClO2饱和溶液在温度低于38℃时析出晶体是NaClO2•3H2O,高于38℃时析出晶体是NaClO2,所以用38~60℃热水洗涤,在55℃干燥,得到成品,
故答案为:用38~60℃热水洗涤;
(4)①配制100mL溶液用到的仪器有托盘天平、药匙、玻璃棒、胶头滴管、烧杯、100mL容量瓶、量筒(可用可不用),故还需要的玻璃仪器有:100mL容量瓶、胶头滴管,
故答案为:100ml容量瓶、胶头滴管;
②ClO2很不稳定,步骤2所得溶液放置时间太长,ClO2分解相当于与碘反应,导致测定结果偏高,
故答案为:偏高;
③二氧化氯具有氧化性,在酸性环境下,能将碘离子氧化,反应的原理方程式为:2ClO2+10I-+8H+=2Cl-+5I2+4H2O,设原ClO2溶液的浓度为x,
2ClO2 ~5I2 ~10Na2S2O3
2mol 10mol
1×10-3cV2mol
x=
g/L=
g/L,
故答案为:
.
| ||
故答案为:温度计;
(2)二氧化氯的熔点较低,为收集二氧化氯,应在较低温度下进行,所以应该采用冰水浴,
故答案为:使ClO2充分冷凝,减少挥发;
(3)从溶液中获得溶质,一般采用蒸发结晶、过滤、洗涤、干燥的方法,为防止析出晶体NaClO2•3H2O,应趁热过滤,NaClO2饱和溶液在温度低于38℃时析出晶体是NaClO2•3H2O,高于38℃时析出晶体是NaClO2,所以用38~60℃热水洗涤,在55℃干燥,得到成品,
故答案为:用38~60℃热水洗涤;
(4)①配制100mL溶液用到的仪器有托盘天平、药匙、玻璃棒、胶头滴管、烧杯、100mL容量瓶、量筒(可用可不用),故还需要的玻璃仪器有:100mL容量瓶、胶头滴管,
故答案为:100ml容量瓶、胶头滴管;
②ClO2很不稳定,步骤2所得溶液放置时间太长,ClO2分解相当于与碘反应,导致测定结果偏高,
故答案为:偏高;
③二氧化氯具有氧化性,在酸性环境下,能将碘离子氧化,反应的原理方程式为:2ClO2+10I-+8H+=2Cl-+5I2+4H2O,设原ClO2溶液的浓度为x,
2ClO2 ~5I2 ~10Na2S2O3
2mol 10mol
| 10 -2x×V1×10 -3 |
| 10 -1 |
x=
| 2cV 2 |
| V 1 |
| 135cV 2 |
| V 1 |
故答案为:
| 135cV 2 |
| V 1 |
看了二氧化氯(ClO2)是目前国际...的网友还看了以下:
为什么co2释放总量最少的位置不是无氧呼吸消失点无氧呼吸不是1摩尔葡萄糖产生2摩尔CO2吗,有氧呼 2020-05-14 …
酵母菌在有氧的条件下进行需氧呼吸,在无氧条件下能进行厌氧呼吸产生酒精.如果如果在有氧呼吸和无氧呼吸 2020-05-14 …
生物必修1的一道试题人体红细胞无线粒体,它所需能量的来源主要是利用()A葡萄糖,进行有氧呼吸 B葡 2020-05-16 …
蜡烛燃烧前后,消耗的氧气与生成的二氧化碳分子数是否相同?好像蜡烛中无氧元素!那照二楼的说是不同了? 2020-05-16 …
原题:马铃薯块茎中的无氧呼吸,与苹果中的无氧呼吸的主要区别是什么?---答案:前者的无氧呼吸产物是乳 2020-10-29 …
问一道高中生物问题原题:马铃薯块茎中的无氧呼吸,与苹果中的无氧呼吸的主要区别是什么?---答案:前者 2020-10-29 …
有关呼吸作用的问题判断下面语句,1.所有生物都可进行无氧呼吸.2.可以进行有氧呼吸的生物必将可进行无 2020-11-03 …
在制果酒、果醋、泡菜时,发酵过程中对氧气的需求情况分别是()A.无氧、有氧、无氧B.有氧、无氧、无氧 2020-12-14 …
在制果酒、果醋、泡菜、腐乳时,发酵过程中对氧气的需求分别是()A.无氧、有氧、无氧、有氧B.有氧、无 2020-12-14 …
在制果酒、果醋、泡菜、腐乳时,发酵过程中对氧气的需求分别是()A、无氧、有氧、无氧、有氧B、有氧、无 2020-12-14 …