早教吧作业答案频道 -->化学-->
氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:依照如图,完成下列填空:(1)写出通电条件下电解饱和食盐水的化学方程式(2)为有效除去粗盐中的Ca2+、Mg2+、SO
题目详情
氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
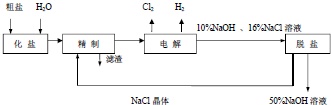
依照如图,完成下列填空:
(1)写出通电条件下电解饱和食盐水的化学方程式___
(2)为有效除去粗盐中的Ca2+、Mg2+、SO
杂质,精制过程中加入试剂的合理顺序为___
A.NaOH溶液,Na2CO3溶液,钡试剂,盐酸
B、NaOH溶液,钡试剂,Na2CO3溶液、盐酸
C.钡试剂,NaOH溶液,Na2CO3溶液、盐酸
(3)钡试剂可以是___
A.Ba(OH)2
B.Ba(NO3)2
C.BaCl2
(4)为了保证杂质能够完全除去,除去试剂均稍过量,判断钡试剂已经过量的方法是___
(5)请写出精制过程中加入适量盐酸时发生反应的离子方程式___
(6)下表是NaOH、NaCl在不同温度下的溶解度(单位:g/100g水)
由此可知:
脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过___,冷却、___(填写操作名称),除去NaCl2该工业流程中循环中可循环利用的物质是___.

依照如图,完成下列填空:
(1)写出通电条件下电解饱和食盐水的化学方程式___
(2)为有效除去粗盐中的Ca2+、Mg2+、SO
| 2- 4 |
A.NaOH溶液,Na2CO3溶液,钡试剂,盐酸
B、NaOH溶液,钡试剂,Na2CO3溶液、盐酸
C.钡试剂,NaOH溶液,Na2CO3溶液、盐酸
(3)钡试剂可以是___
A.Ba(OH)2
B.Ba(NO3)2
C.BaCl2
(4)为了保证杂质能够完全除去,除去试剂均稍过量,判断钡试剂已经过量的方法是___
(5)请写出精制过程中加入适量盐酸时发生反应的离子方程式___
(6)下表是NaOH、NaCl在不同温度下的溶解度(单位:g/100g水)
| 温度(℃) | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 70℃ | 80℃ | 90℃ | 100℃ |
| NaOH | 42 | 51 | 109 | 119 | 129 | 145 | 174 | 299 | 314 | 329 | 347 |
| NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过___,冷却、___(填写操作名称),除去NaCl2该工业流程中循环中可循环利用的物质是___.
▼优质解答
答案和解析
(1)电解氯化钠溶液总反应的化学方程式为:2NaCl+2H2O  2NaOH+H2↑+Cl2↑;故答案为:2NaCl+2H2O
2NaOH+H2↑+Cl2↑;故答案为:2NaCl+2H2O  2NaOH+H2↑+Cl2↑;
2NaOH+H2↑+Cl2↑;
(2)SO42-、Ca2+、Mg2+等分别与BaCl2溶液、Na2CO3溶液、NaOH溶液反应生成沉淀,可再通过过滤除去,Na2CO3溶液能除去过量的BaCl2溶液,盐酸能除去过量的Na2CO3溶液和NaOH溶液,所以应BaCl2溶液再Na2CO3溶液之前加即可,所以加入试剂顺序为bc,故答案为:BC;
(3)添加钡试剂除去SO42-,注意不能引入新的杂质,选Ba(NO3)2会引入杂质硝酸根离子,所以该钡试剂不能选用,
故答案为:AC;
(4)判断钡试剂已经过量的方法是静置,向上层清液中继续滴加氯化钡溶液,如无沉淀产生,证明钡试剂已过量,故答案为:静置,向上层清液中继续滴加氯化钡溶液,如无沉淀产生,证明钡试剂已过量;
(5)加入适量盐酸除去溶液中的碳酸根和氢氧根离子,离子方程式为:H++OH-=H2O;CO32-+2H+═CO2↑+H2O,故答案为:H++OH-=H2O;CO32-+2H+═CO2↑+H2O;
(6)根据表中数据可以得出:氢氧化钠的溶解度随温度的升高而增大,但是氯化钠的溶解度受温度的影响不大,则在温度高的时候,生成氢氧化钠晶体即可除去氯化钠,所以氢氧化钠和氯化钠分离的方法是:蒸发结晶,过滤,可循环利用的物质是NaCl;故答案为:蒸发结晶,过滤;NaCl.
 2NaOH+H2↑+Cl2↑;故答案为:2NaCl+2H2O
2NaOH+H2↑+Cl2↑;故答案为:2NaCl+2H2O  2NaOH+H2↑+Cl2↑;
2NaOH+H2↑+Cl2↑;(2)SO42-、Ca2+、Mg2+等分别与BaCl2溶液、Na2CO3溶液、NaOH溶液反应生成沉淀,可再通过过滤除去,Na2CO3溶液能除去过量的BaCl2溶液,盐酸能除去过量的Na2CO3溶液和NaOH溶液,所以应BaCl2溶液再Na2CO3溶液之前加即可,所以加入试剂顺序为bc,故答案为:BC;
(3)添加钡试剂除去SO42-,注意不能引入新的杂质,选Ba(NO3)2会引入杂质硝酸根离子,所以该钡试剂不能选用,
故答案为:AC;
(4)判断钡试剂已经过量的方法是静置,向上层清液中继续滴加氯化钡溶液,如无沉淀产生,证明钡试剂已过量,故答案为:静置,向上层清液中继续滴加氯化钡溶液,如无沉淀产生,证明钡试剂已过量;
(5)加入适量盐酸除去溶液中的碳酸根和氢氧根离子,离子方程式为:H++OH-=H2O;CO32-+2H+═CO2↑+H2O,故答案为:H++OH-=H2O;CO32-+2H+═CO2↑+H2O;
(6)根据表中数据可以得出:氢氧化钠的溶解度随温度的升高而增大,但是氯化钠的溶解度受温度的影响不大,则在温度高的时候,生成氢氧化钠晶体即可除去氯化钠,所以氢氧化钠和氯化钠分离的方法是:蒸发结晶,过滤,可循环利用的物质是NaCl;故答案为:蒸发结晶,过滤;NaCl.
看了 氯碱厂电解饱和食盐水制取Na...的网友还看了以下:
如图是俄罗斯工业分布图,读图后回答下列问题:(1)A工业区内最大的工业中心是,这个工业区内的、、、 2020-05-01 …
如图为“我国主要工业中心和工业基地分布图”,读图回答.(1)图中阴影部分分别为我国四大工业基地:辽 2020-05-02 …
读我国某重工业基地分布示意图,回答下列问题。1.该工业基地的名称是。其工业中心是和。2.图中城市① 2020-05-14 …
如图是俄罗斯工业分布图,读图回答下列问题.(1)俄罗斯的工业主要分布在洲部分,其中A、B两工业区的 2020-05-14 …
如图所示是印度矿产资源、棉花、黄麻和工业的分布图,读图完成第12题.印度的传统工业大多靠近原料产地 2020-05-14 …
读图1和图2,回答问题.(1)图1反映了我国工业分布的基本格局:东部沿海地区工业中心(密集/稀疏) 2020-06-15 …
2012年11月以来三一重工和中联重科的口水战一直在升级,闹的沸沸扬扬。今年元月份三一重工联合中信 2020-07-15 …
2012年11月以来三一重工和中联重科的口水战一直在升级,闹的沸沸扬扬。今年元月份三一重工联合中信 2020-07-15 …
仔细观察如图的“孟买年内各月气温和降水量”图和“南亚一月、七月风向”图,完成第4-6题孟买是印度最 2020-07-16 …
如图(1)是一种画平行线的工具,在画平行线之前,工人师傅往往要先调整一下工具,如图2,然后画平行线 2020-08-01 …