早教吧作业答案频道 -->化学-->
NaCl是一种基础化工原料,通过电解饱和食盐水可以制得NaOH、H2、Cl2.完成下列填空:(1)写出电解饱和食盐水的化学方程式.(2)氯原子的最外层电子排布式为,氯离子核外有种运
题目详情
NaCl是一种基础化工原料,通过电解饱和食盐水可以制得NaOH、H2、Cl2.完成下列填空:
(1)写出电解饱和食盐水的化学方程式___.
(2)氯原子的最外层电子排布式为___,氯离子核外有___种运动状态不同的电子.
(3)氯气压缩成为液氯属于___变化(选填“物理”“化学”).常用浓氨水来检查输氯管道是否泄漏,泄漏处会观察到大量的白烟(NH4Cl),还生成一种无色无味的单质气体,写出此反应的化学方程式并标出电子转移的方向和数目___.
(4)氯气可用来标定碘水中碘单质的含量:5Cl2+I2+6H2O→10HCl+2HIO3.测定时可用气体流量计准确控制氯气的体积,以淀粉做指示剂来指示反应终点,反应终点时的现象是___.
用氯气标定一定体积碘水中碘单质的浓度,进行三次平行实验,数据记录见表:
则上述碘水中碘单质的浓度为___mol/L,假定碘水的实际浓度为1.02×10-3 mol/L,则实验的相对误差为___(保留两位小数).
(1)写出电解饱和食盐水的化学方程式___.
(2)氯原子的最外层电子排布式为___,氯离子核外有___种运动状态不同的电子.
(3)氯气压缩成为液氯属于___变化(选填“物理”“化学”).常用浓氨水来检查输氯管道是否泄漏,泄漏处会观察到大量的白烟(NH4Cl),还生成一种无色无味的单质气体,写出此反应的化学方程式并标出电子转移的方向和数目___.
(4)氯气可用来标定碘水中碘单质的含量:5Cl2+I2+6H2O→10HCl+2HIO3.测定时可用气体流量计准确控制氯气的体积,以淀粉做指示剂来指示反应终点,反应终点时的现象是___.
用氯气标定一定体积碘水中碘单质的浓度,进行三次平行实验,数据记录见表:
| 碘水的体积(mL) | 标况下氯气的体积(mL) |
| 500 | 56 |
| 500 | 55 |
| 500 | 57 |
▼优质解答
答案和解析
(1)电解饱和食盐水生成氢氧化纳、氢气和氯气,方程式为:2NaCl+2H2O
2NaOH+H2↑+Cl2↑,故答案为:2NaCl+2H2O
2NaOH+H2↑+Cl2↑;
(2)氯原子核外电子数为17,基态原子核外电子排布为1S12S22P63S23P5,故最外层电子排布式为3S23P5;核外每一个电子的运动状态都不同,故氯离子核外有18种运动状态不同的电子,
故答案为:3S23P5;18;
(3)因为气态压缩成为液态属于物理变化,所以氯气压缩成为液氯属于物理变化;氯气与氨气反应生成NH4Cl和氮气,化学反应方程式为:3Cl2+8NH3=6NH4Cl+N2,Cl元素化合价由0→-1价,N元素化合价由-3价→0价,转移电子数为6e-,用双线桥标出电子转移的方向和数目可为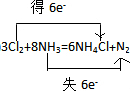 ,
,
故答案为:物理; ;
;
(4)碘溶液中有淀粉,所以溶液呈蓝色,所以用氯气标定碘水中碘单质的含量,判断达到滴定终点的现象是溶液由蓝色逐渐变为无色,且在半分钟内不变色,
取第一、二次和第三次的平均值,消耗标况下氯气的体积56mL,根据5Cl2+I2+6H2O→10HCl+2HIO3,则:
5Cl2~I2
5 1
mol xmol
所以x=
=5×10-4mol;
故碘水中碘单质的浓度为
=1×10-3 mol/L,假定碘水的实际浓度为1.02×10-3 mol/L,则实验的相对误差为
×100%=-1.96%;
故答案为:溶液由蓝色逐渐变为无色,且在半分钟内不变色;1×10-3;-1.96%.
| ||
| ||
(2)氯原子核外电子数为17,基态原子核外电子排布为1S12S22P63S23P5,故最外层电子排布式为3S23P5;核外每一个电子的运动状态都不同,故氯离子核外有18种运动状态不同的电子,
故答案为:3S23P5;18;
(3)因为气态压缩成为液态属于物理变化,所以氯气压缩成为液氯属于物理变化;氯气与氨气反应生成NH4Cl和氮气,化学反应方程式为:3Cl2+8NH3=6NH4Cl+N2,Cl元素化合价由0→-1价,N元素化合价由-3价→0价,转移电子数为6e-,用双线桥标出电子转移的方向和数目可为
 ,
,故答案为:物理;
 ;
;(4)碘溶液中有淀粉,所以溶液呈蓝色,所以用氯气标定碘水中碘单质的含量,判断达到滴定终点的现象是溶液由蓝色逐渐变为无色,且在半分钟内不变色,
取第一、二次和第三次的平均值,消耗标况下氯气的体积56mL,根据5Cl2+I2+6H2O→10HCl+2HIO3,则:
5Cl2~I2
5 1
| 56×10 -3 |
| 22.4 |
所以x=
| 2.5×10 -3mol |
| 5 |
故碘水中碘单质的浓度为
| 5×10 -4mol |
| 0.5L |
| 1.0×10 -3-1.02×10 -3 |
| 1.02×10 -3 |
故答案为:溶液由蓝色逐渐变为无色,且在半分钟内不变色;1×10-3;-1.96%.
看了 NaCl是一种基础化工原料,...的网友还看了以下:
由海水蒸发制得的食盐中,常含有Na2SO4、CaCl2、MgCl2等杂质,这些杂质对后续生产有害需 2020-05-13 …
食盐是生产生活中常见的物质,有广泛的用途(1)海水中含有较多的氯化钠,用海水晒盐可以获得食盐,请说 2020-05-16 …
初一下册科学题.求大神观摩指教~(1)现用20g的食盐溶解在一定质量的水里,配制成150g食盐水溶 2020-05-17 …
急``明天上学用`1海水含有较多的氯化钠,用海水晒盐可以获得食盐,请说明其中的道理.2海水晒盐制得 2020-06-17 …
下列加点字注音有两处错误的一项是()A.搓捻(cuōniàn)恍然(huǎng)迁徙(xǐ)钥匙( 2020-06-29 …
下列关于海水晒盐的叙述中,正确的是A为了得到食盐晶体,所以必须把海水晒干.B海水晒到1.21~1. 2020-07-12 …
蒸发海水可得到食盐,蒸发海水可得到食盐,食盐是一种重要的生活、生产必需品.下列说法正确的是[]A. 2020-07-12 …
小学问题求助1.甲,乙两个仓库各有粮食若干,从甲运出1/3到乙后,又从乙运出2/5到甲,这时乙得粮 2020-08-01 …
下列关于海水晒盐原理的分析,正确的是()A.利用阳光照射使海水升温得到食盐B.利用机械动力搅拌得到食 2020-11-11 …
如何通过食盐水得到食盐晶体如题需要用到搅拌这个操作吗什么情况下不需要搅拌啊08年的镇江中考题中通过食 2020-11-12 …