(1)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。目前已开发出用电解法制取ClO2的新工艺。①图中用石墨做电极,在
(1) 二氧化氯 (ClO 2 ) 为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。目前已开发出用电解法制取 ClO 2 的新工艺。
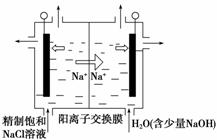
① 图中用石墨做电极,在一定条件下电解饱和食盐水制取 ClO 2 。则阳极产生 ClO 2 的电极反应式为 _____________________________________________________________
________________________________________________________________________ 。
② 电解一段时间,当阴极产生的气体体积为 112 mL( 标准状况 ) 时,停止电解。通过阳离子交换膜的阳离子的物质的量为 ________ mol ;用平衡移动原理解释阴极区 pH 增大的原因: _____________________________________________________________________
________________________________________________________________________ 。
(2) 为提高甲醇燃料的利用率,科学家发明了一种燃料电池,电池的一个电极通入空气,另一个电极通入甲醇气体,电解质是掺入了 Y 2 O 3 的 ZrO 2 晶体,在高温下它能传导 O 2 - 。电池工作时正极反应式为 _________________________________________________
________________________________________________________________________ 。
若以该电池为电源,用石墨作电极电解 100 mL 含有如下离子的溶液。
| 离子 | Cu 2 + | H + | Cl - | SO |
| c /mol·L - 1 | 1 | 4 | 4 | 1 |
电解一段时间后,当两极收集到相同体积 ( 相同条件 ) 的气体时 ( 忽略溶液体积的变化及电极产物可能存在的溶解现象 ) ,阳极上收集到氧气的物质的量为 ________ mol 。
(3) 甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是通电后将 Co 2 + 氧化成 Co 3 + ,然后以 Co 3 + 作氧化剂把水中的甲醇氧化成 CO 2 而净化。实验室用右 图装置模拟上述过程:
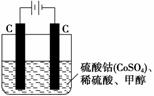
① 写出阳极电极反应式: _________________________________________________ 。
② 除去甲醇的离子反应为 6Co 3 + + CH 3 OH + H 2 O == =CO 2 ↑ + 6Co 2 + + 6H + ,该过程中被氧化的元素是 __________ ,当产生标准状况下 2.24 L CO 2 时,共转移电子 ________ mol 。
答案 (1) ① Cl - - 5e - + 2H 2 O == =ClO 2 ↑ + 4H +
② 0.01 在阴极发生 2H + + 2e - == =H 2 ↑ , H + 浓度减小,使 H 2 O H + + OH - 的平衡向右移动, OH - 浓度增大, pH 增大
(2)O 2 + 4e - == =2O 2 - 0.1
(3) ① Co 2 + - e - == =Co 3 + ② C( 或碳 ) 0.6
解析 (1) ① 阳极失去电子发生氧化反应。 ② 水电离产生的 H + 在阴极上放电产生氢气,转移电子的物质的量 n = 2 n (H 2 ) = 2 × (0.112 L÷22.4 L·mol - 1 ) = 0.01 mol ,则在内电路中移动的电荷为 0.01 mol ,每个 Na + 带一个单位的正电荷,则通过的 Na + 为 0.01 mol 。 (2) 电池工作时,正极上 O 2 得电子发生还原反应生成 O 2 - 。结合离子浓度可知电解过程可分为三个阶段:先是电解 CuCl 2 、然后电解 HCl 、最后电解水,由此可见阴极首先析出 0.1 mol Cu( 同时阳极析出 0.1 mol Cl 2 ) ,然后析出氢气;阳极上先是析出 0.2 mol Cl 2 ( 此时阴极已析出 0.1 mol H 2 ) ,再析出氧气,设阳极析出 x mol O 2 时两极析出气体体积相等,由题意可得: 0.2 + x = 0.1 + 2 x ,解得 x = 0.1 。 (3) ② 利用方程式可知 Co 3 + 被还原,甲醇中碳元素被氧化,依据方程式可知生成 1 mol CO 2 时,有 6 mol Co 3 + 还原为 Co 2 + ,可知转移电子 6 mol ,由此可推知当产生标况下 2.24 L CO 2 (0.1 mol) 时,转移电子 0.6 mol 。
从地面以大小为v1的初速度竖直向上抛出一个皮球,经过时间t皮球落回地面,落地时皮球的速度的大小为v2 2020-03-30 …
物体从a点由静止出发做匀加速运动在做匀减速运动到达b点证明:前后两过程平均速度相等且等于全程的平均速 2020-03-31 …
某汽车从静止出发做匀加速直线运动,经过20秒后改做匀速直线运动10秒,汽车已前进的总位移为330米 2020-04-05 …
某汽车从静止出发做匀加速直线运动,经过20秒后改做匀速直线运动10秒,汽车已前进的总位移为330米 2020-04-05 …
从车站出发,每隔一分钟开出一辆汽车.假设每辆汽车出发以后都是先以某一相同的加速度由静止开始做匀加速 2020-05-13 …
一辆出租车和一辆中巴分别从甲、乙两地出发.经过5分之2小时在距中点5km处相遇,出租车已行了全程的 2020-05-16 …
一辆出租车与一辆中巴分别从甲、乙两地同时出发经过5分之2小时在距中点5km处相遇,出租车已行了全程 2020-05-16 …
甲已从AB两站同时相向开出,已速度是的9/10,在离终点5千米相遇,遇后以原速继续前进,甲达B站时 2020-05-17 …
一艘轮船在水中行驶,已知水流速度为10千米每时,此船在静水中的速度是40千米每时.求此船在a.b两 2020-05-17 …
炮筒与水平方向的夹角为60°,炮弹从炮筒射出的速度为800m/s.求炮筒在竖直方向和水平方向的分速 2020-05-17 …