早教吧作业答案频道 -->化学-->
工业上常利用含硫废水生产Na2S2O3•5H2O,实验室可用如下装置(略去部分加持仪器)模拟生成过程.烧瓶C中发生反应如下:Na2S(aq)+H2O(l)+SO2(g)═Na2SO3(aq)+H2S(aq)(Ⅰ)2H2S(aq)+S
题目详情
工业上常利用含硫废水生产Na2S2O3•5H2O,实验室可用如下装置(略去部分加持仪器)模拟生成过程.
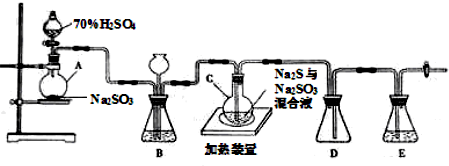
烧瓶C中发生反应如下:
Na2S(aq)+H2O(l)+SO2(g)═Na2SO3(aq)+H2S(aq) (Ⅰ)
2H2S(aq)+SO2(g)═3S(s)+2H2O(l) (Ⅱ)
S(s)+Na2SO3(aq)
Na2S2O3(aq) (Ⅲ)
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液注,若___,则整个装置气密性良好.装置D的作用是___.装置E中为___溶液.
(2)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为___.
(3)装置B的作用之一是观察SO2的生成速率. 实验中,为使SO2缓慢进入烧瓶C,采用的操作是___.已知反应(Ⅲ)相对较慢,则烧瓶C中反应达到终点的现象是___.反应后期可用酒精灯适当加热烧瓶A,实验室用酒精灯加热时必须使用石棉网的仪器含有___.
a.烧杯 b.蒸发皿 c.试管 d.锥形瓶
(4)反应终止后,烧瓶C中的溶液经蒸发浓缩即可析出Na2S2O3•5H2O,其中可能含有Na2SO3、Na2SO4等杂质.利用所给试剂设计实验,检测产品中是否存在Na2SO4,简要说明实验操作,现象和结论:___.
(已知Na2S2O3•5H2O遇酸易分 S2O32‾+2H+═S↓+SO2↑+H2O
供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液)

烧瓶C中发生反应如下:
Na2S(aq)+H2O(l)+SO2(g)═Na2SO3(aq)+H2S(aq) (Ⅰ)
2H2S(aq)+SO2(g)═3S(s)+2H2O(l) (Ⅱ)
S(s)+Na2SO3(aq)
| ||
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液注,若___,则整个装置气密性良好.装置D的作用是___.装置E中为___溶液.
(2)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为___.
(3)装置B的作用之一是观察SO2的生成速率. 实验中,为使SO2缓慢进入烧瓶C,采用的操作是___.已知反应(Ⅲ)相对较慢,则烧瓶C中反应达到终点的现象是___.反应后期可用酒精灯适当加热烧瓶A,实验室用酒精灯加热时必须使用石棉网的仪器含有___.
a.烧杯 b.蒸发皿 c.试管 d.锥形瓶
(4)反应终止后,烧瓶C中的溶液经蒸发浓缩即可析出Na2S2O3•5H2O,其中可能含有Na2SO3、Na2SO4等杂质.利用所给试剂设计实验,检测产品中是否存在Na2SO4,简要说明实验操作,现象和结论:___.
(已知Na2S2O3•5H2O遇酸易分 S2O32‾+2H+═S↓+SO2↑+H2O
供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液)
▼优质解答
答案和解析
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液柱,若液柱高度保持不变,则气密性良好,D中左侧为短导管,为安全瓶,防止倒吸;装置E起到吸收尾气中SO2、H2S的作用,可选用NaOH溶液,
故答案为:液柱高度保持不变,防止倒吸;NaOH;
(2)C中Na2S和Na2SO3恰好完全反应,由Na2S(aq)+H2O(l)+SO2(g)═Na2SO3(aq)+H2S(aq)(Ⅰ)
2H2S(aq)+SO2(g)═3S(s)+2H2O(l)(Ⅱ)
S(g)+Na2SO3(aq)
Na2S2O3(aq)(Ⅲ)
可知,(Ⅰ)×2+(Ⅱ)+(Ⅲ)×3,得到总反应为2Na2S(aq)+Na2SO3(aq)+3SO2(g)
3Na2S2O3(aq),则C中Na2S和Na2SO3物质的量之比为2:1,
故答案为:2:1;
(3)装置B的作用之一是观察SO2的生成速率,控制二氧化硫和氧气的体积比,使气体充分混合,为使SO2缓慢进入烧瓶C,应使二氧化硫的生成速率慢,可以从滴入酸的速率控制,根据C中发生的反应可知,烧瓶C中反应达到终点发生反应为硫与亚硫酸钠反应生成硫代硫酸钠,反:应的现象为溶液变澄清(或混浊消失),玻璃容器加热面积较大的仪器需要均匀加热,避免局部受热炸裂玻璃仪器,烧杯,锥形瓶加热需要垫石棉网,试管蒸发皿直接加热,选ad,
故答案为:控制滴加硫酸的速度,溶液变澄清(或混浊消失),ad;
(4)检测产品中是否存在Na2SO4,操作、现象和结论为取少量产品溶于足量稀盐酸中,静置,取上层清液(或过滤后取滤液),滴加BaCl2溶液,若出现白色沉淀则说明含有Na2SO4杂质,
故答案为:取少量产品溶于足量稀盐酸中,静置,取上层清液(或过滤后取滤液),滴加BaCl2溶液,若出现白色沉淀则说明含有Na2SO4杂质.
故答案为:液柱高度保持不变,防止倒吸;NaOH;
(2)C中Na2S和Na2SO3恰好完全反应,由Na2S(aq)+H2O(l)+SO2(g)═Na2SO3(aq)+H2S(aq)(Ⅰ)
2H2S(aq)+SO2(g)═3S(s)+2H2O(l)(Ⅱ)
S(g)+Na2SO3(aq)
| ||
可知,(Ⅰ)×2+(Ⅱ)+(Ⅲ)×3,得到总反应为2Na2S(aq)+Na2SO3(aq)+3SO2(g)
| ||
故答案为:2:1;
(3)装置B的作用之一是观察SO2的生成速率,控制二氧化硫和氧气的体积比,使气体充分混合,为使SO2缓慢进入烧瓶C,应使二氧化硫的生成速率慢,可以从滴入酸的速率控制,根据C中发生的反应可知,烧瓶C中反应达到终点发生反应为硫与亚硫酸钠反应生成硫代硫酸钠,反:应的现象为溶液变澄清(或混浊消失),玻璃容器加热面积较大的仪器需要均匀加热,避免局部受热炸裂玻璃仪器,烧杯,锥形瓶加热需要垫石棉网,试管蒸发皿直接加热,选ad,
故答案为:控制滴加硫酸的速度,溶液变澄清(或混浊消失),ad;
(4)检测产品中是否存在Na2SO4,操作、现象和结论为取少量产品溶于足量稀盐酸中,静置,取上层清液(或过滤后取滤液),滴加BaCl2溶液,若出现白色沉淀则说明含有Na2SO4杂质,
故答案为:取少量产品溶于足量稀盐酸中,静置,取上层清液(或过滤后取滤液),滴加BaCl2溶液,若出现白色沉淀则说明含有Na2SO4杂质.
看了工业上常利用含硫废水生产Na2...的网友还看了以下:
标准状况下,在干燥的烧瓶中充满纯净的NH3进行如图所示的喷泉实验下列说法错误的是()A.若烧瓶的氨 2020-05-14 …
实验室在标准状况下用一只容积为VL的烧瓶采用排空气法收集一瓶干燥的氨气做“喷泉实验”.实验结束时, 2020-05-14 …
“鹅颈烧瓶”实验的目的是证明? 2020-06-05 …
1、下列生物类群最早出现的是()A、细菌等原核生物.B、单细胞真核生物.C、多细胞真核生物.D、原 2020-06-12 …
巴斯德“鹅颈烧瓶”实验的结果使人们坚信“.”这一观点称为“”,它推翻了. 2020-07-24 …
设计并进行实验:小明同学进行了如下实验来研究烧瓶内水面上方的气体压强:(1)把细玻璃管插人装有半瓶水 2020-11-01 …
喷泉实验中关于大气压强的物理题喷泉实验这个实验可以说明:1.烧瓶里的气压大于大气压强.2.烧瓶里的压 2020-12-03 …
下面是著名的“鹅颈烧瓶”实验:(1)鹅颈烧瓶中放入肉汤后要煮沸的目的是:.(2)第一步实验瓶中无微生 2020-12-12 …
关于生命的起源,有许多假说,下列说法中不正确的是()A.自然发生论者认为生命是自然发生的B.巴斯德的 2020-12-18 …
在标准情况下,用一充有气体的烧瓶做喷泉实验,当水进入烧瓶后,最终可得浓度为0.045MOL/L的)在 2021-01-13 …