硫代硫酸钠是一种重要的化工产品。工业上常利用含硫废水生产Na2S2O3•5H2O,实验室可用如下装置(略去部分加持仪器)模拟生成过程。烧瓶C中
硫代硫酸钠是一种重要的化工产品。工业上常利用含硫废水生产 Na 2 S 2 O 3 •5H 2 O , 实验室可用如下装置 ( 略去部分加持仪器 ) 模拟生成过程。
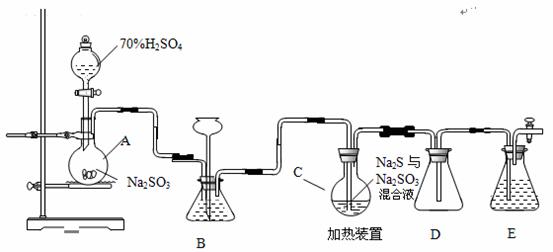
烧瓶 C 中发生反应如下:
Na 2 S ( aq ) +H 2 O ( l ) +SO 2 ( g ) =Na 2 SO 3 ( aq ) +H 2 S ( aq ) ( I )
2H 2 S ( aq ) +SO 2 ( g ) =3S ( s ) +2H 2 O ( l ) ( II )
S ( s ) +Na 2 SO 3 ( aq ) ![]() Na 2 S 2 O 3 ( aq ) ( III )
Na 2 S 2 O 3 ( aq ) ( III )
( 1 ) 仪器组装完成后 , 关闭两端活塞 , 向装置 B 中的长颈漏斗内注入液体至形成一段液注 , 若 , 则整个装置气密性良好。装置 D 的作用是 。装置 E 中为 溶液。
( 2 )为提高产品纯度,应使烧瓶 C 中 Na 2 S 和 Na 2 SO 3 恰好完全反应,则烧瓶 C 中 Na 2 S 和 Na 2 SO 3 物质的量之比为 。
( 3 )装置 B 的作用之一是观察 SO 2 的生成速率,其中的液体最好选择 。
a .蒸馏水 b .饱和 Na 2 SO 3 溶液
c .饱和 NaHSO 3 溶液 d .饱和 NaHCO 3 溶液
( 4 )实验中,为使 SO 2 缓慢进入烧瓶 C ,采用的操作是 。
( 5 )已知反应( III )相对较慢,则烧瓶 C 中反应达到终点的现象是 。
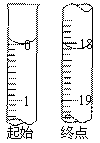 ( 6 )反应终止后,烧瓶 C 中的溶液经蒸发浓缩 冷却 , 过滤,洗涤,干燥, 即得到粗产品(主要含有 Na 2 S 2 O 3 •5H 2 O 和其他杂质)。 某兴趣小组为测定该产品纯度,准确称取 4.96 g 产品,用适量蒸馏水溶解,以淀粉作指示剂,用 0.1000 mol•L¯ 1 碘的标准溶液滴定。反应原理为: 2S 2 O 3 2 - + I 2 = S 4 O 6 2 - + 2I¯ ,滴定至终点时,滴定起始和终点的液面位置如下图,则产品的纯度为 _________ 。经仪器分析,该产品纯度为 16% ,分析该兴趣小组测定产品纯度偏差的原因(忽略人为误差)
( 6 )反应终止后,烧瓶 C 中的溶液经蒸发浓缩 冷却 , 过滤,洗涤,干燥, 即得到粗产品(主要含有 Na 2 S 2 O 3 •5H 2 O 和其他杂质)。 某兴趣小组为测定该产品纯度,准确称取 4.96 g 产品,用适量蒸馏水溶解,以淀粉作指示剂,用 0.1000 mol•L¯ 1 碘的标准溶液滴定。反应原理为: 2S 2 O 3 2 - + I 2 = S 4 O 6 2 - + 2I¯ ,滴定至终点时,滴定起始和终点的液面位置如下图,则产品的纯度为 _________ 。经仪器分析,该产品纯度为 16% ,分析该兴趣小组测定产品纯度偏差的原因(忽略人为误差)
。
[ M ( Na 2 S 2 O 3 •5H 2 O ) =248g / mol]
( 1 )液柱高度保持不变( 1 分 ) 防止倒吸( 1 分 ) NaOH (合理即得分)( 1 分 )
( 2 ) 2:1 ( 2 分 )
(3) c ( 2 分 )
(4) 控制滴加硫酸的速度(合理即得分)( 2 分 )
(5) 溶液变澄清(或浑浊消失)( 2 分 )
( 6 ) 18.1% ( 2 分 )
粗产品中含有 Na 2 SO 3 (或 Na 2 S )可以消耗 I 2 ,使消耗的碘水体积偏大 ( 2 分 )
下列有关电解质溶液的说法正确的是()A.在蒸馏水中滴加浓硫酸,KW不变B.在硫化钠稀溶液中,c(H 2020-04-12 …
在平行四边形ABCD中∠A加∠C=90°,∠A=∠B= 2020-05-13 …
为什么在稀硫酸中滴加碳酸钠,立即有二氧化碳放出,而在碳酸钠中滴加稀硫酸,刚开始没有二氧化碳放出?为 2020-05-16 …
用铁片与稀硫酸反应制取氢气时,下列措施不能使反应速率加快的是( )A. 加热B. 不用稀硫酸改用 2020-05-17 …
下列函数关系图对应正确的一项是()A.向饱和的硝酸钾溶液中加硝酸钾晶体B.向等量的锌和铁中加入足量 2020-06-04 …
九年级化学,在硫酸铜和硫酸亚铁的混合溶液中加入一定量的锌粉,在硫酸铜和硫酸亚铁的混合溶液中加入一定 2020-06-10 …
1.10mlc(MnSO4)=0.0015mol/L的硫酸锰溶液中,先加入0.495g硫酸铵固体( 2020-07-05 …
下列实验操作正确的是()A.直接在瓶口闻药品的气味B.为了避免滴出液体,把胶头滴管伸入试管中滴加C 2020-07-11 …
对下列实验现象描述正确的是()A.氯化铜溶液中加入铁粉后,溶液颜色变为无色B.硫酸铵中加入氢氧化钠 2020-07-15 …
下列各项操作中,能发生先沉淀后溶解的现象的是[]A.向溶液中逐滴加入稀硫酸B.向胶体中逐滴加入过量稀 2020-11-03 …