随着信息产业的高速发展和家用电器的普及,我国印刷电路板(PCB)的生产呈现急剧增长之势。废旧电路板的增多给我们带来了环境问题,目前我们台州大多采用32%~35%的FeCl3溶液溶解
随着信息产业的高速发展和家用电器的普及,我国印刷电路板(PCB)的生产呈现急剧增长之势。废旧电路板的增多给我们带来了环境问题,目前我们台州大多采用32%~35%的FeCl 3 溶液溶解印刷线路板上的金属铜,从而进行对铜的回收和利用。经分析腐蚀废液中主要含有HCl 、FeCl 2 和CuCl 2 等溶质。
(1)用32%~35%的FeCl 3 溶液溶解印刷线路板上的金属铜的原理是
(用离子方程式表示): ▲ 。
(2)工业上有多种回收腐蚀废液中铜的方法,下面是常用的两种方法:
Ⅰ、电化学方法回收腐蚀废液中铜,则阳极(石墨)上的电极反应式为: ▲ 。
Ⅱ、工业上也可以用铁粉回收腐蚀废液中的铜:
①用铁粉回收铜的实验操作为 ▲ 。
②科学家对铁置换铜工艺的研究如下:
分别用还原铁粉、废铁屑和废铁屑在超声波粉碎处理下置换铜,将置换出的铜粉放入250mL烧杯中,加入120mL 1.5 mol·L - 1 的硫酸,水浴加热,控制温度在70 ℃ ,搅拌,在10、20、30、40、50、60min时,分别用吸管移取0.5g左右的铜于试管内,将上层清液倒回小烧杯中,用蒸馏水洗净试样,过滤,在105℃烘箱中烘干后测定铜粉中铁的含量。其结果如图所示。
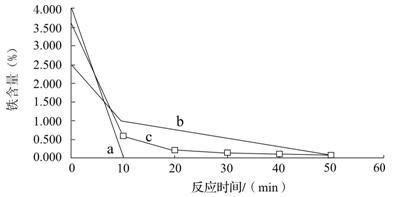
已知a表示用还原铁粉置换铜的除铁效果,b表示用废铁屑置换铜的除铁效果,c表示用废铁屑在超声波下置换铜的除铁效果,你认为除铁效果最好的是 ▲ (填a、b或c),其原因是 ▲ 。
(3)工业上也可用腐蚀废液生成CuCl 2 ·2H 2 O,从而进行对废液的利用,其工艺流程如下:

已知:pH ≥9.6时,Fe 2+ 以Fe(OH) 2 的形式完全沉淀; pH ≥6.4时,Cu 2+ 以Cu(OH) 2 的形式完全沉淀; pH在3~4时,Fe 3+ 以Fe(OH) 3 的形式完全沉淀。
①试剂A最好应选用 ▲ 。
a.浓硫酸 b.Cl 2 c.NaClO d.NaOH溶液
理由是 ▲ 。
②分析有关物质的溶解度曲线(如下图),为了获得CuCl 2 ·2H 2 O晶体,对滤液B进行的操作是: ▲ 、 ▲ ,过滤得到产品。
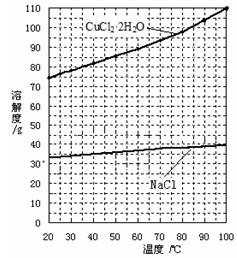
③测定CuCl 2 ·2H 2 O产品的质量分数可按下法:取2.000g产品,用水溶解后,加入60.00 mL 0.4000 mol·L - 1 的KI溶液(足量),充分反应后加入淀粉指示剂,用0.4000 mol·L - 1 Na 2 S 2 O 3 标准溶液滴定,耗去此标准液25.00 mL时,刚好到达滴定终点。
已知:2Cu 2 + +4I - =2CuI↓+I 2 I 2 +2S 2 O 3 2 - =2I - +S 4 O 6 2 -
此产品中CuCl 2 ·2H 2 O的质量分数为 ▲ 。
(15分)
(1) 2Fe 3+ +Cu=2Fe 2+ +Cu 2+ (1分)
(2)Ⅰ、阳极:Fe 2+ -e -  Fe 3+ (2分)
Fe 3+ (2分)
Ⅱ、①加入过量铁粉CuCl 2 + Fe Cu + FeCl 2 , 过滤,在所得固体中加入稀盐酸溶解残余的铁,再滤出固体洗涤得铜。(2分)②a (1分) ;使用细铁粉,还原得细铜粉,铜粉颗粒越小,与酸接触的表面积越大,内部的铁与酸反应越快,即除铁效率越高。(2分)
Cu + FeCl 2 , 过滤,在所得固体中加入稀盐酸溶解残余的铁,再滤出固体洗涤得铜。(2分)②a (1分) ;使用细铁粉,还原得细铜粉,铜粉颗粒越小,与酸接触的表面积越大,内部的铁与酸反应越快,即除铁效率越高。(2分)
(3)①c (1分) ;NaClO能将Fe 2 + 氧化为Fe 3 + ,且反应能消耗H + ,增大溶液的pH使Fe 3 + ?? 沉淀(2分)
②蒸发浓缩,冷却结晶(2分) ③85.50% (2分)
给经理写一封邮件:要求购买电脑和打印机,因为现有的己使用五年以上,经常出现故障,影响工作.此外,3 2020-05-13 …
某种打印机每台售价460元,比进价贵15%.如果一次性进货120台以上,则进价可下降5%.某商场一 2020-05-13 …
突然有个疑问!比较.点,关于台风的问题.印象中,台风是发生在夏季的,但是,书上说:发生在太平洋西部 2020-06-09 …
阳光小学购买电脑60台,购买打印机的台数比电脑少50%,电脑和打印机共购买了多少台? 2020-07-18 …
电脑有45台,比复印机的台数多四分之一,复印机有多少台?急急急 2020-11-20 …
1、某地区代理商第一年销售打印机4000台,计划平均每年的销售量比上一年增加12%,那么第五年销售量 2020-11-21 …
因印度与台湾的市场和经济互补性很强,近年来,两地不断在多个领域加强合作.认真阅读下列材料回答问题.材 2020-12-01 …
六年级数学题一台复印机共有7个缩小或放大的按键,如下图.如果其中那个“100%”的按键坏了,我们进行 2020-12-02 …
印度河台古城之迷①1856年,英属东印度公司在印度河谷铺设铁路轨道时偶然发现,这一带除了优质的硬砖, 2020-12-08 …
等多少台和多少台等意思一样吗比如:“打印机10台,电话机30台,电脑35台等”和“打印机10台,电话 2021-01-12 …