早教吧作业答案频道 -->化学-->
[背景材料]氮化铝(AlN)陶瓷是一种类金刚石氮化物的新型无机非金属材料,最高可稳定到2200℃.导热性好,热膨胀系数小,是良好的耐热冲击材料.抗熔融金属侵蚀的能力强,是熔铸纯铁
题目详情
[背景材料]氮化铝(AlN)陶瓷是一种类金刚石氮化物的新型无机非金属材料,最高可稳定到2200℃.导热性好,热膨胀系数小,是良好的耐热冲击材料.抗熔融金属侵蚀的能力强,是熔铸纯铁、铝或铝合金理想的坩埚材料.氮化铝还是电绝缘体,介电性能良好,用作电器元件也很有希望.超细氮化铝粉末被广泛应用于大规模集成电路生产领域.
其制取原理为:Al2O3+3C+N2
2AlN+3CO
[问题探究]某化学研究性学习小组成员根据氮化铝的制取原理,进行了如下探究.
问题1、在制取氮化铝时由于反应不完全,氮化铝产品中所含杂质除了碳以外还可能存在___.
问题2、为测定该产品中有关成分的含量,甲、乙两同学设计了以下两个实验:
(1)甲同学:称取10.00g样品,将其加入过量的氢氧化钠溶液中共热并蒸干,AlN跟氢氧化钠溶液反应生成NaAlO2,并放出氨气3.36L(标准状况).上述反应的化学方程式为___.
(2)乙同学:称取10.00g样品置于反应器中,通入2.016L(标准状况)O2,在高温下充分反应后测得气体的密度为1.34g•L-1(已折成标准状况,AlN不跟O2反应).该样品中含杂质碳___g.
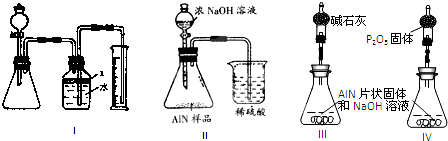
问题3、丙同学受到甲、乙同学实验的启发,认为测定某氮化铝中含有碳或氧化铝杂质,可用图中I的一些装置来进行检验,根据AlN与NaOH溶液反应所生成氨气的体积来测定样品中氮化铝的质量分数,并根据实验现象来确定杂质的成分(实验中导管体积忽略不计)
(1)实验有关操作为:
①往锥形瓶中放入适量的AlN样品:②从分液漏斗往锥形瓶中加入过量的浓NaOH;③检验装置的气密性;④测定收集到水的体积.
正确的操作顺序为___.
(2)本试验中检查装置气密性的方法是___.
(3)广口瓶中的试剂X可最好选用___(填选项的标号).
A、苯 B、酒精 C、植物油 D、CCl4
(4)广口瓶的液体没有装满(上方留有少量空间),实验测得NH3的体积将___(填偏大、偏小或不变).
(5)若实验中测得样品的质量为wg,氨气的体积为aL(标况下),则样品中AlN的质量分数为___(AlN的式量为41).
问题4、丁同学认为,丙同学的实验方法,可能因气体体积测量不准,导致误差较大.建议改用图中的Ⅱ装置进行同样实验,通过测定烧杯中硫酸的增重来确定样品中AlN的质量分数.你认为是否可行?___(填入“可行”、“不可行”),最简单的改进方法为___.
问题5、戊同学仔细思考了丁同学的装置后,认为此装置所测测得的样品中AlN含量偏小.其原因是___.若忽略此原因的话,只要用图中的III或IV两个装置中的一种,只需进行简单而又必要的数据测定,可比较准确地确定样品中AlN的质量分数.较合理的装置为___(填代号).但是戊同学的装置有缺陷所测结果将偏高或偏低___.
其制取原理为:Al2O3+3C+N2
| 高温 |
| |
[问题探究]某化学研究性学习小组成员根据氮化铝的制取原理,进行了如下探究.
问题1、在制取氮化铝时由于反应不完全,氮化铝产品中所含杂质除了碳以外还可能存在___.
问题2、为测定该产品中有关成分的含量,甲、乙两同学设计了以下两个实验:
(1)甲同学:称取10.00g样品,将其加入过量的氢氧化钠溶液中共热并蒸干,AlN跟氢氧化钠溶液反应生成NaAlO2,并放出氨气3.36L(标准状况).上述反应的化学方程式为___.
(2)乙同学:称取10.00g样品置于反应器中,通入2.016L(标准状况)O2,在高温下充分反应后测得气体的密度为1.34g•L-1(已折成标准状况,AlN不跟O2反应).该样品中含杂质碳___g.
问题3、丙同学受到甲、乙同学实验的启发,认为测定某氮化铝中含有碳或氧化铝杂质,可用图中I的一些装置来进行检验,根据AlN与NaOH溶液反应所生成氨气的体积来测定样品中氮化铝的质量分数,并根据实验现象来确定杂质的成分(实验中导管体积忽略不计)

(1)实验有关操作为:
①往锥形瓶中放入适量的AlN样品:②从分液漏斗往锥形瓶中加入过量的浓NaOH;③检验装置的气密性;④测定收集到水的体积.
正确的操作顺序为___.
(2)本试验中检查装置气密性的方法是___.
(3)广口瓶中的试剂X可最好选用___(填选项的标号).
A、苯 B、酒精 C、植物油 D、CCl4
(4)广口瓶的液体没有装满(上方留有少量空间),实验测得NH3的体积将___(填偏大、偏小或不变).
(5)若实验中测得样品的质量为wg,氨气的体积为aL(标况下),则样品中AlN的质量分数为___(AlN的式量为41).
问题4、丁同学认为,丙同学的实验方法,可能因气体体积测量不准,导致误差较大.建议改用图中的Ⅱ装置进行同样实验,通过测定烧杯中硫酸的增重来确定样品中AlN的质量分数.你认为是否可行?___(填入“可行”、“不可行”),最简单的改进方法为___.
问题5、戊同学仔细思考了丁同学的装置后,认为此装置所测测得的样品中AlN含量偏小.其原因是___.若忽略此原因的话,只要用图中的III或IV两个装置中的一种,只需进行简单而又必要的数据测定,可比较准确地确定样品中AlN的质量分数.较合理的装置为___(填代号).但是戊同学的装置有缺陷所测结果将偏高或偏低___.
▼优质解答
答案和解析
问题1、碳和氧化铝是固体,由于反应不完全,反应物中有氧化铝固体可能未反应完而留在AlN中,故答案为:氧化铝;
问题2、(1)由于AlN跟氢氧化钠溶液反应生成NaAlO2、并放出NH3,其反应方程式为:AlN+NaOH+H2O=NaAlO2+NH3↑,故答案为:AlN+NaOH+H2O=NaAlO2+NH3↑;
(2)反应产物可能CO2、CO或CO2和CO、CO2和O2的混合气体,根据气体产物的密度可计算出气体产物的平均相对分子质量为30,所以生成气体必定是CO2和CO混合气体.设混合气体中含有CO2xmol,CO ymol,根据氧原子守恒有2x+y=0.18…①,根据平均相对分子质量有44x+28y=30(x+y)…②,联立方程解得:x=0.02,y=0.14.所以,样品中C的质量为(0.02+0.14)×12=1.92g,故答案为:1.92;
问题3、(1)检查装置的气密性往往是在加药品前进行,否则将可能造成药品的浪费,故先检验气密性,然后在锥形瓶中放入适量的AlN样品,再从分液漏斗往锥形瓶中加入过量的浓NaOH,测定收集到水的体积,
故答案为:③①②④;
(2)检查气密性的关键是整个体系要处于密闭状态,常用的方法有:密封气体利用气体的热胀冷缩或液封气体形成液面高度差.由装置可知,适合利用气体热胀冷缩.具体操作为:关闭分液漏斗活塞,微热锥形瓶,广口瓶中右侧导管水柱上升,恒温时水柱并不回落.
故答案为:关闭分液漏斗活塞,微热锥形瓶,广口瓶中右侧导管水柱上升,恒温时水柱并不回落;
(3)A.苯易挥发,会浪费试剂、影响氨气体积测定,故A错误;
B.酒精易挥发,挥发出来的气体对实验有影响,同时由于酒精易溶于水,也不能达到隔离的目的,故B错误;
C.植物油既不溶于水,密度小于水也不易挥发,可以把氨气与水进行隔离,故C正确;
D.CCl4密度大于水,不能起到隔离作用,故D错误.
故答案为:C;
(4)本次实验的目的在于测定产生气体的体积而不是收集纯净的气体,氨气排出装置的气体,按占据原来气体空间,广口瓶内的液体是否充满不影响所收集到的NH3体积大小,故答案为:不变;
(5)氨气的体积为aL(标况下)的物质的量为
=
mol,由方程式AlN+NaOH+H2O=NaAlO2+NH3↑可知,样品中AlN的物质的量为=
mol,所以AlN的质量为
mol×41g/mol=
g,样品中AIN的质量分数为
×100%=
%.故答案为:
%;
问题4、II中NH3极易被吸收,发生倒吸现象,同时氨气中含有水蒸气,影响氨气质量的测定,所以不可行.所作的改正为:在装置之间添加盛有碱石灰的干燥管,烧杯导管的末端接一倒扣的漏斗来吸收氨气.故答案为:不可行;在装置之间添加盛有碱石灰的干燥管,烧杯导管的末端接一倒扣的漏斗来吸收氨气;
问题5、通过测定氨气的质量(即实验中硫酸增重量)来推算氮化铝的质量.因为有一部分氨气留在锥形瓶中,反应产生的氨气无法全部被稀硫酸吸收,因此实验测得AlN的质量分数将偏小.
戊同学设计的装置Ⅲ较合理,这是通过反应前后总质量减少来测定AlN的质量分数.这里的干燥管作用是吸收被NH3带出来的水蒸气(反应放热,更容易使产生的水蒸气被NH3带走),若用IV,则NH3被吸收,反应前后几无质量差.但戊同学仍未考虑到空气中的水蒸气或CO2的进入,否则,将造成反应后的总质量增大,相当于NH3的减少,导致结果偏低.故答案为:反应产生的氨气不可能被完全吸收;Ⅲ;偏低.
问题2、(1)由于AlN跟氢氧化钠溶液反应生成NaAlO2、并放出NH3,其反应方程式为:AlN+NaOH+H2O=NaAlO2+NH3↑,故答案为:AlN+NaOH+H2O=NaAlO2+NH3↑;
(2)反应产物可能CO2、CO或CO2和CO、CO2和O2的混合气体,根据气体产物的密度可计算出气体产物的平均相对分子质量为30,所以生成气体必定是CO2和CO混合气体.设混合气体中含有CO2xmol,CO ymol,根据氧原子守恒有2x+y=0.18…①,根据平均相对分子质量有44x+28y=30(x+y)…②,联立方程解得:x=0.02,y=0.14.所以,样品中C的质量为(0.02+0.14)×12=1.92g,故答案为:1.92;
问题3、(1)检查装置的气密性往往是在加药品前进行,否则将可能造成药品的浪费,故先检验气密性,然后在锥形瓶中放入适量的AlN样品,再从分液漏斗往锥形瓶中加入过量的浓NaOH,测定收集到水的体积,
故答案为:③①②④;
(2)检查气密性的关键是整个体系要处于密闭状态,常用的方法有:密封气体利用气体的热胀冷缩或液封气体形成液面高度差.由装置可知,适合利用气体热胀冷缩.具体操作为:关闭分液漏斗活塞,微热锥形瓶,广口瓶中右侧导管水柱上升,恒温时水柱并不回落.
故答案为:关闭分液漏斗活塞,微热锥形瓶,广口瓶中右侧导管水柱上升,恒温时水柱并不回落;
(3)A.苯易挥发,会浪费试剂、影响氨气体积测定,故A错误;
B.酒精易挥发,挥发出来的气体对实验有影响,同时由于酒精易溶于水,也不能达到隔离的目的,故B错误;
C.植物油既不溶于水,密度小于水也不易挥发,可以把氨气与水进行隔离,故C正确;
D.CCl4密度大于水,不能起到隔离作用,故D错误.
故答案为:C;
(4)本次实验的目的在于测定产生气体的体积而不是收集纯净的气体,氨气排出装置的气体,按占据原来气体空间,广口瓶内的液体是否充满不影响所收集到的NH3体积大小,故答案为:不变;
(5)氨气的体积为aL(标况下)的物质的量为
| aL |
| 22.4L/mol |
| a |
| 22.4 |
| a |
| 22.4 |
| a |
| 22.4 |
| 41a |
| 22.4 |
| ||
| wg |
| 4100a |
| 22.4w |
| 4100a |
| 22.4w |
问题4、II中NH3极易被吸收,发生倒吸现象,同时氨气中含有水蒸气,影响氨气质量的测定,所以不可行.所作的改正为:在装置之间添加盛有碱石灰的干燥管,烧杯导管的末端接一倒扣的漏斗来吸收氨气.故答案为:不可行;在装置之间添加盛有碱石灰的干燥管,烧杯导管的末端接一倒扣的漏斗来吸收氨气;
问题5、通过测定氨气的质量(即实验中硫酸增重量)来推算氮化铝的质量.因为有一部分氨气留在锥形瓶中,反应产生的氨气无法全部被稀硫酸吸收,因此实验测得AlN的质量分数将偏小.
戊同学设计的装置Ⅲ较合理,这是通过反应前后总质量减少来测定AlN的质量分数.这里的干燥管作用是吸收被NH3带出来的水蒸气(反应放热,更容易使产生的水蒸气被NH3带走),若用IV,则NH3被吸收,反应前后几无质量差.但戊同学仍未考虑到空气中的水蒸气或CO2的进入,否则,将造成反应后的总质量增大,相当于NH3的减少,导致结果偏低.故答案为:反应产生的氨气不可能被完全吸收;Ⅲ;偏低.
看了[背景材料]氮化铝(AlN)陶...的网友还看了以下:
我正在学习带钢的销售,请问他们说的材料要高速冲的是什么意思 跟普通材料有什么不一样,我做的光亮带就 2020-05-17 …
把一本口语书(57篇)背得滚瓜烂熟有用吗是把有限的几本英语材料背得滚瓜烂熟(背下来后再背100遍) 2020-06-16 …
巴以冲突是当前地区冲突的热点之一,冲突背后隐藏着深刻的历史根源.既有宗教的、民族的因素,更重要的是大 2020-11-16 …
对于四冲程的柴油机和汽油机,下列说法正确的是()A.第一冲程进入气缸里的都是燃料的混合物B.第二冲程 2020-12-05 …
在人类历史上,文明的交流演进过程异彩纷呈,特点鲜明,阅读材料回答问题.材料一材料二世界与西方的冲突至 2020-12-08 …
在人类历史上,文明的交流演进过程异彩纷呈,特点鲜明,阅读材料回答问题.材料一材料二世界与西方的冲突至 2020-12-08 …
阅读下列材料,结合所学知识回答问题:阅读下列材料:材料一……冲突中的融合是社会发展的一种模式。在这种 2020-12-18 …
(13分)阅读下列材料并回答问题。材料一……冲突中的融合是社会发展的一种模式。在这种模式中,相互制约 2021-01-13 …
阅读下列材料:材料一……冲突中的融合是社会发展的一种模式。在这种模式中,相互制约的历史传统通过冲突而 2021-01-13 …
阅读下列材料:材料一……冲突中的融合是社会发展的一种模式。在这种模式中,相互制约的历史传统通过冲突而 2021-01-13 …