乙醇是重要的有机化工原料,可由乙烯气相直接水合法生产或间接水合法生产。回答下列问题:(1)间接水合法是指先将乙烯与浓硫酸反应生成硫酸氢乙酯(C2H5OSO3H),再
乙醇是重要的有机化工原料,可由乙烯气相直接水合法生产或间接水合法生产。回答下列问题:
(1) 间接水合法是指先将乙烯与浓硫酸反应生成硫酸氢乙酯 (C 2 H 5 OSO 3 H) ,再水解生成乙醇。写出相应反应的化学方程式: ________________________________________ 。
(2) 已知:
甲醇的脱水反应
2CH 3 OH(g) == =CH 3 OCH 3 (g) + H 2 O(g)
Δ H 1 =- 23.9 kJ·mol - 1
甲醇制烯烃的反应
2CH 3 OH(g) == =C 2 H 4 (g) + 2H 2 O(g)
Δ H 2 =- 29.1 kJ·mol - 1
乙醇的异构化反应 C 2 H 5 OH(g) == =CH 3 OCH 3 (g)
Δ H 3 =+ 50.7 kJ·mol - 1
则乙烯气相直接水合反应 C 2 H 4 (g) + H 2 O(g) == =C 2 H 5 OH(g) 的 Δ H ________kJ·mol - 1 。与间接水合法相比,气相直接水合法的优点是 ____________________________________ 。
(3) 如图所示为气相直接水合法中乙烯的平衡转化率与温度、压强的关系 [ 其中 n (H 2 O) ∶ n (C 2 H 4 ) = 1 ∶ 1] 。
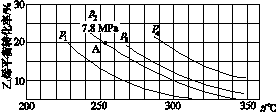
①列式计算乙烯水合制乙醇反应在图中 A 点的平衡常数 K p = ____________________( 用平衡分压代替平衡浓度计算,分压=总压 × 物质的量分数 ) 。
②图中压强 ( p 1 、 p 2 、 p 3 、 p 4 ) 的大小顺序为 ____ ,理由是 ___________________ 。
③气相直接水合法常采用的工艺条件为:磷酸 / 硅藻土为催化剂,反应温度 290 ℃、压强 6.9 MPa , n (H 2 O) ∶ n (C 2 H 4 ) = 0.6 ∶ 1 。乙烯的转化率为 5% ,若要进一步提高乙烯转化率,除了可以适当改变反应温度和压强外,还可采取的措施有 ________________________________________________________________________ 、
________________________________________________________________________ 。
(1)C 2 H 4 + H 2 SO 4 ― →C 2 H 5 OSO 3 H 、 C 2 H 5 OSO 3 H + H 2 O ― →C 2 H 5 OH + H 2 SO 4 (2) - 45.5 污染小、腐蚀性小等 (3) ① ![]() =
= 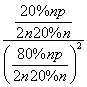 =
=
![]() = 0.07(MPa) - 1 ② p 1 < p 2 < p 3 < p 4 反应分子数减少,相同温度下,压强升高乙烯转化率提高
= 0.07(MPa) - 1 ② p 1 < p 2 < p 3 < p 4 反应分子数减少,相同温度下,压强升高乙烯转化率提高
③ 将产物乙醇液化移去 增加 n (H 2 O) ∶ n (C 2 H 4 ) 比
[ 解析 ] (1) 根据题中信息可写出由乙烯与浓硫酸间接水合法制乙醇的反应为 C 2 H 4 + H 2 SO 4 ― →C 2 H 5 OSO 3 H 和 C 2 H 5 OSO 3 H + H 2 O ― →C 2 H 5 OH + H 2 SO 4 。 (2) 根据盖斯定律 ① - ② - ③ 得: C 2 H 4 (g) + H 2 O(g) == =C 2 H 5 OH(g) Δ H =- 45.5 kJ·mol - 1 。间接水合法中用到浓硫酸等强腐蚀性物质,与其相比直接水合法具有污染小、腐蚀性小等优点。 (3) ① 设起始时 C 2 H 4 和 H 2 O(g) 的物质的量均为 n ,根据 C 2 H 4 的转化率为 20% ,则平衡时 C 2 H 4 、 H 2 O(g) 和 C 2 H 5 OH 的物质的量分别为 80% n 、 80% n 和 20% n ,则 K p = ![]() =
= 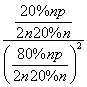 =
= ![]() = 0.07(MPa) - 1 。 ② 增大压强,平衡将正向移动,能提高 C 2 H 4 的转化率,即压强 p 1 < p 2 < p 3 < p 4 。 ③ 为了使平衡正向移动,还可以将乙醇液化及时分离,或增大 n (H 2 O) : n (C 2 H 4 ) 之比等措施。
= 0.07(MPa) - 1 。 ② 增大压强,平衡将正向移动,能提高 C 2 H 4 的转化率,即压强 p 1 < p 2 < p 3 < p 4 。 ③ 为了使平衡正向移动,还可以将乙醇液化及时分离,或增大 n (H 2 O) : n (C 2 H 4 ) 之比等措施。
下列合成高分子化合物的反应及类型都正确的是()A.合成有机玻璃:缩聚反应B.合成橡胶:加聚反应C. 2020-04-08 …
为什么CATIA动态仿真CV接合我第三个旋转选不了轴线啊?下面是简化的,三根轴的XY平面我全选择了 2020-05-12 …
下列合同关于履行地点的说法正确的是A.不作为债务的履行地应是债权人的所在的B.不动产权的转移,应在 2020-05-22 …
水绵接合生殖时,从一个配子囊放出的配子与另一个配子囊放出的配子在水中结合形成合子。()A.正确B. 2020-05-25 …
128.根据我国《担保法》规定,下列选项所列合同中哪些合同债务人不履行的,债权人享有留置权?()A 2020-06-21 …
英语语法中,某些连接词的用法一个句子:,()~.在()处能否填and、so、though、if、b 2020-06-26 …
设计合同是委托合同吗第95题下列合同中属于委托合同的有()。A.工程监理合同B.设计合同C.咨询合 2020-07-06 …
(2014•秦淮区二模)小明使用电阻箱间接测量小灯泡的电阻,实验电路如图所示.请将实验步骤填写完整 2020-07-18 …
如何在Excel中,连接两列,如何使第三列中的等号对齐?如,我有两列,A列:zhangliwang 2020-07-25 …
下列合同适用于《合同法》的是?A.政府采购合同B.以悬赏广告为要约订立的合同C.以招标、投标订立的合 2020-12-21 …