早教吧作业答案频道 -->化学-->
为测定某种胃药中CaCO3含量,化学兴趣小组同学设计了以下两种方案(药片中的其它成分与盐酸和NaOH均不反应,请回答有关问题:方案一:用图1装置测量一定量样品与足量稀盐酸反应生成CO2
题目详情
为测定某种胃药中CaCO3含量,化学兴趣小组同学设计了以下两种方案(药片中的其它成分与盐酸和NaOH均不反应,请回答有关问题:
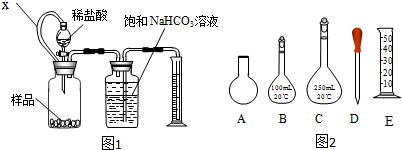
方案一:用图1装置测量一定量样品与足量稀盐酸反应生成CO2的体积计算CaCO3的含量;装置中连通管X的作用是___.
方案二:用滴定法测定,有以下几步操作:
A.配制0.1mol/LHC1溶液和0.100mol/LNaOH溶液
B.取一粒药片(0.100g),研碎后加入20mL蒸馏水
C.以酚酞为指示剂,用0.100mol/LNaOH溶液滴定时,消耗NaOH溶液VmL达到终点
D.用酸式滴定管加入25ml 0.1mol/LHC1溶液,充分反应
(1)滴定过程的正确操作顺序为___(填字母).滴定终点的判断依据是___.
(2)若需重复滴定4次,配制0.1mol/LHC1溶液需选用图2所示仪器中的___(填字母).
(3)对滴定过程两种假定情况的讨论:(填“无影响”、“偏高”、“偏低”)
①若用蒸馏水冲洗锥形瓶,则会使测定的胃药中CaCO3含量:___;
②碱式滴定管用蒸馏水洗涤后,未用标准液润洗导致所测胃药中CaCO3含量___,
(4)经测定,每次消耗NaOH溶液体积的平均值为13.00ml,则该胃药中CaCO3的质量分数为___.

方案一:用图1装置测量一定量样品与足量稀盐酸反应生成CO2的体积计算CaCO3的含量;装置中连通管X的作用是___.
方案二:用滴定法测定,有以下几步操作:
A.配制0.1mol/LHC1溶液和0.100mol/LNaOH溶液
B.取一粒药片(0.100g),研碎后加入20mL蒸馏水
C.以酚酞为指示剂,用0.100mol/LNaOH溶液滴定时,消耗NaOH溶液VmL达到终点
D.用酸式滴定管加入25ml 0.1mol/LHC1溶液,充分反应
(1)滴定过程的正确操作顺序为___(填字母).滴定终点的判断依据是___.
(2)若需重复滴定4次,配制0.1mol/LHC1溶液需选用图2所示仪器中的___(填字母).
(3)对滴定过程两种假定情况的讨论:(填“无影响”、“偏高”、“偏低”)
①若用蒸馏水冲洗锥形瓶,则会使测定的胃药中CaCO3含量:___;
②碱式滴定管用蒸馏水洗涤后,未用标准液润洗导致所测胃药中CaCO3含量___,
(4)经测定,每次消耗NaOH溶液体积的平均值为13.00ml,则该胃药中CaCO3的质量分数为___.
▼优质解答
答案和解析
方案一:连通管X能使漏斗和广口瓶中的压强保持一致,保证盐酸顺利流下,
故答案为:使广口瓶内与分液漏斗内气体压强相等,便于溶液顺利流下;
方案二:(1)由于A、B是并列操作,不存在先后问题,故可以为ABDC或BADC;
滴定结束前,滴有酚酞的盐酸溶液为无色,当盐酸和氢氧化钠溶液完全反应后,溶液变成浅红色,则滴定终点的现象为:滴入最后一定溶液后,溶液由无色变为浅红色,且半分钟不褪色,
故答案为:ABDC或BADC;滴入最后一定溶液后,溶液由无色变为浅红色,且半分钟不褪色;
(2)因为每次滴定用的盐酸是25.00 mL,重复操作4次,再加上润洗滴定管、调零、赶气泡也需消耗盐酸,则所需盐酸大于100 mL,故配制时需用250 mL的容量瓶,定容时需要用胶头滴管,而加水稀释时也可以借助量筒来量水的量,所以需要的仪器为:CD或CDE,
故选:CD或CDE;
(3)①若用蒸馏水冲洗锥形瓶,对待测液和标准液都没有影响,所以不影响胃药中CaCO3含量,
故答案为:无影响;
②碱式滴定管用蒸馏水洗涤后,未用标准液润洗,导致滴定过程中消耗的标准液体积偏大,计算出的碳酸钙消耗的盐酸的量偏小,导致所测胃药中CaCO3含量偏低,
故答案为:偏低;
(4)反应所用盐酸与氢氧化钠溶液的浓度相等,氢氧化钠溶液的体积为13.00 mL,则与碳酸钙反应的盐酸为25.00mL-13.00 mL=12.00 mL,根据反应,CaCO3+2HCl=CaCl2+H2O+CO2↑可知,100g:2mol=m(CaCO3):0.100 mol/L×0.012L,解得:m=0.06 g,
碳酸钙的质量分数为:
×100%=60%,
故答案为:60%.
故答案为:使广口瓶内与分液漏斗内气体压强相等,便于溶液顺利流下;
方案二:(1)由于A、B是并列操作,不存在先后问题,故可以为ABDC或BADC;
滴定结束前,滴有酚酞的盐酸溶液为无色,当盐酸和氢氧化钠溶液完全反应后,溶液变成浅红色,则滴定终点的现象为:滴入最后一定溶液后,溶液由无色变为浅红色,且半分钟不褪色,
故答案为:ABDC或BADC;滴入最后一定溶液后,溶液由无色变为浅红色,且半分钟不褪色;
(2)因为每次滴定用的盐酸是25.00 mL,重复操作4次,再加上润洗滴定管、调零、赶气泡也需消耗盐酸,则所需盐酸大于100 mL,故配制时需用250 mL的容量瓶,定容时需要用胶头滴管,而加水稀释时也可以借助量筒来量水的量,所以需要的仪器为:CD或CDE,
故选:CD或CDE;
(3)①若用蒸馏水冲洗锥形瓶,对待测液和标准液都没有影响,所以不影响胃药中CaCO3含量,
故答案为:无影响;
②碱式滴定管用蒸馏水洗涤后,未用标准液润洗,导致滴定过程中消耗的标准液体积偏大,计算出的碳酸钙消耗的盐酸的量偏小,导致所测胃药中CaCO3含量偏低,
故答案为:偏低;
(4)反应所用盐酸与氢氧化钠溶液的浓度相等,氢氧化钠溶液的体积为13.00 mL,则与碳酸钙反应的盐酸为25.00mL-13.00 mL=12.00 mL,根据反应,CaCO3+2HCl=CaCl2+H2O+CO2↑可知,100g:2mol=m(CaCO3):0.100 mol/L×0.012L,解得:m=0.06 g,
碳酸钙的质量分数为:
| 0.06g |
| 0.1g |
故答案为:60%.
看了为测定某种胃药中CaCO3含量...的网友还看了以下:
六年级参加书法兴趣小组的同学是没有参加同学的3/7,后来又有30人参加书法兴趣小组,这时,参加书法 2020-04-27 …
化学兴趣小组设计实验,测定Na2CO3与NaHCO3混合物中Na2CO3的质量分数.甲方案:实验步 2020-06-26 …
突然对数学感兴趣了,高中学得不错,大学几乎没学,工作了也涉及数学很少,那么现在怎么发展这兴趣呢对数 2020-06-27 …
某化学兴趣小组的同学在配制1:2体积比的酒精溶液时,分工为:甲同学量取50mL酒精,乙同学量取10 2020-07-18 …
某学校各个年级数学兴趣小组中,有25名不是六年级学生,有26名不是五年级学生,五、六年级参加数学兴 2020-07-20 …
有关王国维全集亲们谁有新版的《王国维全集》王国维在《国学丛刊序》言:“居今日之世,讲今日之学,未有 2020-07-26 …
数学量词有哪些多些,完善点 2020-07-31 …
没学过大学力学课程可以自学量子力学吗本人大一新生,高中学的理科,自学过微积分,没学过大学的经典力学, 2020-11-04 …
“兴趣是最好的老师”.下面选项能体现这个道理的有()①有了学习兴趣,才能保持旺盛的求知欲②只要培养学 2020-11-14 …
差倍问题列方程解...学校展开学科兴趣小组活动,参加数学兴趣小组的同学比参加语文兴趣小组的人数多22 2020-11-20 …