早教吧作业答案频道 -->化学-->
某研究性学习小组将无水亚硫酸钠隔绝空气加热,并利用受热后的固体试样和如图所示的实验装置进行实验.已知:Na2SO3开始分解>600℃Na2S+Na2S4(反应
题目详情
某研究性学习小组将无水亚硫酸钠隔绝空气加热,并利用受热后的固体试样和如图所示的实验装置进行实验.已知:Na2SO3
Na2S+Na2S4(反应未配平).请回答下列问题:
Ⅰ、若某种固体物质受热发生了分解,下列说法正确的是___.
A.一定是氧化还原反应 B.反应后一定有气体生成
C.一定有多种物质生成 D.一定是吸热反应
Ⅱ、(1)在该实验中,如果加热温度低于600℃,向所得固体试样中缓缓滴加稀盐酸至足量,在滴加稀盐酸的整个过程中HSO3-的物质的量浓度变化趋势为___.
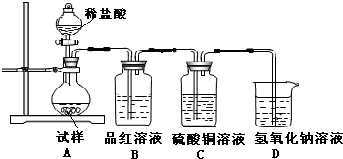
(2)如果加热温度为700℃,向所得固体试样中缓缓滴加稀盐酸至足量,观察到烧瓶中出现淡黄色沉淀,且有大量气泡产生,则固体试样跟盐酸反应生成淡黄色沉淀的离子方程式为___;此时在B、C两装置中可能观察到的现象为___.
(3)为检验分解产物中生成的SO42-离子,其操作方法、现象和结论是___.
(4)取上述受热后的固体试样进行分析,测得其中含硫元素的质量分数为25.39%,通过计算知该产物中氧元素的质量分数为___.
| 开始分解>600℃ |
| |

Ⅰ、若某种固体物质受热发生了分解,下列说法正确的是___.
A.一定是氧化还原反应 B.反应后一定有气体生成
C.一定有多种物质生成 D.一定是吸热反应
Ⅱ、(1)在该实验中,如果加热温度低于600℃,向所得固体试样中缓缓滴加稀盐酸至足量,在滴加稀盐酸的整个过程中HSO3-的物质的量浓度变化趋势为___.
(2)如果加热温度为700℃,向所得固体试样中缓缓滴加稀盐酸至足量,观察到烧瓶中出现淡黄色沉淀,且有大量气泡产生,则固体试样跟盐酸反应生成淡黄色沉淀的离子方程式为___;此时在B、C两装置中可能观察到的现象为___.
(3)为检验分解产物中生成的SO42-离子,其操作方法、现象和结论是___.
(4)取上述受热后的固体试样进行分析,测得其中含硫元素的质量分数为25.39%,通过计算知该产物中氧元素的质量分数为___.
▼优质解答
答案和解析
Ⅰ、某种固体物质受热发生了分解,一定生成多种物质,不一定是氧化还原反应,不一定有气体生成,不一定吸热,故选C;
Ⅱ、(1)由题意,Na2SO3要加热到600度以上才分解,因此题中加热温度600度以下冷却后得到的固体仍为Na2SO3,向所得固体试样中缓缓滴加稀盐酸至足量,首先HCl与SO32-反应生成HSO3-,加到一定程度时,SO32-已完全转化为HSO3-,再加盐酸,HSO3-与HCl反应生成SO2,所以HSO3-浓度先增大后将逐渐减小,直至最后下降到接近于零;
故答案为:先逐渐增大,后逐渐减小;
(2)如果加热温度为700℃,向所得固体试样中缓缓滴加稀盐酸至足量,观察到烧瓶中出现淡黄色沉淀为硫,且有大量气泡产生说明为二氧化硫,则固体试样跟盐酸反应生成淡黄色沉淀的离子方程式为:2S2-+SO32-+6H+=3S↓+3H2O;生成二氧化硫的反应为SO32-+2H+=SO2↑+H2O,此时在B、C两装置中可能观察到得现象为二氧化硫具有漂白作用使品红褪色,生成的气体不是硫化氢通过硫酸铜无现象,
故答案为:2S2-+SO32-+6H+=3S↓+3H2O;B中品红溶液褪色,C中无明显变化;
(3)要检验硫酸根离子的存在,先取固体试样溶于水配成溶液,取少量溶液于试管中,先加稀盐酸,若物明显现象,再加氯化钡溶液,若有白色沉淀生成,说明SO42-有存在;
故答案为:先取固体试样溶于水配成溶液,取少量溶液于试管中,先加稀盐酸,若物明显现象,再加氯化钡溶液,若有白色沉淀生成,说明SO42-有存在;
(4)受热后的固体试样中硫元素和氧元素的质量之比为32:(16×3)=2:3,硫元素的质量分数为25.39%,则氧元素的质量分数为
×3=38.09%;
故答案为:38.09%;
Ⅱ、(1)由题意,Na2SO3要加热到600度以上才分解,因此题中加热温度600度以下冷却后得到的固体仍为Na2SO3,向所得固体试样中缓缓滴加稀盐酸至足量,首先HCl与SO32-反应生成HSO3-,加到一定程度时,SO32-已完全转化为HSO3-,再加盐酸,HSO3-与HCl反应生成SO2,所以HSO3-浓度先增大后将逐渐减小,直至最后下降到接近于零;
故答案为:先逐渐增大,后逐渐减小;
(2)如果加热温度为700℃,向所得固体试样中缓缓滴加稀盐酸至足量,观察到烧瓶中出现淡黄色沉淀为硫,且有大量气泡产生说明为二氧化硫,则固体试样跟盐酸反应生成淡黄色沉淀的离子方程式为:2S2-+SO32-+6H+=3S↓+3H2O;生成二氧化硫的反应为SO32-+2H+=SO2↑+H2O,此时在B、C两装置中可能观察到得现象为二氧化硫具有漂白作用使品红褪色,生成的气体不是硫化氢通过硫酸铜无现象,
故答案为:2S2-+SO32-+6H+=3S↓+3H2O;B中品红溶液褪色,C中无明显变化;
(3)要检验硫酸根离子的存在,先取固体试样溶于水配成溶液,取少量溶液于试管中,先加稀盐酸,若物明显现象,再加氯化钡溶液,若有白色沉淀生成,说明SO42-有存在;
故答案为:先取固体试样溶于水配成溶液,取少量溶液于试管中,先加稀盐酸,若物明显现象,再加氯化钡溶液,若有白色沉淀生成,说明SO42-有存在;
(4)受热后的固体试样中硫元素和氧元素的质量之比为32:(16×3)=2:3,硫元素的质量分数为25.39%,则氧元素的质量分数为
| 25.39% |
| 2 |
故答案为:38.09%;
看了某研究性学习小组将无水亚硫酸钠...的网友还看了以下:
童装厂加工一批童装,原计划每天加工45套,4天完成.实际3天完成了任务,实际每天比计划多加工多少套 2020-04-26 …
实验小学新近一批电脑,原计划每天装配30台,4天完成任务.实际每天比原计划多装配1/3,照这样计算 2020-05-20 …
建筑材料题经测定,质量为3.4千克,容积为10.0升的容量筒装满绝干石子后的总重量为18.4千克建 2020-06-25 …
质量为3.4kg,容积为10l的容量筒装满绝干石子后的总质量为18.4kg.若向筒内注入水容积为1 2020-06-25 …
如图甲所示,在观察水的沸腾实验中.(1)在组装实验装置时,图乙中温度计放置正确的是.(2)如图丙是 2020-07-10 …
下表所示为两国生产1单位对应商品必须投入的劳动时间小麦服装美国3小时9小时英国4小时4小时a.哪个 2020-07-22 …
请高手来答.有三个直径相同的金属小球.小球1和2带等量同号电荷,两者的距离远大于小球直径,相互作用 2020-07-30 …
一道物理题请高手来回答.有三个直径相同的金属小球.小球1和2带等量同号电荷,两者的距离远大于小球直 2020-07-30 …
装订一批儿童课外读物,计划每天装订180本,40天可装订完,实际3天就装订了720本,照这样计算,多 2020-11-05 …
(2014•十堰)如图是初中化学中几个重要实验,有关该几个实验的说法错误的是()A.实验1中热水的作 2020-11-12 …