光气(COCl2)在塑料、制革、制药等工业中有许多用途,工业上采用高温下CO与Cl2在活性炭催化下合成。COCl2的分解反应为COCl2(g)Cl2(g)+CO(g)△H=+108KJ·mol-1。反应体系达
光气(COCl 2 )在塑料、制革、制药等工业中有许多用途,工业上采用高温下CO与Cl 2 在活性炭催化下合成。
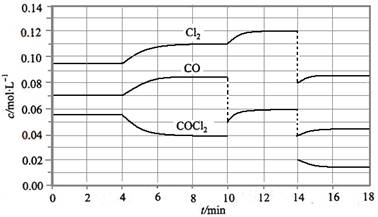
COCl 2 的分解反应为COCl 2 (g) 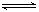 Cl 2 (g) + CO(g) △H = + 108 KJ·mol -1 。反应体系达到平衡后,各物质的浓度在不同条件下的变化状况如下图所示(第10 min到14 min的COCl 2 浓度变化曲线未画出):
Cl 2 (g) + CO(g) △H = + 108 KJ·mol -1 。反应体系达到平衡后,各物质的浓度在不同条件下的变化状况如下图所示(第10 min到14 min的COCl 2 浓度变化曲线未画出):
(1) 计算反应在第8 min 时的平衡常数K = ;
(2) 比较第2 min 反应温度T(2)与第8 min反应温度T(8)的高低:T(2) T(8)(填“<”、“>”或“=”);
(3) 若12 min 时反应于温度T(8)下重新达到平衡,则此时c(COCl 2 ) = mol·l -1 ;
(4) 比较产物CO在2~3 min、5~6 min和12~13 min时平均反应速率[平均反应速率分别以v(2~3)、v(5~6)、v(12~13)表示]的大小 ;
(5)比较反应物COCl 2 在5~6 min和15~16 min时平均反应速率的大小v(5~6) v(12~13) (填“<”、“>”或“=”),原因是 。
(1)根据图像可知,反应在第8 min 时光气、CO和氯气的平衡浓度分别是(mol/L)0.04、0.085、0.11,所以此时平衡常数K=。 (2)反应在第2 min 时光气、CO和氯气的平衡浓度分别是(mol/L)0.055、0.07、0.095,所以此时平衡常数K=<0.234。K值很明显小于T(8)时的K值,由于正反应是吸热反应,所以T(2)小于T(8),即升高温度平衡向正反应方向进行,平衡常数增大。 (3)由于题目说了是不同条件下的平衡状态,那么后面温度就不会改变,所以K值不变。此时CO和氯气的浓度分别是0.06mol/L和0.12mol/L,所以c(COCl2)==0.031molL。 (4)因为5-6分钟,CO浓度在改变所以平均反应速率大于其它的,因为处于平衡状态,根据V的计算公式,2-3、12-13的平均反应速率为0,即v(5-6)>v(2-3)=v(12-13)。 (5)因为随着反应的进行,反应物的浓度是逐渐降低的。由于在相同温度时,反应的反应物浓度越高,反应速率越大,所以5-6分钟时浓度改变大于12-13时浓度的改变。
一根轻质弹簧,当它上端固定,下端挂一重力为G的物体时,长度为L1;当它下端固定在水平面上,上端压一 2020-04-05 …
悬挂一物体P,绳的拉力为F,物体的重力为G,则下列说法正确的是()A,F与G大小相等,且方向相反. 2020-05-21 …
物理帝帮帮忙,自由落体的完全失重和航空中的完全失重一样吗?为什么一个是往下掉,一个是飘浮在那?不都 2020-06-07 …
有没有G物=G排液这一说法?因为F浮=P液gV排=G排液又因为当物体漂浮或悬浮时,F浮=G物.那么 2020-06-20 …
写出下列实验情况产生的原因:做木炭在氧气中燃烧的实验时,木炭伸入集气瓶后很快熄灭.原因:一开始就将 2020-07-06 …
据《汉书》记载,“豫章郡出石,可燃为薪”,我国人民很早就懂得用煤炭作为燃料。现在煤炭不仅是重要的动 2020-07-29 …
N2O4(g)易发生分解:N2O4(g)=2NO2(g).实验测得100kPa下,333K达到平衡时 2020-11-03 …
(2008•漳州)(1)现有一瓶500mL医用的生理盐水(NaCl的质量分数为0.9%,溶液的密度约 2020-11-12 …
关于失重有些问题求解答.1,绕地球作匀速圆周运动的航天器为什么加速度向下为g?它并没有向下运动.2. 2020-12-02 …
本题中用大写字母代表原子核,E经α衰变成为F,再经β衰变成为G,再经α衰变成为H.上述系列衰变可记为 2021-01-08 …