空气中的SO2含量和可吸入颗粒的含量(可用g/cm3表示)都是重要的空气质量指标。在工业生产上规定:空气中二氧化硫的最大允许排放浓度不得超过0.02mg/L。《2004年江苏省环境状况公
空气中的SO 2 含量和可吸入颗粒的含量(可用g/cm3表示)都是重要的空气质量指标。在工业生产上规定:空气中二氧化硫的最大允许排放浓度不得超过0.02 mg/L。《2004年江苏省环境状况公报》指出:江苏省2004年工业(主要是热电厂)二氧化硫排放总量为1.24×10 6 t,全省酸雨污染比较严重。分析降雨成分发现,雨水中阴离子仍以硫酸根离子为主,约占阴离子总量的61.9%。
(一)(1)正常的雨水显 性(填:酸、碱、或中),原因是 ;
(2)由于大气中SO 2 和NOx(NO和NO 2 )的含量不断升高,并转变为H 2 SO 4 型和HNO 3 型雨水降落而形成的。我省主要是硫酸型酸雨。我省这种酸雨形成过程有两种途径:一种是SO 2 在空气中的飘尘做催化剂的作用下被氧气氧化为SO 3 ,溶于水生成硫酸,写出有关的反应化学方程式 、 ;
另一种是SO 2 溶于水生成亚硫酸,再被空气中的氧气氧化成硫酸,写出有关的反应化学方程式 、 。由于SO 2 的氧化非常缓慢,故后一种途径是其主要形成过程。
(3)兴趣小组同学取刚降到热电厂附近的雨水进行测定,每隔五分钟测一次pH,其数据如下表所示:
| 测定时刻 | 5∶05 | 5∶10 | 5∶15 | 5∶20 | 5∶25 | 5∶30 | 5∶35 |
| pH | 4.95 | 4.94 | 4.94 | 4.88 | 4.86 | 4.85 | 4.85 |
分析上述数据变化,你可以得出的结论是 ;针对此结论,你猜测其中的原因为 。结合大理石被酸雨腐蚀的事实,你认为碳酸、硫酸、亚硫酸酸性由强到弱的顺序为__________________________。
(二)SO 2 气体能使品红溶液、高锰酸钾溶液褪色。
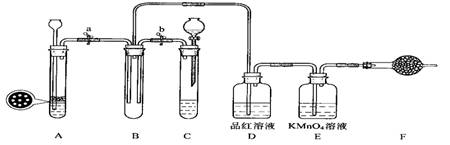
回答以下问题:
(1)单独检查装置C的气密性的操作是:关闭活塞b,然后________________________ ,
若发现________________,说明装置C气密性良好。
(2)实验室用Na 2 SO 3 固体和硫酸溶液制取SO 2 气体,应选用__________(选“A”或“C”)做气体发生装置,不选用另一装置的理由是 。
(3)小组的同学在A、C装置中的另一个用块状FeS固体和稀硫酸制取H 2 S气体,反应的方程式为_________________ 。
(4)SO 2 气体通过D装置时现象是____________________ ,通过E装置时现象是________________ ;SO 2 与H 2 S在B装置中反应,生成一种氧化物和一种单质,反应的方程式是 。
(5)F仪器的名称是___________;F中盛有NaOH固体,作用是
(三)⑴为测定某地方的空气中SO 2 和可吸入颗粒的含量,查阅资料得知:可用含有一定量碘的溶液测定空气中的SO 2 含量,反应方程式是:SO 2 +I 2 +2H 2 O=H 2 SO 4 +2HI。甲同学设计了如下图所示的实验装置:

①应用上述装置测定空气中的SO 2 含量和可吸入颗粒的含量,除测定气体流速(单位:cm 3 /min)外,还需要测定吸收前后颗粒吸附剂、棉花、盛放容器的总质量和 。
②已知:碘单质微溶于水,KI可以增大碘在水中的溶解度。
请你协助甲同学完成稀碘溶液的配制:
第一步:准确称取1.27g碘单质加入烧杯中, ;
第二步:加适量水使之完全溶解,然后加水至溶液体积为1000 mL;
第三步:从第二步所得溶液中,取出10.00mL溶液加入稀释至100mL。
⑵乙同学拟用下列简易装置测定空气中的SO 2 含量:准确取50mL第三步所得的碘溶液,注入右图所示广口瓶中,加2~3滴淀粉指示剂,此时溶液呈蓝色。在指定的测定地点抽气,每次抽气100mL,直到溶液的蓝色全部褪尽为止,记录抽气次数( n )。
假设乙同学的测量是准确的,乙同学抽气的次数为80次,计算说明该地空气中的SO 2 含量是否符合排放标准。(写出解题过程,此题3分)

⑶该小组同学认为这些工厂要对排出的废气进行处理,为了达到最好效果,在实验室进行了实验模拟,你认为他们为了吸收产生的SO 2 气体,所使用药品应该是________,发生的化学反应方程式______________________________________
经过再三思考,设计了以下装置,认为下列哪种不能采用______ 因为其他装置都具有________作用。

A B C D E F G H I J
质量相同的下列物质熔化热最大的是()A.铝在熔化过程中吸收了395.7kJ能量B.铜在熔化过程中吸 2020-04-07 …
下列气体的干燥和吸收方法正确的是()A.氨气可以用五氧化二磷干燥B.氮气和氢气反应合成氨气由于反应 2020-05-12 …
化学中吸入2少一多和呼出两多一少指什么 2020-05-14 …
2008年9月19日,胡锦涛在学习实践科学发展观活动动员大会发表重要讲话。他强调,适应新形势,完成 2020-05-15 …
为什么用氢氧化钠吸收二氧化碳,而用澄清石灰水检验二氧化碳?有人说:氢氧化钠的溶解度大所以用于吸收, 2020-05-16 …
氨法吸收二氧化碳中如何将吸收的二氧化碳解吸我要用解吸出来的二氧化碳做一种化工产品 2020-05-20 …
在运输食品的过程中,常用干冰作为冷却剂,这是因为A.干冰熔化时可吸热B.干冰升华时可以吸热C.干冰 2020-06-14 …
求问呼吸作用中吸进的氧气最终被氧化成水形成尿排出体外么? 2020-06-22 …
吸解的定义在化学中,吸解是什么意思?以及吸附的定义! 2020-07-15 …
下列叙述中正确的有:A.绿色植物通过细胞呼吸合成的ATP通常比同化作用中消耗的ATP少,动物细胞呼吸 2020-11-05 …