某工厂排出的废液中含有CuSO4、ZnSO4、FeSO4三种物质,如果将废液直接排放就会造成下水道水污染。于是同学们利用课余处理废液,回收工业重要原料硫酸锌和有关金属
某工厂排出的废液中含有 CuSO 4 、 ZnSO 4 、 FeSO 4 三种物质,如果将废液直接排放就会造成下水道水污染。于是同学们利用课余处理废液,回收工业重要原料硫酸锌和有关金属。实验过程如下:
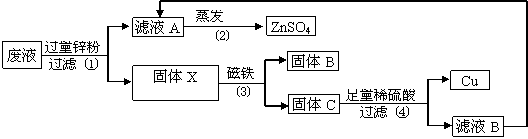
请回答:
( 1 )固体 X 是 ;固体 B 的化学式为 ,
滤液 A 的溶质是 ( 名称)
( 2 ) 写出步骤 ① 其中一个反应的化学方程式 ;
步骤 ④ 发生反应的化学方程式为 。
( 3 )要检验步骤 ④ 中加入的稀硫酸是否足量的方法是 。
( 4 ) 已知 废液的 质量为 m 1 g ,完全反应后剩余固体 B 质量为 m 2 g , 废液中硫酸锌 ZnSO 4 的质量为 m 3 g ,锌粉的质量为 m 4 g 。 若实验过程中的物质损失可以忽略,要计算该废液中硫酸锌的质量分数,必须称量:废液的质量和 。 (填字母)
A . m 2 g 、 m 3 g B . m 4 g 、 m 3 g C . m 2 g 、 m 4 g D . m 2 g 、 m 3 g 、 m 4 g
英语翻译各位大神帮忙把以下汉语翻译成英文工作平台制作工艺说明总图支撑架支撑架制作工艺1下料:将40 2020-04-26 …
一篇英文的接替工作的介绍急求一篇英文的介绍,大概内容是,JACK已经离开本公司。我将接替他的工作, 2020-05-17 …
回答下列有关微生物的问题.如图1显示微生物的接种实验中的一些步骤.(1)图中的接种工具的名称是.( 2020-05-17 …
(2013•虹口区二模)回答下列有关微生物的问题.如图1显示微生物的接种实验中的一些步骤.(1)图 2020-05-17 …
()是接待工作中的三个基本环节,A.迎客B.见客C.待客D.送客 2020-05-31 …
工作表的冻结是指将工作表窗口的()固定性,不随滚动条移动。 2020-05-31 …
对溺水者抢救的下列叙述中正确的是()A.直接人工呼吸时用最大力气按压胸部B.直接对溺水者的口吹气C 2020-06-28 …
对溺水者抢救的下列叙述中正确的是()A.直接人工呼吸时用最大力气按压胸部B.直接对溺水者的口吹气C 2020-06-28 …
公路工程中桥涵的水下挖土方是指什么?是指墩柱施工时接桩而开挖的水下土方?还是需将河床整体挖至标高? 2020-06-29 …
a4A2034将0.1H的电感线圈接在工频220V交流电源上,则通过线圈的电流为().(A)220 2020-07-09 …