25℃时,向盛有50mLpH=2的一元酸HA溶液的绝热容器中加入pH=13的NaOH溶液,加入NaOH溶液的体积(V)与所得混合溶液的温度(T)的关系如图所示.下列叙述正确的是()A.25℃时,HA的电离平
25℃时,向盛有50mLpH=2的一元酸HA溶液的绝热容器中加入pH=13的NaOH溶液,加入NaOH溶液的体积(V)与所得混合溶液的温度(T)的关系如图所示.下列叙述正确的是( )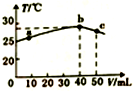
A. 25℃时,HA的电离平衡常数Ka约为1.43×10-3
B. a→b的过程中,溶液中c(A-)与c(HA)之和始终不变
C. b→c的过程中,温度降低的主要原因是溶液中发生了吸热反应
D. 等浓度的NaOH和NaA混合溶液中一定存在关系:c(Na+)>c(A-)>c(OH-)>c(H+)
| c(H+)c(A-) |
| c(HA) |
| 0.01mol/L×0.01mol/L |
| 0.08mol/L-0.01mol/L |
B.当酸碱中和恰好完全时,溶液中的溶质为NaA,根据物料守恒c(A-)+c(HA)=c(Na+),若酸过量或碱过量时不再相等,故B错误;
C.b→c的过程中,温度降低的原因是溶液中发生了反应恰好生成NaA,继续滴加氢氧化钠溶液不再发生反应,溶液温度降低,故C错误;
D.根据物料守恒,等浓度的NaOH和NaA混合溶液中c(Na+)>c(OH-)>c(A-)>c(H+),故D错误.
故选A.
一道对数函数的题很简单的帮忙已知alog₄5=1(1)求5a次方+5-a次方(2)求使不等式a的2x 2020-03-30 …
有哪一个英文单词,或者任何一种外语含有a,h,a的单词,求回复希望有3个单词每个单词的开头首字母是 2020-04-06 …
未知数的右下角有数字我看好像是次方,如果知道是什么一并回答,a的n次方=a的1次方+(n-1)乘d 2020-05-13 …
计算:-a的5次方*(-a)³+(-a)²*a的6次方. 2020-05-15 …
幂的乘方化简(送分)!1.(0.75A)的立方*(0.25A)的4次方.2.若x的3n次方=5,y 2020-06-02 …
比a的5倍少7的数是().比x小4的数与a相乘的积是()买3千克黄瓜用了a元,a÷3表示()王老师 2020-06-02 …
()的4倍是3分之2.3,甲数的5分之1和乙数的6分之1相等,甲数是30,乙数是().()的4倍是 2020-06-06 …
已知a,b,c,d均为正数,且a5=5,b4=4,c3=3,d2=2,试比较a,b,c,d的大小是 2020-06-12 …
a^5-1(a的5次方减1)因式分解a^5-1(a的5次方减1)如何因式分解 2020-06-20 …
不过水平有限,看不懂英文题目.1.factor the following completely: 2020-06-27 …