早教吧作业答案频道 -->化学-->
工业上用硅石为原料,制备高纯多晶硅的流程如下:有关性质如下表:物质熔点/℃沸点/℃其他SiHCl3-126.5℃33.0易与水强烈反应,空气中易自然SiCl4-7057.6易
题目详情
工业上用硅石为原料,制备高纯多晶硅的流程如下:
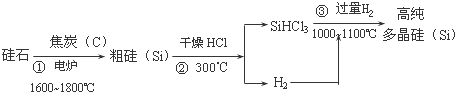
有关性质如下表:
(1)制备粗硅的化学反应方程式为___;硅的一种重要用途是___.
(2)第②步经冷凝得到的SiHCl3中含有少量SiCl4和HCl,提纯SiHCl3采用的方法是___;尾气中含有少量SiCl4和HCl,可通过___溶液除去.
(3)实验室用SiHCl3与过量H2反应制备纯硅的装置如下(热源及夹持装置略去):
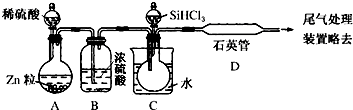
①需要加热的装置有___(填序号);如无装置B则C中能发生的副反应方程式是___.
②制备实验操作成功的关键是检查实验装置的气密性,控制好反应温度以及实验开始时先___;反应一段时间后,装置D中观察到的现象是___.
(4)粗硅中一般含有微量铁、铝、碳、硼、磷、铜等杂质,为鉴定硅中是否含铁,将试样用稀盐酸溶解,取上层清液后加入的最佳试剂是:___(填写字母代号).
a.碘水 b.氯水 c.NaOH溶液 d.KSCN溶液 e.Na2SO3溶液.

有关性质如下表:
| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
| SiHCl3 | -126.5℃ | 33.0 | 易与水强烈反应,空气中易自然 |
| SiCl4 | -70 | 57.6 | 易水解 |
| HCl | -114.2 | -84.7 |
(2)第②步经冷凝得到的SiHCl3中含有少量SiCl4和HCl,提纯SiHCl3采用的方法是___;尾气中含有少量SiCl4和HCl,可通过___溶液除去.
(3)实验室用SiHCl3与过量H2反应制备纯硅的装置如下(热源及夹持装置略去):

①需要加热的装置有___(填序号);如无装置B则C中能发生的副反应方程式是___.
②制备实验操作成功的关键是检查实验装置的气密性,控制好反应温度以及实验开始时先___;反应一段时间后,装置D中观察到的现象是___.
(4)粗硅中一般含有微量铁、铝、碳、硼、磷、铜等杂质,为鉴定硅中是否含铁,将试样用稀盐酸溶解,取上层清液后加入的最佳试剂是:___(填写字母代号).
a.碘水 b.氯水 c.NaOH溶液 d.KSCN溶液 e.Na2SO3溶液.
▼优质解答
答案和解析
在高温条件下,C和硅石发生置换反应生成Si,反应方程式为SiO2+2C
Si+2CO↑;得到的粗硅用干燥的氯化氢在加热条件下发生反应,反应方程式为Si+3HCl
SiHCl3+H2,然后在高温条件下将SiHCl3和过量氢气发生还原反应,反应方程式为SiHCl3+H2
Si+3HCl,从而得到纯硅;
(1)高温条件下,硅和C发生置换反应生成Si,反应方程式为;Si能作半导体材料(制造晶体管、集成电路)(硅整流器和太阳能电池)(变压器铁芯)等,
故答案为:SiO2+2C
Si+2CO↑;半导体材料(制造晶体管、集成电路)(硅整流器和太阳能电池)(变压器铁芯)等;
(2)第②步经冷凝得到的SiHCl3中含有少量SiCl4和HCl,SiHCl3易与水强烈反应,空气中易自然,四氯化硅易水解,所以应该采用蒸馏方法分离提纯;SiCl4和HCl能和NaOH溶液反应而用NaOH溶液除去,所以用NaOH处理尾气,故答案为:蒸馏;NaOH(碱);
(3)稀硫酸和Zn反应生成氢气,该反应是放热反应,所以生成的氢气中含有水蒸气,SiHCl3易与水强烈反应,为了防止SiHCl3与水反应,通入C中的氢气应该用浓硫酸干燥,所以浓硫酸的作用是作干燥剂;加热C装置能SiHCl3转化为蒸气,且氢气和SiHCl3充分混合,则D装置中SiHCl3和氢气发生置换反应生成单质Si,尾气中含有HCl等气体,用碱液吸收;
①C装置加热时分液漏斗中的液体转化为气体;D装置加热使SiHCl3和氢气发生置换反应生成单质Si,所以需要加热的装置是CD;
SiHCl3易和水发生水解反应,如果没有B装置,生成的氢气中含有水蒸气,发生的反应为SiHCl3+3H2O═H2SiO3+H2↑+3HCl;
故答案为:CD;SiHCl3+3H2O═H2SiO3+H2↑+3HCl;
②氢气属于易燃气体,和氧气混合在加热条件下易产生爆炸,所以实验开始前应该通一段时间H2,将装置中的空气排尽;
装置加热使SiHCl3和氢气发生置换反应生成单质Si,所以D中看到的现象是有固体物质生成(石英管的内壁附有灰黑色晶体);
故答案为:通一段时间H2,将装置中的空气排尽;有固体物质生成(石英管的内壁附有灰黑色晶体);
(4)铁与盐酸反应产生Fe2+,其检验方法常采用先将Fe2+氧化为Fe3+然后再加入KSCN溶液看是否变红来检验,故选bd.
| ||
| ||
| ||
(1)高温条件下,硅和C发生置换反应生成Si,反应方程式为;Si能作半导体材料(制造晶体管、集成电路)(硅整流器和太阳能电池)(变压器铁芯)等,
故答案为:SiO2+2C
| ||
(2)第②步经冷凝得到的SiHCl3中含有少量SiCl4和HCl,SiHCl3易与水强烈反应,空气中易自然,四氯化硅易水解,所以应该采用蒸馏方法分离提纯;SiCl4和HCl能和NaOH溶液反应而用NaOH溶液除去,所以用NaOH处理尾气,故答案为:蒸馏;NaOH(碱);
(3)稀硫酸和Zn反应生成氢气,该反应是放热反应,所以生成的氢气中含有水蒸气,SiHCl3易与水强烈反应,为了防止SiHCl3与水反应,通入C中的氢气应该用浓硫酸干燥,所以浓硫酸的作用是作干燥剂;加热C装置能SiHCl3转化为蒸气,且氢气和SiHCl3充分混合,则D装置中SiHCl3和氢气发生置换反应生成单质Si,尾气中含有HCl等气体,用碱液吸收;
①C装置加热时分液漏斗中的液体转化为气体;D装置加热使SiHCl3和氢气发生置换反应生成单质Si,所以需要加热的装置是CD;
SiHCl3易和水发生水解反应,如果没有B装置,生成的氢气中含有水蒸气,发生的反应为SiHCl3+3H2O═H2SiO3+H2↑+3HCl;
故答案为:CD;SiHCl3+3H2O═H2SiO3+H2↑+3HCl;
②氢气属于易燃气体,和氧气混合在加热条件下易产生爆炸,所以实验开始前应该通一段时间H2,将装置中的空气排尽;
装置加热使SiHCl3和氢气发生置换反应生成单质Si,所以D中看到的现象是有固体物质生成(石英管的内壁附有灰黑色晶体);
故答案为:通一段时间H2,将装置中的空气排尽;有固体物质生成(石英管的内壁附有灰黑色晶体);
(4)铁与盐酸反应产生Fe2+,其检验方法常采用先将Fe2+氧化为Fe3+然后再加入KSCN溶液看是否变红来检验,故选bd.
看了工业上用硅石为原料,制备高纯多...的网友还看了以下:
近年来,有科学家提出硅是“21世纪的能源”、“未来的石油”的观点.假如硅作为一种普遍使用的新型能源 2020-05-14 …
把高岭石的化学式写成氧化物的形式怎么写?谢谢!用氧化物的形式表示下列硅酸盐的组成:(如硅酸钠Na2 2020-05-16 …
PHP做距离星期一还有几天?上面中的:date("l",$week)="Monday";中"l"是 2020-05-16 …
据《参考消息》报道,有科学家提出硅是“21世纪的能源”、“未来的石油”的观点.假如硅作为一种普遍使 2020-06-18 …
有科学家提出硅是“21世纪的能源”、“未来的石油”的观点。假如硅作为一种普遍使用的新型能源被开发利 2020-07-06 …
某品牌矿泉水的标签上标明的矿泉水主要成分如下表所示,请根据本表回答下列问题水质主要成分(mg/L) 2020-07-18 …
硅是“21世纪的能源”.假如硅作为一种普遍使用的新型能源被开发利用,下列说法中,你认为不妥的是() 2020-07-29 …
硅烷化是一个什么化学反应?就是我们修补金属.瓷.等表面要用一个硅烷化的处理.这个反应是怎么个反应.如 2020-11-21 …
硅是一种半导体材料,可用于制作半导体器件和集成电路.还可以合金的形式使用(如硅铁合金),用于汽车和机 2020-12-07 …
据报导,有科学家提出硅是“21世纪的能源”、“未来的石油”的观点.假如硅作为一种普通使用的新型能源被 2021-01-13 …