早教吧作业答案频道 -->化学-->
汽车尾气中CO、NOx以及燃煤废气中的SO2都是大气污染物,对它们的治理具有重要意义.(1)氧化一还原法消除NOx的转化如下:NOO2反应ⅠNO2C
题目详情
汽车尾气中CO、NOx以及燃煤废气中的SO2都是大气污染物,对它们的治理具有重要意义.
(1)氧化一还原法消除NOx的转化如下:NO
NO2
N2
①反应I为NO+O3=NO2+O2,生成标准状况下11.2L O2时,转移电子的物质的量是___mol.
②反应Ⅱ中,当n( NO2):n[CO(NH2)2]=3:2时,氧化产物与还原产物的质量比为___
(2)使用“催化转化器”可以减少尾气中的CO和NOx,转化过程中发生反应的化学方程式为:
CO+NO→N2+CO2(未配平),若x=1.5,则化学方程式中CO2和N2的化学计量数比为___.
(3)吸收SO2和NO,获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素).装置Ⅱ中,酸性条件下,NO被Ce4+氧化的产物主要是NO3-、NO2-,请写出生成等物质的量的NO3-和NO2-时的离子方程式___.
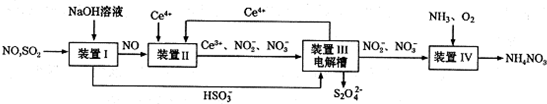
(4)装置Ⅲ的作用之一是用质子交换膜电解槽电解使得Ce4+再生,再生时生成的Ce4+在电解槽的___(填“阳极”或“阴极”),同时在另一极生成S2O42一的电极反应式为___.
(5)已知进入装置Ⅳ的溶液中,NO2-的浓度为ag.L-1,要使1m3该溶液中的NO2-完全转化为NH4NO3,至少需向装置Ⅳ中通人标准状况下的氧气___L(用含a代数式表示,结果保留整数).
(1)氧化一还原法消除NOx的转化如下:NO
| O2 |
| |
| 反应Ⅰ |
| CO(NH2)2 |
| |
| 反应Ⅱ |
①反应I为NO+O3=NO2+O2,生成标准状况下11.2L O2时,转移电子的物质的量是___mol.
②反应Ⅱ中,当n( NO2):n[CO(NH2)2]=3:2时,氧化产物与还原产物的质量比为___
(2)使用“催化转化器”可以减少尾气中的CO和NOx,转化过程中发生反应的化学方程式为:
CO+NO→N2+CO2(未配平),若x=1.5,则化学方程式中CO2和N2的化学计量数比为___.
(3)吸收SO2和NO,获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素).装置Ⅱ中,酸性条件下,NO被Ce4+氧化的产物主要是NO3-、NO2-,请写出生成等物质的量的NO3-和NO2-时的离子方程式___.

(4)装置Ⅲ的作用之一是用质子交换膜电解槽电解使得Ce4+再生,再生时生成的Ce4+在电解槽的___(填“阳极”或“阴极”),同时在另一极生成S2O42一的电极反应式为___.
(5)已知进入装置Ⅳ的溶液中,NO2-的浓度为ag.L-1,要使1m3该溶液中的NO2-完全转化为NH4NO3,至少需向装置Ⅳ中通人标准状况下的氧气___L(用含a代数式表示,结果保留整数).
▼优质解答
答案和解析
解(1)①NO+O3═NO2+O2,生成1mol氧气转移电子是2mol,生成11.2L即0.5mol O2(标准状况)时,转移电子的物质的量是0.5mol×2=1mol,故答案为:1;
②当n(NO2):n[CO(NH2)2]=3:2,即NO2和CO(NH2)2的系数之比是3:2,其方程式表示为:6NO2+4CO(NH2)2=7N2+8H2O+4CO2,只有N元素的化合价变化,氮气为氧化产物也是还原产物,由N原子守恒可知氧化产物与还原产物的质量比为8:6=4:3,故答案为:4:3;
(2)转换过程中发生反应的化学方程式为:CO+NOx→CO2+N2(未配平),若x=1.5,可利用“定一法”进行配平,把CO2的化学计量数定为1,则CO、NO1.5、N2前面的化学计量数分别为:1、
、
.即3CO+2NO1.5→3CO2+N2,则化学方程式中CO2与N2的系数之比为3:1,故答案为:3:1;
(3)生成等物质的量的NO3-和NO2-时,Ce4+被还原为Ce3+,由电子守恒、电荷守恒可知,离子方程式为:2NO+3H2O+4Ce4+=4Ce3++NO3-+NO2-+6H+,
故答案为:2NO+3H2O+4Ce4+=4Ce3++NO3-+NO2-+6H+;
(4)生成Ce4+为氧化反应,发生在阳极上,连接电源正极,因此再生时生成的Ce4+在电解槽的阳极;反应物是HSO3-被还原成S2O42-,得到电子,电极反应式为:2HSO3-+2H++2e-=S2O42-+2H2O,故答案为:阳极;2HSO3-+2H++2e-=S2O42-+2H2O;
(5)NO2-的浓度为a g•L-1,要使1m3该溶液中的NO2-完全转化为NH4NO3,则失去电子数目是:1000×(5-3)a/46,设消耗标况下氧气的体积是V,则失电子数目是:
×2×(2-0),根据电子守恒:
=
×2×(2-0),解得V=243a,故答案为:243a.
②当n(NO2):n[CO(NH2)2]=3:2,即NO2和CO(NH2)2的系数之比是3:2,其方程式表示为:6NO2+4CO(NH2)2=7N2+8H2O+4CO2,只有N元素的化合价变化,氮气为氧化产物也是还原产物,由N原子守恒可知氧化产物与还原产物的质量比为8:6=4:3,故答案为:4:3;
(2)转换过程中发生反应的化学方程式为:CO+NOx→CO2+N2(未配平),若x=1.5,可利用“定一法”进行配平,把CO2的化学计量数定为1,则CO、NO1.5、N2前面的化学计量数分别为:1、
| 2 |
| 3 |
| 1 |
| 3 |
(3)生成等物质的量的NO3-和NO2-时,Ce4+被还原为Ce3+,由电子守恒、电荷守恒可知,离子方程式为:2NO+3H2O+4Ce4+=4Ce3++NO3-+NO2-+6H+,
故答案为:2NO+3H2O+4Ce4+=4Ce3++NO3-+NO2-+6H+;
(4)生成Ce4+为氧化反应,发生在阳极上,连接电源正极,因此再生时生成的Ce4+在电解槽的阳极;反应物是HSO3-被还原成S2O42-,得到电子,电极反应式为:2HSO3-+2H++2e-=S2O42-+2H2O,故答案为:阳极;2HSO3-+2H++2e-=S2O42-+2H2O;
(5)NO2-的浓度为a g•L-1,要使1m3该溶液中的NO2-完全转化为NH4NO3,则失去电子数目是:1000×(5-3)a/46,设消耗标况下氧气的体积是V,则失电子数目是:
| V |
| 22.4 |
| 1000a×(5-3) |
| 46 |
| V |
| 22.4 |
看了汽车尾气中CO、NOx以及燃煤...的网友还看了以下:
二氧化塔排放空中属不属于二次污染?一氧化氮,二氧化氮?急那属不属于二次污染? 2020-03-30 …
物质的结构决定物质的性质,物质的性质决定物质的用途.下列叙述正确的是()A.木炭疏松多孔,所以具有 2020-05-13 …
对下列事实的解释不正确的是()事实解释A汽油除可用于去除衣服上的油污汽油能溶解油污B洗洁精可用于去 2020-05-13 …
衣服油污汽油衣服上沾有油污,用水不易洗去,在油污上倒些汽油,油污就容易洗去,这个现象说明了什么,为 2020-06-07 …
以下哪些气体分别在日间和夜间经由植物叶片的气孔离开的?()选项日间夜间A二氧化碳二氧化碳和水汽B氧 2020-06-16 …
低层大气中吸收地面辐射的主要是A水汽和氧气B氮气和水汽C二氧化碳和水汽D氧气和氮气 2020-07-10 …
下列每组的说法都正确的是()A、油污的洗涤原理B、实验现象①用洗洁精洗是乳化油污②用汽油洗是溶解油污 2020-11-05 …
关于污水需氧量的问题《室外给水设计规范GB50013-2006》6.8.2生物反应池中好氧区的污水需 2020-12-01 …
关于废水处理工艺的一些问题操作规程里面写着“曝气池的运行每隔一段时间检查污泥量,如果每1000ML污 2020-12-01 …
下列物质的用途与性质对应不正确的是()选项物质用途性质A洗涤剂清洗油污洗涤剂能溶解油污B一氧化碳作燃 2021-02-19 …