早教吧作业答案频道 -->化学-->
漂白粉的主要成分为次氯酸钙[Ca(ClO)2]和氯化钙,即可用作漂白剂,又可用作消毒剂.漂白粉中有效成分是[Ca(ClO)2],漂白的原理是:Ca(ClO)2在空气中发生反应.Ca(ClO)2+CO2+H2O═CaCO3
题目详情
漂白粉的主要成分为次氯酸钙[Ca(ClO)2]和氯化钙,即可用作漂白剂,又可用作消毒剂.漂白粉中有效成分是[Ca(ClO)2],漂白的原理是:Ca(ClO)2在空气中发生反应.Ca(ClO)2+CO2+H2O═CaCO3↓+2HClO;HClO是一种酸性比盐酸弱的酸,不稳定,具有漂白性,能使品红等有色物质褪色.
(1)HClO在常温下分解,反应为2HClO=2HCl+O2↑.某瓶HClO溶液放置一段时间后,溶液的pH___ (填“增大”或“减小”或“不变”).
(2)在漂白粉中滴加盐酸,能加快漂白的速率.写出漂白粉中加入盐酸反应的化学方程式___.
(3)有一包长时间放置的漂白粉,想知道该漂白粉是否变质,某同学设计了下列探究实验.
【提出问题】长时间放置的漂白粉是否变质?
【猜 想】
猜想1:该漂白粉未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为___;
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3.
【实验探究】限选试剂及仪器,盐酸、石灰水、品红溶液、试管、带导管的单孔塞.
(4)现有实验后的HCl与CaCl2的混合溶液,为了分析混合溶液中HCl和CaCl2的质量分数,设计了如图实验方案:
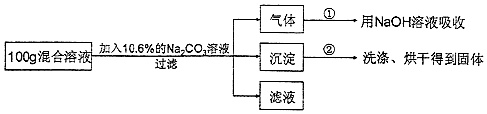
【实验数据】上述实验中100g混合溶液与mg溶质的质量分数为10.6%的Na2CO3溶液恰好完全反应后,共记录了两组实验数据:第①组,气体吸收完全后,NaOH溶液质量增加4.4g;第②组,沉淀完全后,经过滤、洗涤、烘干后得到固体的质量为10g.
根据实验设计及有关数据进行分析与计算:
(1)m=___.
(2)上述实验中100g混合溶液与mg溶质的质量分数为10.6%的Na2CO3溶液恰好完全反应,经过滤后所得“滤液”中溶质的质量分数为多少?(不考虑过滤中的损失,计算结果保留到小数点后一位.)
(1)HClO在常温下分解,反应为2HClO=2HCl+O2↑.某瓶HClO溶液放置一段时间后,溶液的pH___ (填“增大”或“减小”或“不变”).
(2)在漂白粉中滴加盐酸,能加快漂白的速率.写出漂白粉中加入盐酸反应的化学方程式___.
(3)有一包长时间放置的漂白粉,想知道该漂白粉是否变质,某同学设计了下列探究实验.
【提出问题】长时间放置的漂白粉是否变质?
【猜 想】
猜想1:该漂白粉未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为___;
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3.
【实验探究】限选试剂及仪器,盐酸、石灰水、品红溶液、试管、带导管的单孔塞.
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量样品于试管中, ___ | 有气体产生, 气体使石灰水变浑浊. | 猜想2成立 |
| ②在上述反应后试管中加少量 ___ | ___ |

【实验数据】上述实验中100g混合溶液与mg溶质的质量分数为10.6%的Na2CO3溶液恰好完全反应后,共记录了两组实验数据:第①组,气体吸收完全后,NaOH溶液质量增加4.4g;第②组,沉淀完全后,经过滤、洗涤、烘干后得到固体的质量为10g.
根据实验设计及有关数据进行分析与计算:
(1)m=___.
(2)上述实验中100g混合溶液与mg溶质的质量分数为10.6%的Na2CO3溶液恰好完全反应,经过滤后所得“滤液”中溶质的质量分数为多少?(不考虑过滤中的损失,计算结果保留到小数点后一位.)
▼优质解答
答案和解析
(1)某瓶HClO溶液放置一段时间后,次氯酸分解生成了盐酸,溶液的酸性增强,pH减小.
故填:减小.
(2)漂白粉中的次氯酸钙和稀盐酸反应生成氯化钙和次氯酸,加入盐酸反应的化学方程式为:Ca(ClO)2+2HCl=CaCl2+2HClO.
故填:Ca(ClO)2+2HCl=CaCl2+2HClO.
(3)【猜 想】
猜想1:该漂白粉未变质,成分不变,因此固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,一部分次氯酸钙和空气中的水、二氧化碳反应生成了碳酸钙,因此固体成分为CaCl2、Ca(ClO)2、CaCO3;
猜想3:该漂白粉全部变质,全部的次氯酸钙和空气中的水、二氧化碳反应生成了碳酸钙,因此固体成分为CaCl2、CaCO3.
故填:CaCl2、Ca(ClO)2、CaCO3.
【实验探究】实验方案如下表所示:
(4)【实验数据】
(1)设和稀盐酸反应的碳酸钠质量为x,生成的氯化钠质量为y,和氯化钙反应的碳酸钠质量为m,反应生成的氯化钠质量为n,
Na2CO3+2HCl=2NaCl+H2O+CO2↑ Na2CO3+CaCl2=CaCO3↓+2NaCl
106 117 44 106 100 117
x y 4.4g m 10g n
=
=
,
=
=
,
x=10.6g,y=11.7g,m=10.6g,n=11.7g,
碳酸钠溶液的质量为:(10.6g+10.6g)÷10.6%=200g,因此m=200,
故填:200.
(2)经过滤后所得“滤液”中溶质的质量分数为:
×100%=8.2%,
答:过滤后所得“滤液”中溶质的质量分数为8.2%.
故填:减小.
(2)漂白粉中的次氯酸钙和稀盐酸反应生成氯化钙和次氯酸,加入盐酸反应的化学方程式为:Ca(ClO)2+2HCl=CaCl2+2HClO.
故填:Ca(ClO)2+2HCl=CaCl2+2HClO.
(3)【猜 想】
猜想1:该漂白粉未变质,成分不变,因此固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,一部分次氯酸钙和空气中的水、二氧化碳反应生成了碳酸钙,因此固体成分为CaCl2、Ca(ClO)2、CaCO3;
猜想3:该漂白粉全部变质,全部的次氯酸钙和空气中的水、二氧化碳反应生成了碳酸钙,因此固体成分为CaCl2、CaCO3.
故填:CaCl2、Ca(ClO)2、CaCO3.
【实验探究】实验方案如下表所示:
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量样品于试管中,加入足量的稀盐酸,塞上带导管的单孔塞,把导管插入另一盛有澄清石灰水的试管中 | 有气体产生, 气体使石灰水变浑浊. | 猜想2成立 |
| ②在上述反应后试管中加少量品红溶液 | 品红溶液褪色 |
(1)设和稀盐酸反应的碳酸钠质量为x,生成的氯化钠质量为y,和氯化钙反应的碳酸钠质量为m,反应生成的氯化钠质量为n,
Na2CO3+2HCl=2NaCl+H2O+CO2↑ Na2CO3+CaCl2=CaCO3↓+2NaCl
106 117 44 106 100 117
x y 4.4g m 10g n
| 106 |
| x |
| 117 |
| y |
| 44 |
| 4.4g |
| 106 |
| m |
| 100 |
| 10g |
| 117 |
| n |
x=10.6g,y=11.7g,m=10.6g,n=11.7g,
碳酸钠溶液的质量为:(10.6g+10.6g)÷10.6%=200g,因此m=200,
故填:200.
(2)经过滤后所得“滤液”中溶质的质量分数为:
| 11.7g+11.7g |
| 200g+100g-4.4g-10g |
答:过滤后所得“滤液”中溶质的质量分数为8.2%.
看了漂白粉的主要成分为次氯酸钙[C...的网友还看了以下:
法律的规范作用包括()。A.指引作用B.管理作用C.评价作用D.预测作用 2020-06-04 …
企业领用的出租包装物,如果金额不大,可将其成本直接计入()。A.销售费用B.管理费用C.制造费用D 2020-06-20 …
企业对银行存款利息收入的处理,应贷记()A.“财务费用”B.“管理费用”C.“其他业务收入”D.“ 2020-06-20 …
领用低值易耗品时,下列账务处理中不正确的是()A,借记“制造费用”B借记“管理费用”C,借记“销售 2020-06-25 …
库存现金盘亏的账务处理中可能涉及到的账户有()。A.库存现金B.管理费用C.其他应收款库存现金盘亏 2020-06-27 …
会计基础题计提本月固定资产折旧12000元,其中:生产车间使用的固定资产折旧9000,企业管理部门 2020-07-16 …
下列解决生活中实际问题的方法与相应科学原理不对应的是()选项方法科学原理A用洗涤灵清洗油污利用了洗涤 2020-11-05 …
计提本月固定资产折旧12000元,其中:生产车间使用的固定资产折旧为9000元,企业管理部门使用的为 2020-11-21 …
关于房地产费用的问题15.房地产公司工程部管理人员的工资属于()A.财务费用B.管理费用C.销售费用 2020-12-06 …
由于非正常损失导致存货的盘亏一般应作为()处理A营业外支出B管理费用C资产减值损失D财务费用如果是自 2020-12-16 …