早教吧作业答案频道 -->化学-->
经测定某溶液中只含NH4+、Cl-、H+、OH-四种离子,已知这种溶液中含有一种或两种溶质.查资料表明等物质的量浓度的氨水和氯化铵溶液等体积混合后溶液显碱性,试完成下列各题.(1)试
题目详情
经测定某溶液中只含NH4+、Cl-、H+、OH-四种离子,已知这种溶液中含有一种或两种溶质.查资料表明等物质的量浓度的氨水和氯化铵溶液等体积混合后溶液显碱性,试完成下列各题.
(1)试推测能组成这种溶液的可能的溶质组合有___种(填数字).
(2)有关这种溶液,下列说法不正确的是___
A.若溶液中离子间满足c(NH4+)>c(Cl-)>c(OH-)>c(H+),则溶液中溶质一定为NH4Cl和NH3•H2O
B.若溶液中离子间满足c(Cl-)>c(NH4+)>c(H+)>c(OH-),则溶液中溶质一定只有NH4Cl
C.若溶液中c(NH4+)=c(Cl-),则该溶液一定显中性
D.若溶液中c(NH3•H2O)>c(Cl-),则溶液一定显碱性
(3)若溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl___c(NH3•H2O)(填“>”、“<”或“=”),简述理由___.
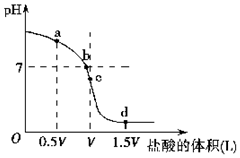
(4)水的电离程度与溶液中所溶解的电解质有关,如图是用一定浓度的HCl滴定V L同浓度NH3•H2O时得到的滴定曲线.试分析如图所示滴定过程中的a、b、c、d各点,水的电离程度最大的是___理由为___.
(5)写出a点、c点所对应溶液中各离子浓度由大到小的比较顺序
a点:___.
c点:___.

(1)试推测能组成这种溶液的可能的溶质组合有___种(填数字).
(2)有关这种溶液,下列说法不正确的是___
A.若溶液中离子间满足c(NH4+)>c(Cl-)>c(OH-)>c(H+),则溶液中溶质一定为NH4Cl和NH3•H2O
B.若溶液中离子间满足c(Cl-)>c(NH4+)>c(H+)>c(OH-),则溶液中溶质一定只有NH4Cl
C.若溶液中c(NH4+)=c(Cl-),则该溶液一定显中性
D.若溶液中c(NH3•H2O)>c(Cl-),则溶液一定显碱性
(3)若溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl___c(NH3•H2O)(填“>”、“<”或“=”),简述理由___.
(4)水的电离程度与溶液中所溶解的电解质有关,如图是用一定浓度的HCl滴定V L同浓度NH3•H2O时得到的滴定曲线.试分析如图所示滴定过程中的a、b、c、d各点,水的电离程度最大的是___理由为___.
(5)写出a点、c点所对应溶液中各离子浓度由大到小的比较顺序
a点:___.
c点:___.
▼优质解答
答案和解析
(1)某溶液中只含NH4+、Cl-、H+、OH-四种离子,已知该溶液中含有一种或两种溶质,查资料表明等物质的量浓度的氨水和氯化铵溶液等体积混合后溶液显碱性,依据溶液中存在的阴阳离子结合电荷守恒分析判断可能的溶质微粒为,NH4Cl、NH3•H2O和NH4Cl、NH4Cl和HCl,组成这种溶液的可能的溶质组合有3种,
故答案为:3;
(2)A.等物质的量浓度的氨水和氯化铵溶液等体积混合后溶液显碱性,若溶液中离子间满足c(NH4+)>c(Cl-)>c(OH-)>c(H+),则溶液中溶质一定为NH4Cl和NH3•H2O,故A正确;
B.若溶液中离子间满足c(Cl-)>c(NH4+)>c(H+)>c(OH-),则溶液中溶质可以是NH4Cl或NH4Cl和HCl混合溶液,故B错误;
C.若溶液中c(NH4+)=c(Cl-),溶液中电荷守恒,c(Cl-)+c(OH-)=c(NH4+)+c(H+),c(OH-)=c(H+),则该溶液一定显中性,故C正确;
D.等物质的量浓度的氨水和氯化铵溶液等体积混合后溶液显碱性,若溶液中c(NH3•H2O)>c(Cl-),则溶液中溶质为NH3•H2O和NH4Cl,一定显碱性,故D正确;
故答案为:B.
(3)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则c(H+)=c(OH-),溶液中的溶质是氯化铵和氨水;要使混合溶液呈中性,则氨水的物质的量大于HCl,混合前c(HCl)3•H2O),pH为7的溶液,一定是氨水与氯化铵的混合溶液,即混合时氨水略过量,c(HCl)3•H2O),
故答案为:<;pH为7的溶液,一定是氨水与氯化铵的混合溶液,即混合时氨水略过量,c(HCl)3•H2O)
(4)NH3•H2O对水的电离起抵制作用,而NH4Cl对水的电离起促进作用,所以两者恰好完全反应生成氯化铵,对水电离促进程度最大,即为c,
故答案为:c;分析题图可知,c点时盐酸和氨水正好完全反应,生成氯化铵溶液,这时水的电离程度最大;
(5)a点是等浓度的氨水和氯化铵的混合物,一水合氨电离大于铵根离子电离溶液显碱性,溶液中离子浓度:c(NH4+)>c(Cl-)>c(OH-)>c(H+),c点是恰好完全反应生成的氯化铵溶液,铵根离子水解溶液显酸性,离子浓度为:c(Cl-)>c(NH4+)>c(H+)>c(OH-),
故答案为:c(NH4+)>c(Cl-)>c(OH-)>c(H+),c(Cl-)>c(NH4+)>c(H+)>c(OH-);
故答案为:3;
(2)A.等物质的量浓度的氨水和氯化铵溶液等体积混合后溶液显碱性,若溶液中离子间满足c(NH4+)>c(Cl-)>c(OH-)>c(H+),则溶液中溶质一定为NH4Cl和NH3•H2O,故A正确;
B.若溶液中离子间满足c(Cl-)>c(NH4+)>c(H+)>c(OH-),则溶液中溶质可以是NH4Cl或NH4Cl和HCl混合溶液,故B错误;
C.若溶液中c(NH4+)=c(Cl-),溶液中电荷守恒,c(Cl-)+c(OH-)=c(NH4+)+c(H+),c(OH-)=c(H+),则该溶液一定显中性,故C正确;
D.等物质的量浓度的氨水和氯化铵溶液等体积混合后溶液显碱性,若溶液中c(NH3•H2O)>c(Cl-),则溶液中溶质为NH3•H2O和NH4Cl,一定显碱性,故D正确;
故答案为:B.
(3)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则c(H+)=c(OH-),溶液中的溶质是氯化铵和氨水;要使混合溶液呈中性,则氨水的物质的量大于HCl,混合前c(HCl)
故答案为:<;pH为7的溶液,一定是氨水与氯化铵的混合溶液,即混合时氨水略过量,c(HCl)
(4)NH3•H2O对水的电离起抵制作用,而NH4Cl对水的电离起促进作用,所以两者恰好完全反应生成氯化铵,对水电离促进程度最大,即为c,
故答案为:c;分析题图可知,c点时盐酸和氨水正好完全反应,生成氯化铵溶液,这时水的电离程度最大;
(5)a点是等浓度的氨水和氯化铵的混合物,一水合氨电离大于铵根离子电离溶液显碱性,溶液中离子浓度:c(NH4+)>c(Cl-)>c(OH-)>c(H+),c点是恰好完全反应生成的氯化铵溶液,铵根离子水解溶液显酸性,离子浓度为:c(Cl-)>c(NH4+)>c(H+)>c(OH-),
故答案为:c(NH4+)>c(Cl-)>c(OH-)>c(H+),c(Cl-)>c(NH4+)>c(H+)>c(OH-);
看了经测定某溶液中只含NH4+、C...的网友还看了以下:
(2005•崇明县一模)(A组)将氯化镁和硫酸镁固体混合物20克溶解于100克水中,再加入100克 2020-05-17 …
1.在某浓度的氯化钡溶液200ml中,加入一定体积,物质的量浓度为0.500mol/L的稀硫酸时, 2020-05-21 …
初2一道简单的科学溶液题尽快回答3.30度时氯化钾的饱和溶液250g.求(1)温度不变时,将其蒸发 2020-06-05 …
将100克质量分数为40%的氯化氨溶液,从某温度降至40摄氏度(40摄氏度时氯化氨的溶解度为45克 2020-06-05 …
等体积等物质的量浓度的氯化钠、氯化钾溶液中,阴、阳离子数目之和均为2NA.这个说法不正确等体积等物 2020-06-18 …
化学中的问题现在碳酸钾和氯化钾的混合物28.6g,和160g稀盐酸恰好完全反应,所得到的溶液质量是 2020-07-18 …
如表是氯化钠、氯化铵两种固体在不同温度下的溶解度.温度/020406080物质的溶解度/g氯化钠3 2020-07-23 …
20摄氏度时向氯化钠饱和溶液(内含水100克)里加入34克氯化钾,请问氯化钾能否完全溶解?为什么?请 2020-12-02 …
在某温度下,在体积一定的密闭容器中有适量的氨气和氯气,恰好完全反应,若生成物只有氮气气体和氯化铵固体 2021-02-08 …
1.把50克20度时的硝酸钾饱和溶液蒸干,得到12克硝酸钾.求20度时硝酸钾的溶解度2.把20度时5 2021-02-11 …