早教吧作业答案频道 -->化学-->
将等物质的量浓度的CuSO4溶液和NaCl溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如图,则下列说法正确的是A.阳极产物一定是Cl2,阴极产
题目详情
将等物质的量浓度的CuSO 4 溶液和NaCl溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如图,则下列说法正确的是
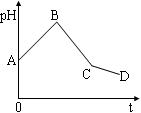

| A.阳极产物一定是Cl 2 ,阴极产物一定是Cu |
| B.BC段表示在阴极上是H + 放电产生了H 2 |
| C.整个过程中阳极先产生Cl 2 ,后产生O 2 |
| D.CD段表示阳极上OH - 放电破坏了水的电离平衡,产生了H + ,故pH减小 |
▼优质解答
答案和解析
分 析:
等物质的量浓度的CuSO 4 溶液和NaCl溶液等体积混合就是硫酸铜和氯化钠的物质的量相等。用石墨电极进行电解,电解过程中,发生的反应:开始时阳极2Cl - —2e - =Cl 2 ↑.阴极:Cu 2+ +2e - =Cu.当氯离子完全转化为氯气后,这时的溶液为Na 2 SO 4 和CuSO 4 混合溶液。接着阳极氢氧根离子放电:4OH - -4e - =2H 2 O+O 2 ↑阳极还是Cu 2+ +2e - =Cu至铜离子反应完全。此时溶液为Na 2 SO 4 和H 2 SO 4 混合溶液。后来实质就是电解水。溶剂水不断消耗,使得硫酸的浓度逐渐增大,溶液的的酸性逐渐增强,溶液的PH逐渐减小。A—B段实质相当于电解氯化铜溶液;B—C段电解的是硫酸钠和硫酸铜的混合溶液,由于阳极氢氧根离子放电:4OH - -4e - =2H 2 O+O 2 ↑,是整个溶液中C(H + )>C(OH - ) 溶液的酸性增强,PH降低。到C点硫酸铜反应完全。C—D段电解的是Na 2 SO 4 和H 2 SO 4 。实质是电解水。所以溶液的酸性增强,PH降低。所以答案为C。
C
分 析:
等物质的量浓度的CuSO 4 溶液和NaCl溶液等体积混合就是硫酸铜和氯化钠的物质的量相等。用石墨电极进行电解,电解过程中,发生的反应:开始时阳极2Cl - —2e - =Cl 2 ↑.阴极:Cu 2+ +2e - =Cu.当氯离子完全转化为氯气后,这时的溶液为Na 2 SO 4 和CuSO 4 混合溶液。接着阳极氢氧根离子放电:4OH - -4e - =2H 2 O+O 2 ↑阳极还是Cu 2+ +2e - =Cu至铜离子反应完全。此时溶液为Na 2 SO 4 和H 2 SO 4 混合溶液。后来实质就是电解水。溶剂水不断消耗,使得硫酸的浓度逐渐增大,溶液的的酸性逐渐增强,溶液的PH逐渐减小。A—B段实质相当于电解氯化铜溶液;B—C段电解的是硫酸钠和硫酸铜的混合溶液,由于阳极氢氧根离子放电:4OH - -4e - =2H 2 O+O 2 ↑,是整个溶液中C(H + )>C(OH - ) 溶液的酸性增强,PH降低。到C点硫酸铜反应完全。C—D段电解的是Na 2 SO 4 和H 2 SO 4 。实质是电解水。所以溶液的酸性增强,PH降低。所以答案为C。
看了将等物质的量浓度的CuSO4溶...的网友还看了以下:
下列情况混合后溶液中溶质质量分数最大的是A、8gNaOH放到42gH2O中B、6.2gNa2O放到 2020-04-09 …
下列说法正确的是()A.强电解质的稀溶液中不存在溶质分子B.强电解质溶液一定比弱电解质溶液的导电性 2020-04-10 …
下列关于电解质的说法中正确的是()A.强电解质在水中一定能全部溶解B.Cu能导电,因此Cu是电解质 2020-04-11 …
强电解质与弱电解质的不同点在于A.强电解质溶液的导电能力一定很强,而弱电解质溶液的导电能力一定很弱 2020-04-11 …
下列有关生物体遗传物质的叙述,正确的是A,碗豆的遗传物质主要是DNAB,酵母菌的遗传物质主要分布在 2020-04-27 …
某蛋白质分子由M个氨基酸、4条肽链组成,则该蛋白质分子()A.共有M个肽键B.至少含有20种氨基酸 2020-05-13 …
如图是A、B、C三种物质的溶解度曲线.据图回答下列问题.(1)10℃时,B物质的溶解度为g,(2) 2020-07-20 …
确定ABC的值,使e^x(1+Bx+Cx^2)=1+Ax+0(x^3)答案A=1/2,B=0,C=- 2020-10-31 …
下列有关生物体遗传物质的叙述,正确的是()A.肺炎双球菌的遗传物质主要是DNAB.染色体是遗传物质的 2020-12-02 …
下列说法正确的是()A.食用加碘盐可预防碘缺乏症,加碘盐中加的含碘物质是碘单质B.因为NaCl的水溶 2021-02-05 …