早教吧作业答案频道 -->化学-->
现有含Na2O杂质的Na2O2试样,某同学欲测定Na2O2试样的纯度.回答下列问题(1)请从图①~⑦中选用适当的装置,其连接顺序为(填各接口的字母).(2)写出该实验中发生反应的化学方程
题目详情
现有含Na2O杂质的Na2O2试样,某同学欲测定Na2O2试样的纯度.回答下列问题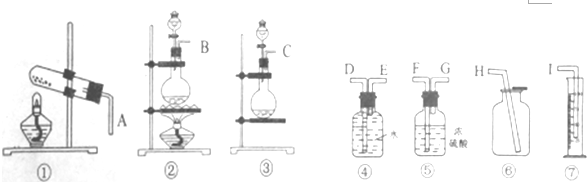
(1)请从图①~⑦中选用适当的装置,其连接顺序为(填各接口的字母)___.
(2)写出该实验中发生反应的化学方程式___.
(3)本实验中测量气体体积时主要应注意的事项有___.
(4)若实验时称取的试样为ag,产生的气体在标准状况下的体积为Vml,此试样中Na2O2的质量分数为___.

(1)请从图①~⑦中选用适当的装置,其连接顺序为(填各接口的字母)___.
(2)写出该实验中发生反应的化学方程式___.
(3)本实验中测量气体体积时主要应注意的事项有___.
(4)若实验时称取的试样为ag,产生的气体在标准状况下的体积为Vml,此试样中Na2O2的质量分数为___.
▼优质解答
答案和解析
(1)含Na2O杂质的Na2O2试样,欲测定Na2O2试样的纯度,根据题中提供的装置可知,该实验利用氧化钠和过氧化钠与水反应,该反应不需要不加热,其中过氧化钠与水反应产生氧气,称取一定量的样品,使其与水反应,根据产生的氧气的体积可计算出过氧化钠的质量,进而确定过氧化钠的质量分数,本实验中测量气体的体积是用排水量气法,所以实验装置的连接顺序为C接E,D接I,
故答案为:C接E,D接I;
(2)实验中氧化钠和过氧化钠均能和水反应,方程式为:2Na2O2+2H2O=4NaOH+O2↑;Na2O+H2O=2NaOH,
故答案为:2Na2O2+2H2O=4NaOH+O2↑;Na2O+H2O=2NaOH;
(3)由于过氧化钠与水反应是放热反应,为了准确测量气体的体积,要使气体的温度与室温相同,所以测量气体时要冷却到室温,同时也要使集气瓶中的压强与大气压相同,所以在读数时,注意量筒中液面的高度与集气瓶中液面的高度相同,
故答案为:读数时气体要冷却到室温、量筒中液面的高度与集气瓶中液面的高度相同;
(4)根据反应2Na2O2+2CO2=2Na2CO3+O2,反应结束后测得气体体积为VmL(标准状况),即生成的氧气的物质的量为
mol,过氧化钠的物质的量为
×2mol,
过氧化钠的纯度=
×100%=
%,
故答案为:
%.
故答案为:C接E,D接I;
(2)实验中氧化钠和过氧化钠均能和水反应,方程式为:2Na2O2+2H2O=4NaOH+O2↑;Na2O+H2O=2NaOH,
故答案为:2Na2O2+2H2O=4NaOH+O2↑;Na2O+H2O=2NaOH;
(3)由于过氧化钠与水反应是放热反应,为了准确测量气体的体积,要使气体的温度与室温相同,所以测量气体时要冷却到室温,同时也要使集气瓶中的压强与大气压相同,所以在读数时,注意量筒中液面的高度与集气瓶中液面的高度相同,
故答案为:读数时气体要冷却到室温、量筒中液面的高度与集气瓶中液面的高度相同;
(4)根据反应2Na2O2+2CO2=2Na2CO3+O2,反应结束后测得气体体积为VmL(标准状况),即生成的氧气的物质的量为
| 0.001V |
| 22.4 |
| 0.001V |
| 22.4 |
过氧化钠的纯度=
| ||
| a |
| 39V |
| 112a |
故答案为:
| 39V |
| 112a |
看了 现有含Na2O杂质的Na2O...的网友还看了以下:
怎样学 应该是写成比喻句 2020-05-16 …
你对:“您觉得该不该在公共场所禁烟”作民意调查,下面是三名同学设计的调查方案:同学A:我把要调查的 2020-06-14 …
水煤气是重要的气体燃料,某水煤气样品可能含有CO2、CO和H2,某化学兴趣小组的同学对该水煤气样品 2020-06-25 …
某城市有学校500所,其中大学10所,中学200所,小学290所.现在取50所学校作为一个样本进行 2020-07-09 …
成长路上,我们总会遇到这样或那样的诱惑。面对诱惑,漫画中的同学应该学会()A.与世隔绝,远离诱惑B 2020-07-10 …
多个样本均值比较发现这些样本并不全部符合近似正态总体分布的抽样,那应该采取什么统计学对于多个样本均 2020-08-03 …
情景分析(1)某同学帮助他人解决学习上难题,但是让别人帮他值日为条件。①该同学行为有什么错误?②该 2020-08-04 …
请解答有关学前教育方面的知识,1.在教学过程中,教师向儿童出示事先准备好的各种样品,如绘画、纸工、泥 2020-11-23 …
会英语的请留步:请看下面我的疑惑英语学习新句子、新单词该怎样学习,我是一名初三的学生,我想要提高英语 2020-11-26 …
在学校大扫除时,卫生委员总是这样分工:女同学负责擦玻璃等需要细心的活,男同学负责拉车、打水等重活,相 2020-12-01 …