有50mLNaOH溶液,向其中逐渐通入一定量的CO2,随后取此溶液100mL,并向此稀稀释后的溶液中逐滴加入0.1mol/L的HCl溶液,产生的CO2气体体积(标况)与所加
有50mLNaOH溶液,向其中逐渐通入一定量的CO 2 ,随后取此溶液100mL,并向此稀稀释后的溶液中逐滴加入0.1mol/L的HCl溶液,产生的
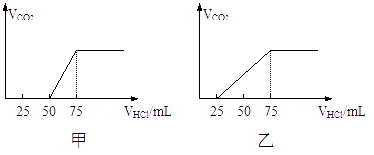 |
CO 2 气体体积(标况)与所加入的盐酸的体积之间的关系如下图所示:
试分析NaOH在吸收CO 2 气体后,在甲、乙两种情况下,所得溶液中存在的溶质是什么?其物质的量之比是多少?产生的CO 2 气体体积(标况)是多少?
如图所示,物体自O点由静止开始做匀加速直线运动,途经A、B、C三点,其中A、B之间的距离l1=2m 2020-05-13 …
已知椭圆C的中心在坐标原点O,焦点在x轴上,离心率为根号3/3,过其右焦点F的直线l的斜率为1时, 2020-05-16 …
L.O.L和XOXO分别是什么意思?英国人喜欢在信的最末加上这两个东西,不知是何用意? 2020-06-02 …
Ad、Add、BatchNo、mug、ug、O.D.、O.S.、O.L.、O.U.、q.s.中文含 2020-06-05 …
找出发音相同的单词opposite中第二个o发音相同的是:A.c[o]mpanion[kəmˈpæ 2020-06-06 …
急!高二数学直线与圆设过P(2.5)的直线l与圆x^2+y^2=4交于A,B两点,O为坐标原点(1 2020-06-06 …
如图,△ABC内接于⊙O,过BC中点D作平行于AC的直线l,l交AB于E,交⊙O于G、F,交⊙O在 2020-06-12 …
(2014•成都)如图,在⊙O的内接△ABC中,∠ACB=90°,AC=2BC,过C作AB的垂线l 2020-06-12 …
已知圆O:x2+y2=4内一定点Q(1,0),过点Q作倾斜角不为0°的直线L交圆O于A、B两点.( 2020-06-12 …
如图,点A在y轴上,点B在x轴上,且OA=OB=1,经过原点O的直线l交线段AB于点C,过C作OC 2020-06-15 …