早教吧作业答案频道 -->化学-->
工业上以铬铁矿(主要成分FeO•Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠(Na2Cr2O7•2H2O)的主要反应如下:①4FeO•Cr2O3+8Na2CO3+7O2高温
题目详情
工业上以铬铁矿(主要成分FeO•Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠(Na2Cr2O7•2H2O)的主要反应如下:
①4FeO•Cr2O3+8Na2CO3+7O2
8Na2CrO4+2Fe2O3+8CO2
②2Na2CrO4+H 2SO4⇌Na2SO4+Na2Cr2O7+H2O
(1)工业上反应①需不断搅拌,其目的是___.
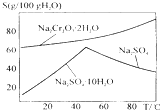
(2)如图是红矾钠(Na2Cr2O7•2H2O)和Na2SO4的溶解度曲线.从Na2Cr2O7和 Na2SO4的混合溶液中提取Na2Cr2O7晶体的操作:先将混合溶液蒸发结晶,趁热过滤.趁热过滤的目的是___;然后将滤液___,从而析出红矾钠.
(3)Na2Cr2O7与KCl进行复分解反应可制取K2Cr2O7,现用重铬酸钾测定铁矿石中铁的含量,测定原理为:Fe2++Cr2O72-+H+ Fe3++Cr3++7H2O (未配平) 实验步骤如下:
步骤1:将m g铁矿石加浓盐酸加热溶解
步骤2:加入SnCl2溶液将Fe3+还原
步骤3:将所得溶液冷却,加入HgCl2溶液,将过量的Sn2+氧化为Sn4+
步骤4:加入15mL硫酸和磷酸的混合酸及5滴0.2%二苯胺磺酸钠指示剂
步骤5:立即用c mol•L-1重铬酸钾溶液滴定至溶液呈稳定紫色,即为终点,消耗重铬酸钾溶液V mL
①如省去步骤③,则所测定的铁的含量___(填“偏高”、“偏低”或“无影响”).
②步骤5使用的主要玻璃仪器有___.
③则测定铁矿石中铁的含量的计算式为___(用字母表示,不用化简).
①4FeO•Cr2O3+8Na2CO3+7O2
| ||
②2Na2CrO4+H 2SO4⇌Na2SO4+Na2Cr2O7+H2O

(1)工业上反应①需不断搅拌,其目的是___.
(2)如图是红矾钠(Na2Cr2O7•2H2O)和Na2SO4的溶解度曲线.从Na2Cr2O7和 Na2SO4的混合溶液中提取Na2Cr2O7晶体的操作:先将混合溶液蒸发结晶,趁热过滤.趁热过滤的目的是___;然后将滤液___,从而析出红矾钠.
(3)Na2Cr2O7与KCl进行复分解反应可制取K2Cr2O7,现用重铬酸钾测定铁矿石中铁的含量,测定原理为:Fe2++Cr2O72-+H+ Fe3++Cr3++7H2O (未配平) 实验步骤如下:
步骤1:将m g铁矿石加浓盐酸加热溶解
步骤2:加入SnCl2溶液将Fe3+还原
步骤3:将所得溶液冷却,加入HgCl2溶液,将过量的Sn2+氧化为Sn4+
步骤4:加入15mL硫酸和磷酸的混合酸及5滴0.2%二苯胺磺酸钠指示剂
步骤5:立即用c mol•L-1重铬酸钾溶液滴定至溶液呈稳定紫色,即为终点,消耗重铬酸钾溶液V mL
①如省去步骤③,则所测定的铁的含量___(填“偏高”、“偏低”或“无影响”).
②步骤5使用的主要玻璃仪器有___.
③则测定铁矿石中铁的含量的计算式为___(用字母表示,不用化简).
▼优质解答
答案和解析
(1)反应①是在回转窑中进行,反应时需不断搅拌,使反应物充分接触,加快反应速率;故答案为:使反应物充分接触,加快反应速率;(2)由图可知,温度高有利于硫酸钠结晶析出,趁热过滤可以防止Na2Cr2O7•2H2O结晶析...
看了 工业上以铬铁矿(主要成分Fe...的网友还看了以下:
已知集合E={x||x-1|≥m},F={x|10/x+6>1}(1)若m=3,求E交F.(2)若E 2020-03-30 …
已知函数f(x)=5x3+3x2,f(2),f(a-2),f(a)-f(2)的值 2020-05-23 …
定义在R上的函数f(x)满足(x-1)f’(x)≤0,且y=f(x+1)为偶函数,当|x1-1|< 2020-06-08 …
设一数列a,b,c,d,e,f,通过栈结构不可能不可能排成的顺序数列为()A)c,b,e,f,d, 2020-06-28 …
某同学用显微镜观察洋葱鳞片叶内表皮细胞时看到了如图所示几幅图象,这几幅图象在操作过程中出现的顺序依 2020-07-01 …
几道高中函数题(求详解)1.已知函数f(X)=ax²+bx+c满足f(1)=f(4),则()A.f 2020-07-05 …
条件概率问题P(E|F)=P(EF)/P(F)这个是如何从最原始的公式推导出来的?另外P(EF)我 2020-07-09 …
设f(x)有二阶连续导数,且f'(2)=2,limf''(x)/|x-2|=-2(x-->2)则一 2020-07-31 …
三道数学选择题1.当X→0时,e^(-1/x)是()A.无穷小量B.有界变量C.无界变量2.已知随 2020-07-31 …
若偶函数f(x)在x≤-1上是增函数,则下列关系中成立的是a.f(2)<f(-3/2)<f(-1) 2020-08-01 …