早教吧作业答案频道 -->化学-->
过氧化钠(Na2O2)是一种淡黄色固体.在一次科技活动中,化学兴趣小组设计了如图1所示的实验,其中A、C是包有过氧化钠的棉花,B是未包过氧化钠的棉花.实验中观察到A、C棉花依次燃烧
题目详情
过氧化钠(Na2O2)是一种淡黄色固体.在一次科技活动中,化学兴趣小组设计了如图1所示的实验,其中A、C是包有过氧化钠的棉花,B是未包过氧化钠的棉花.实验中观察到A、C棉花依次燃烧,B棉花未燃烧.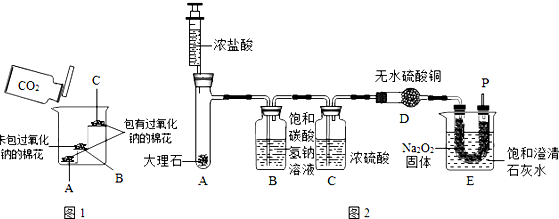
(1)B棉花起的作用是___
(2)棉花能燃烧,除了满足棉花是可燃物之外,还需满足___与氧气接触,温度达到棉花的着火点以上
的条件.
【提出问题】上述实验中是如何给棉花提供燃烧条件的?
【查阅资料】
①Na2O2与稀盐酸反应时,生成NaCl、H2O和O2.
②在常温下Na2O2与CO2、H2O均能发生化学反应.
③无水硫酸铜为白色固体,吸水后变为蓝色.
【实验设计】经过讨论,小组同学设计用如图2所示装置进行实验探究.
【实验步骤】
①检查整套装置的气密性;
②把相关的试剂放入对应的仪器内;
③用力推动针筒的活塞,把稀盐酸注入试管内;
④一段时间后,在P处放置一根带火星的木条,观察现象.
【实验现象】
①无水硫酸铜没有变蓝色;
②___ ③___
【实验分析】
(3)B装置的作用是___
(4)E装置中产生现象的原因是___
①Na2O2和CO2反应产生的一种气体,使图1中的棉花满足了燃烧的一个条件.
②Na2O2和CO2反应过程中伴随能量变化,使图1中的棉花满足了燃烧的另一个条件.
【拓展提高】
①Na2O2和CO2反应除生成一种气体外,还生成了一种固体,学生甲认为生成的固体是NaOH,学生乙认为是Na2CO3,同学们经思考后认为___同学的猜想是错误的,理由是___.
②写出Na2O2和CO2反应的化学方程式___.

(1)B棉花起的作用是___
(2)棉花能燃烧,除了满足棉花是可燃物之外,还需满足___与氧气接触,温度达到棉花的着火点以上
的条件.
【提出问题】上述实验中是如何给棉花提供燃烧条件的?
【查阅资料】
①Na2O2与稀盐酸反应时,生成NaCl、H2O和O2.
②在常温下Na2O2与CO2、H2O均能发生化学反应.
③无水硫酸铜为白色固体,吸水后变为蓝色.
【实验设计】经过讨论,小组同学设计用如图2所示装置进行实验探究.
【实验步骤】
①检查整套装置的气密性;
②把相关的试剂放入对应的仪器内;
③用力推动针筒的活塞,把稀盐酸注入试管内;
④一段时间后,在P处放置一根带火星的木条,观察现象.
【实验现象】
①无水硫酸铜没有变蓝色;
②___ ③___
【实验分析】
(3)B装置的作用是___
(4)E装置中产生现象的原因是___
①Na2O2和CO2反应产生的一种气体,使图1中的棉花满足了燃烧的一个条件.
②Na2O2和CO2反应过程中伴随能量变化,使图1中的棉花满足了燃烧的另一个条件.
【拓展提高】
①Na2O2和CO2反应除生成一种气体外,还生成了一种固体,学生甲认为生成的固体是NaOH,学生乙认为是Na2CO3,同学们经思考后认为___同学的猜想是错误的,理由是___.
②写出Na2O2和CO2反应的化学方程式___.
▼优质解答
答案和解析
(1)A、C是包有过氧化钠的棉花,B是未包过氧化钠的棉花.实验中观察到A、C棉花依次燃烧,B棉花未燃烧,是将B与A、C对比,从而得出结论;
故答案为:对照实验;
(2)物质燃烧需要三个条件:①物质是可燃物②与氧气接触③温度达到着火点.棉花是可燃物,还缺少另外两个条件;
故答案为:与氧气接触,温度达到棉花的着火点以上.
【实验现象】大理石和浓盐酸反应生成二氧化碳,进入B装置,饱和的碳酸氢钠溶液可与浓盐酸挥发出来的氯化氢气体反应从而除去氯化氢气体;通过C得到干燥的二氧化碳,除去混有的水蒸气,故D中无现象;E中过氧化钠固体与二氧化碳反应放热,氢氧化钙的溶解度随着温度升高而减小溶质析出,澄清的石灰水变浑浊;过氧化钠与二氧化碳反应生成氧气,使P处带火星的木条复燃;
故答案为:
②E中石灰水变浑浊;
③P处带火星木条复燃
【实验分析】
(3)E装置中需要纯净的二氧化碳,二氧化碳与碳酸氢钠溶液不反应,氯化氢气体与之可反应从而被除去;
故答案为:除去A中浓盐酸挥发出的氯化氢气体;
(4)Na2O2与CO2反应放出热量,使烧杯E中石灰水温度升高,由于Ca(OH)2溶解度随温度升高而减小,因此升温导致饱和石灰水析出固体Ca(OH)2,产生浑浊;
故答案为:
Na2O2与CO2反应放出热量,使烧杯E中石灰水温度升高,由于Ca(OH)2溶解度随温度升高而减小,因此升温导致饱和石灰水析出固体Ca(OH)2,产生浑浊;
【拓展提高】①根据质量守恒定律,化学反应前后元素的种类不变;而反应前的物质是Na2O2与CO2,没有H元素,因此不可能生成NaOH,故甲同学猜想错误;
故答案为:甲;反应前没有H元素,因此不可能生成NaOH;
②Na2O2与CO2反应生成碳酸钠和氧气,方程式是:2Na2O2+2CO2═2Na2CO3+O2↑;
故答案为:2Na2O2+2CO2═2Na2CO3+O2↑.
故答案为:对照实验;
(2)物质燃烧需要三个条件:①物质是可燃物②与氧气接触③温度达到着火点.棉花是可燃物,还缺少另外两个条件;
故答案为:与氧气接触,温度达到棉花的着火点以上.
【实验现象】大理石和浓盐酸反应生成二氧化碳,进入B装置,饱和的碳酸氢钠溶液可与浓盐酸挥发出来的氯化氢气体反应从而除去氯化氢气体;通过C得到干燥的二氧化碳,除去混有的水蒸气,故D中无现象;E中过氧化钠固体与二氧化碳反应放热,氢氧化钙的溶解度随着温度升高而减小溶质析出,澄清的石灰水变浑浊;过氧化钠与二氧化碳反应生成氧气,使P处带火星的木条复燃;
故答案为:
②E中石灰水变浑浊;
③P处带火星木条复燃
【实验分析】
(3)E装置中需要纯净的二氧化碳,二氧化碳与碳酸氢钠溶液不反应,氯化氢气体与之可反应从而被除去;
故答案为:除去A中浓盐酸挥发出的氯化氢气体;
(4)Na2O2与CO2反应放出热量,使烧杯E中石灰水温度升高,由于Ca(OH)2溶解度随温度升高而减小,因此升温导致饱和石灰水析出固体Ca(OH)2,产生浑浊;
故答案为:
Na2O2与CO2反应放出热量,使烧杯E中石灰水温度升高,由于Ca(OH)2溶解度随温度升高而减小,因此升温导致饱和石灰水析出固体Ca(OH)2,产生浑浊;
【拓展提高】①根据质量守恒定律,化学反应前后元素的种类不变;而反应前的物质是Na2O2与CO2,没有H元素,因此不可能生成NaOH,故甲同学猜想错误;
故答案为:甲;反应前没有H元素,因此不可能生成NaOH;
②Na2O2与CO2反应生成碳酸钠和氧气,方程式是:2Na2O2+2CO2═2Na2CO3+O2↑;
故答案为:2Na2O2+2CO2═2Na2CO3+O2↑.
看了 过氧化钠(Na2O2)是一种...的网友还看了以下:
甘氨酸二肽氧化反应为3O2(g)+C4H8N2O3=H2NCONH2(s)+3CO2(g)+2H2 2020-05-12 …
现将71.9g高锰酸钾与二氧化氢混合物充分加热,冷却后称得剩余固体的质量为65.5g.请计算1.生 2020-05-13 …
碳酸钠和氯化钠的固体混合物13.6g,与一定质量的稀盐酸恰好完全反应,得到10%的氯化钠溶液147 2020-05-16 …
(1)氢氧化钠固体曝露在空气会吸收水分而潮解,还会吸收二氧化碳而变质,这一变化的化学方程式可表示为 2020-05-17 …
氢氧化钙与氢氧化钠的固体混合物22、8g与237、2g碳酸钠溶液恰好完全反应...氢氧化钙与氢氧化 2020-07-19 …
谢谢在实验室里加热30g氯酸钾KClO3和二氧化锰的混合物制取氧气,完全反应后剩余固体质量为20. 2020-07-22 …
将a克氯酸钾与1克二氧化锰混合充分加热,最终可得10克氧气.已知在标准状况下氧气的密度为1.429克 2020-11-10 …
将a克氯酸钾与1克二氧化锰混合充分加热,最终可得10克氧气.已知在标准状况下氧气的密度为1.429克 2020-11-10 …
实验室有一瓶久置的氢氧化钠固体.(1)氢氧化钠俗称、、,其固体暴露在空气中时易与空气中的反应而变质, 2021-01-10 …
实验室物质的制取(1)固体和固体反应需要加热的有氧气氨气(2)固体和液体反应需要加热的有氯气氯化氢( 2021-02-01 …