早教吧作业答案频道 -->化学-->
某化学兴趣小组为探究铜跟浓硫酸反应,用如图装置进行有关实验.请回答下列问题:(1)装置A中发生的化学反应的化学方程式为;(2)装置B的作用是贮存多余的气体,B中广口瓶内应
题目详情
某化学兴趣小组为探究铜跟浓硫酸反应,用如图装置进行有关实验.请回答下列问题:
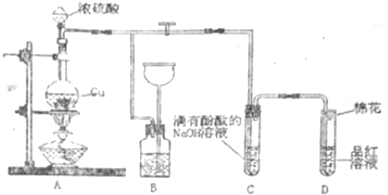
(1)装置A中发生的化学反应的化学方程式为___;
(2)装置B的作用是贮存多余的气体,B中广口瓶内应盛放的液体是___(填序号);
①水 ②酸性KMnO4 ③Na2CO3溶液 ④饱和的NaHSO3溶液
(3)装置C和D中产生的现象相同,但原因却不同.C中是由于SO2___,而D中则是由于SO2具有___;
(4)装置D中试管口塞一团棉花,棉花中应浸有一种液体,其作用是___;
(5)实验完毕,待A中烧瓶内液体冷却后,过滤,向滤液中加入少量的蒸馏水稀释,溶液为蓝色,为了证明蓝色只与Cu2+有关,而与其它离子无关,某同学设计了下列实验,其中对实验目的没有意义的是___(填序号);
①观察稀H2SO4溶液呈无色
②观察CuSO4粉末呈白色
③稀释CuSO4溶液,溶液蓝色变浅
④往CuSO4溶液中加入足量NaOH溶液,生成蓝色沉淀,过滤,滤液呈无色
⑤往CuSO4溶液中加入足量BaCl2的溶液,生成白色沉淀,过滤,滤液仍显蓝色
(6)若实验中用7.2g铜片和12.5ml18.0ml•L-1的浓硫酸在加热条件充分反应,最终铜片仍有剩余.根据所学的知识,某同学认为溶液中一定还有硫酸剩余,其理由是___.
假定反应前后溶液的体积不变,设剩余硫酸的浓度为amol/L,现向反应后溶液中缓慢加入硝酸钾固体,充分搅拌直到剩余铜片恰好完全反应,反应消耗硝酸钾___mol(用含a的代数式表示,要化简).

(1)装置A中发生的化学反应的化学方程式为___;
(2)装置B的作用是贮存多余的气体,B中广口瓶内应盛放的液体是___(填序号);
①水 ②酸性KMnO4 ③Na2CO3溶液 ④饱和的NaHSO3溶液
(3)装置C和D中产生的现象相同,但原因却不同.C中是由于SO2___,而D中则是由于SO2具有___;
(4)装置D中试管口塞一团棉花,棉花中应浸有一种液体,其作用是___;
(5)实验完毕,待A中烧瓶内液体冷却后,过滤,向滤液中加入少量的蒸馏水稀释,溶液为蓝色,为了证明蓝色只与Cu2+有关,而与其它离子无关,某同学设计了下列实验,其中对实验目的没有意义的是___(填序号);
①观察稀H2SO4溶液呈无色
②观察CuSO4粉末呈白色
③稀释CuSO4溶液,溶液蓝色变浅
④往CuSO4溶液中加入足量NaOH溶液,生成蓝色沉淀,过滤,滤液呈无色
⑤往CuSO4溶液中加入足量BaCl2的溶液,生成白色沉淀,过滤,滤液仍显蓝色
(6)若实验中用7.2g铜片和12.5ml18.0ml•L-1的浓硫酸在加热条件充分反应,最终铜片仍有剩余.根据所学的知识,某同学认为溶液中一定还有硫酸剩余,其理由是___.
假定反应前后溶液的体积不变,设剩余硫酸的浓度为amol/L,现向反应后溶液中缓慢加入硝酸钾固体,充分搅拌直到剩余铜片恰好完全反应,反应消耗硝酸钾___mol(用含a的代数式表示,要化简).
▼优质解答
答案和解析
(1)浓硫酸具有强氧化性,在加热条件下与铜发生氧化还原反应:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O,
故答案为:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O;
(2)SO2易溶于水,具有酸性和还原性,可与酸性KMnO4、Na2SO3溶液反应,难溶于水饱和的NaHSO3溶液,可用排饱和NaHSO3溶液收集,
故答案为:④;
(3)SO2溶液具有酸性,可与NaOH溶液反应,发生:SO2+2OH-=SO32-+H2O,则滴加酚酞的氢氧化钠溶液褪色,具有漂白性,可使品红溶液褪色,
故答案为:溶液具有酸性,中和了溶液中的NaOH;漂白性;
(4)二氧化硫有毒,不能排放到空气中,应可氢氧化钠溶液反应,则棉花上可浸有氢氧化钠溶液,防止污染空气,
故答案为:吸收多余的二氧化硫,防止污染空气;
(5)①观察稀硫酸溶液呈无色,可说明SO42-无色;
②观察CuSO4粉末呈白色,不能证明蓝色只与Cu2+有关;
③稀释CuSO4溶液,溶液蓝色变浅,因阳离子和阴离子浓度都变浅,不能证明;
④往CuSO4溶液中加入足量NaOH溶液,生成蓝色沉淀,过滤,滤液呈无色,铜离子浓度减小,可说明与铜离子有关;
⑤往CuSO4溶液中加入足量BaCl2的溶液,生成白色沉淀,过滤,滤液仍呈蓝色,铜离子物质的量不变,可说明与铜离子有关,
则对实验目的没有意义的是②③,
故答案为:②③;
(6)浓硫酸具有强氧化性,而稀硫酸与铜不反应,随着反应的进行,硫酸浓度不断降低,稀硫酸与铜不反应,则反应后溶液中一定含有硫酸,浓H2SO4与铜反应的过程中,浓度会变稀,而稀硫酸不与铜反应,所以会有剩余,加入硝酸钾后,硝酸根离子在氢离子存在情况下有强氧化性,能与铜反应,剩余硫酸浓度为amol/L,则硫酸物质的量=0.0125L×amol/L=0.0125amol,n(Cu)=
=0.1125mol,n(H2SO4)=0.0125L×18mol/L=0.225mol,参加反应的硫酸物质的量=0.225mol-0.0125amol,Cu+2H2SO4
CuSO4+SO2↑+2H2O,2mol硫酸反应单质转移2mol,则电子转移为:0.225mol-0.0125amol,设加入硝酸钾物质的量为x,依据电子守恒列式计算得到:0.1125mol×2=0.225mol-0.0125amol+3x,得到x=
mol,
故答案为:反应过程中浓H2SO4被不断消耗,生成的水逐渐增多,使浓硫酸逐渐变稀,至一定浓度就不再与铜片反应;
;
| ||
故答案为:Cu+2H2SO4(浓)
| ||
(2)SO2易溶于水,具有酸性和还原性,可与酸性KMnO4、Na2SO3溶液反应,难溶于水饱和的NaHSO3溶液,可用排饱和NaHSO3溶液收集,
故答案为:④;
(3)SO2溶液具有酸性,可与NaOH溶液反应,发生:SO2+2OH-=SO32-+H2O,则滴加酚酞的氢氧化钠溶液褪色,具有漂白性,可使品红溶液褪色,
故答案为:溶液具有酸性,中和了溶液中的NaOH;漂白性;
(4)二氧化硫有毒,不能排放到空气中,应可氢氧化钠溶液反应,则棉花上可浸有氢氧化钠溶液,防止污染空气,
故答案为:吸收多余的二氧化硫,防止污染空气;
(5)①观察稀硫酸溶液呈无色,可说明SO42-无色;
②观察CuSO4粉末呈白色,不能证明蓝色只与Cu2+有关;
③稀释CuSO4溶液,溶液蓝色变浅,因阳离子和阴离子浓度都变浅,不能证明;
④往CuSO4溶液中加入足量NaOH溶液,生成蓝色沉淀,过滤,滤液呈无色,铜离子浓度减小,可说明与铜离子有关;
⑤往CuSO4溶液中加入足量BaCl2的溶液,生成白色沉淀,过滤,滤液仍呈蓝色,铜离子物质的量不变,可说明与铜离子有关,
则对实验目的没有意义的是②③,
故答案为:②③;
(6)浓硫酸具有强氧化性,而稀硫酸与铜不反应,随着反应的进行,硫酸浓度不断降低,稀硫酸与铜不反应,则反应后溶液中一定含有硫酸,浓H2SO4与铜反应的过程中,浓度会变稀,而稀硫酸不与铜反应,所以会有剩余,加入硝酸钾后,硝酸根离子在氢离子存在情况下有强氧化性,能与铜反应,剩余硫酸浓度为amol/L,则硫酸物质的量=0.0125L×amol/L=0.0125amol,n(Cu)=
| 7.2g |
| 64g/mol |
| ||
| a |
| 240 |
故答案为:反应过程中浓H2SO4被不断消耗,生成的水逐渐增多,使浓硫酸逐渐变稀,至一定浓度就不再与铜片反应;
| a |
| 240 |
看了某化学兴趣小组为探究铜跟浓硫酸...的网友还看了以下:
数学题(六年级数学广角)在线等的~~~~~~~!希望小学有367位同学,至少有两人的生日是在同一天 2020-05-13 …
物理探究题:小明同学有是三个外形一样的凸透镜,但它们分别是玻璃,塑料和水晶制成的,现在小明想要比较 2020-05-13 …
一道数学题,是七年级下学期的.有一个多边形,最小的内角为120度,再大一点的是12 度,之后每一个 2020-05-13 …
内外积的由来为什么叫数量积是内积,而向量积是外积,为什么不反过来,叫数量积是外积,向量机是内积?不 2020-05-14 …
高一高二有数学要学,那高三还有数学要学吗,如果有,那高三的数学是有新内容还是只是复习高一高二的内容 2020-06-03 …
英语作文你是王林,一名交流学生来到英国小镇学习.内容:校园比你在国内就读的中学大三倍,绿树环绕,拥 2020-06-11 …
学了《咏雪》后,有一位同学根据课文内容写出了上联,请你结合《陈太丘与友期》的有关内容对出下联。上学 2020-06-12 …
李明同学说:“进到中学来,功课变多了,内容也变了,老师不熟悉,同学多是新面孔,真烦恼。”我们应建议 2020-06-18 …
孙中山是中国近代政治文明——共和制的重要催生人.他的学说是“内审中国之情势,外察世界之潮流,兼收. 2020-06-18 …
有时做不起数学题,是不是就说明我太笨,没有学数学的天赋.有数学天赋的人是不是一学概念定理做几道练习 2020-06-26 …