早教吧作业答案频道 -->化学-->
利用黄铜矿(CuFeS2)生产铜、绿矾的过程如下.请回答:(1)CuFeS2中铜的化合价为+2价,则铁的化合价为.(2)要从溶液中得到绿矾,必须进行的实验操作是(按前后顺序填写字母序号
题目详情
利用黄铜矿(CuFeS2)生产铜、绿矾的过程如下.请回答:
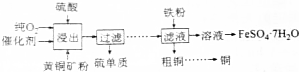
(1)CuFeS2中铜的化合价为+2价,则铁的化合价为___.
(2)要从溶液中得到绿矾,必须进行的实验操作是___(按前后顺序填写字母序号).
a.过滤洗涤 b.蒸发浓缩 c.冷却结晶 d.灼烧 e.干燥
(3)实验室中配制FeSO4溶液时常将绿矾溶于一定浓度的硫酸中国,再加水稀释,这样操作的目的是___.
(4)绿矾产品的纯度可用滴定法进行测定,实验步骤如下:
步骤1:称取6.000g绿矾产品,经溶解、定容等步骤准确配制250mL溶液.
步骤 2:从上述容量瓶中量取25.00mL待测液溶于锥形瓶中.
步骤3:用硫酸酸化的0.0100mol/LKMnO4溶液滴定至终点,记录消耗KMnO4溶液的体积.
步骤4:重复步骤2、步骤3两次.三次平均消耗KMnO4溶液40.00mL.
①判断此滴定实验达到终点的现象是___.
②写出滴定过程中发生反应的离子方程式___.
③计算上述样品中FeSO4•7H2O的质量分数为___(保留四位有效数字).
(5)粗铜经过电解精炼可制得纯铜,电解精炼过程中阴极发生的电极反应式为___.

(1)CuFeS2中铜的化合价为+2价,则铁的化合价为___.
(2)要从溶液中得到绿矾,必须进行的实验操作是___(按前后顺序填写字母序号).
a.过滤洗涤 b.蒸发浓缩 c.冷却结晶 d.灼烧 e.干燥
(3)实验室中配制FeSO4溶液时常将绿矾溶于一定浓度的硫酸中国,再加水稀释,这样操作的目的是___.
(4)绿矾产品的纯度可用滴定法进行测定,实验步骤如下:
步骤1:称取6.000g绿矾产品,经溶解、定容等步骤准确配制250mL溶液.
步骤 2:从上述容量瓶中量取25.00mL待测液溶于锥形瓶中.
步骤3:用硫酸酸化的0.0100mol/LKMnO4溶液滴定至终点,记录消耗KMnO4溶液的体积.
步骤4:重复步骤2、步骤3两次.三次平均消耗KMnO4溶液40.00mL.
①判断此滴定实验达到终点的现象是___.
②写出滴定过程中发生反应的离子方程式___.
③计算上述样品中FeSO4•7H2O的质量分数为___(保留四位有效数字).
(5)粗铜经过电解精炼可制得纯铜,电解精炼过程中阴极发生的电极反应式为___.
▼优质解答
答案和解析
(1)CuFeS2中铜的化合价为+2价,硫为-2价,根据元素化合价代数和为零可和铁的化合价为+2价,
故答案为:+2;
(2)要从溶液中得到绿矾,可以通过蒸发浓缩,冷却结晶,过滤,洗涤,干燥等步骤,所以实验操作的序号为bcae,
故答案为:bcae;
(3)亚铁离子易水解,在配制硫酸亚铁溶液时要防止亚铁离子水解,所以将绿矾溶于一定浓度的硫酸中可以抑制亚铁离子水解,
故答案为:抑制亚铁离子水解;
(4)①根据题中实验步骤可知,滴定实验达到终点时,溶液中的高锰酸钾不完全褪色,溶液呈浅红色,所以判断滴定实验达到终点的现象是滴加最后一滴KMnO4溶液时,溶液变成浅红色且半分钟内不褪色,
故答案为:滴加最后一滴KMnO4溶液时,溶液变成浅红色且半分钟内不褪色;
②酸性KMnO4被FeSO4还原时生成Mn2+,同时生成铁离子,反应的离子方程式为MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O,
故答案为:MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O;
③根据电子得失守恒有关系式MnO4-~5Fe2+,滴定中用去的高锰酸钾的物质的量为0.0100mol/L×0.04L=0.0004mol,所以6.000g绿矾产品中FeSO4•7H2O的物质的量为
×5×0.0004mol=0.02mol,所以样品中FeSO4•7H2O的质量分数为
×100%=92.67%,
故答案为:92.67%;
(5)粗铜电解精炼过程中阴极上是铜离子得电子生成铜单质,电极反应式为Cu2++2e-═Cu,
故答案为:Cu2++2e-═Cu.
故答案为:+2;
(2)要从溶液中得到绿矾,可以通过蒸发浓缩,冷却结晶,过滤,洗涤,干燥等步骤,所以实验操作的序号为bcae,
故答案为:bcae;
(3)亚铁离子易水解,在配制硫酸亚铁溶液时要防止亚铁离子水解,所以将绿矾溶于一定浓度的硫酸中可以抑制亚铁离子水解,
故答案为:抑制亚铁离子水解;
(4)①根据题中实验步骤可知,滴定实验达到终点时,溶液中的高锰酸钾不完全褪色,溶液呈浅红色,所以判断滴定实验达到终点的现象是滴加最后一滴KMnO4溶液时,溶液变成浅红色且半分钟内不褪色,
故答案为:滴加最后一滴KMnO4溶液时,溶液变成浅红色且半分钟内不褪色;
②酸性KMnO4被FeSO4还原时生成Mn2+,同时生成铁离子,反应的离子方程式为MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O,
故答案为:MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O;
③根据电子得失守恒有关系式MnO4-~5Fe2+,滴定中用去的高锰酸钾的物质的量为0.0100mol/L×0.04L=0.0004mol,所以6.000g绿矾产品中FeSO4•7H2O的物质的量为
| 250 |
| 25 |
| 0.02×278 |
| 6.000 |
故答案为:92.67%;
(5)粗铜电解精炼过程中阴极上是铜离子得电子生成铜单质,电极反应式为Cu2++2e-═Cu,
故答案为:Cu2++2e-═Cu.
看了利用黄铜矿(CuFeS2)生产...的网友还看了以下:
写出下列氧化物的化学式:(1)二氧化碳,(2)氧化镁,(3)四氧化三铁,(4)双氧水,(5)五氧化 2020-04-11 …
1987年2月,朱经武教授等发现钇钡铜氧化合物在温度90K下即具有超导性,若该化合物的基本结构单元 2020-04-27 …
学好化学符号是学习化学的关键,用化学符号填空:(1)硅元素;(2)2个铜原子;(3)3个氯离子;( 2020-05-02 …
用元素符号或化学式表示1.2个铜原子2.带2个单位正电荷的钙离子3.二氧化硫4.硫化氢5.四氧化三 2020-05-14 …
氢氧化铁,氢氧化亚铁,氢氧化铜的化学式还有,氢氧化亚铜,氢氧化锌,氢氧化钡,氢氧化钾,氢氧化铝,氢 2020-05-16 …
Cu可以形成化合价为+2和+1的化合物,其中+1价化合物称为亚铜化合物.(1)写出下列物质的化学式 2020-07-12 …
一道初三化学题急死!写出碳在高温还原氧化铜的化学方程式,并计算使08g氧化铜完全还原,需要碳的质量至 2021-01-21 …
下面的能发生复分解反应嘛?,如果能就帮忙写下出来1.硝酸钡溶液和硫酸铜溶液2.氢氧化钡溶液和碳酸铜溶 2021-02-01 …
写出下列反应的化学方程式:(1)用过氧化氢制氧气;(2)铜与硝酸银溶液反应:;(3)高温下水蒸气和氧 2021-02-13 …
按要求完成以下方程式:(1)SO2使溴水褪色的化学方程式:.(2)铜与稀硝酸反应的离子方程式:.(3 2021-02-13 …